Clear Sky Science · he
פיתוח מודל חמור של תסמונת הזנה מחדש בעכברים (עמיתים) ומידול מתמטי של היפופוספטמיה הנלווית
מדוע אכילה מחדש עלולה להיות מסוכנת
כאשר אנשים שסבלו מתת־תזונה חמורה מקבלים לבסוף מזון או תזונה תוך־ורידית, הרופאים צריכים לפעול בזהירות. גל פתאומי של קלוריות יכול להצית "תסמונת הזנה מחדש," סיבוך שמפר את מאזן המלח של הגוף ועלול לפגוע בלב, בשרירים ובריאות. שחקן מרכזי אחד הוא זרחן, מינרל הדרוש לאנרגיה בכל תא. מחקר זה השתמש בעכברים (חולדות) ובמידול ממוחשב כדי לגלות מדוע ריכוז הזרחן בדם עלול לקרוס כל‑כך דרמטית בזמן הזנה מחדש, וכיצד ייתכן שנמנע את הנפילה המסוכנת הזו.
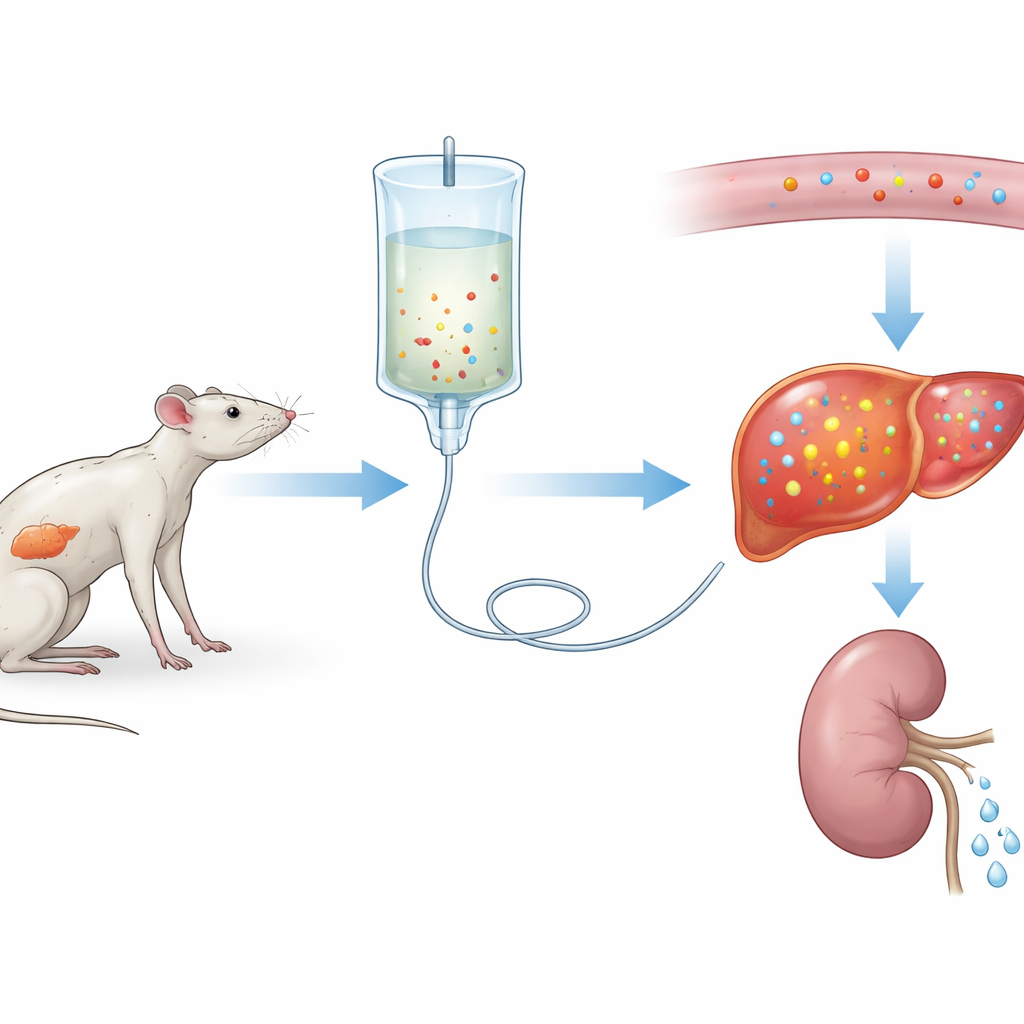
מבט קרוב על הבעיות בהזנה מחדש
החוקרים יצרו תחילה גרסה חמורה של תסמונת הזנה מחדש בחולדות. במשך שלושה שבועות קבוצה אחת קיבלה דיאטה רגילה בעוד קבוצה אחרת קיבלה כמות חלבון נמוכה מאוד, המדמה תת־תזונה ממושכת. בשתי הקבוצות ניתן לאחר מכן אותה תזונה תוך־ורידית למשך שלושה ימים. אצל החולדות שקיבלו דיאטה דלה בחלבון נרשמה ירידה חדה בזרחן בדם—כמוצע של כ‑75%—לצד שינויים במלחים אחרים וסימנים לפגיעה באיברים, במיוחד בכבד ובשרירים. שינויים אלה דמו לתסמונת הזנה מחדש חמורה במטופלים, מה שמרמז שהצוות בנה מודל ניסיוני מהימן.
מה קורה לזרחן במהלך ההזנה מחדש
כדי להבין כיצד זרחן נע בגוף לאורך זמן, המדענים לקחו דגימות דם ושתן חוזרות מאותן חולדות. הם מצאו שרמות הזרחן בדם ירדו גם בחיות הרגילות וגם באלו המושמנו מחלבון לאחר תחילת ההזנה, אך הירידה הייתה עמוקה וממושכת יותר בקבוצת החוסר תזונה. באופן מפתיע, הכליות דווקא הפחיתו את אובדן הזרחן בשתן מיד לאחר ההזנה, כך שהמינרל לא יועד להפטר ממנו. במקום זאת, הזרחן נספג מזרם הדם אל הרקמות, בראש ובראשונה אל הכבד, שבו מאגריו דוללו אחרי שבועות של דיאטה לקויה. חישובים ממוחשבים אישרו שהחולדות המושמזו החלו עם רמות פנימיות של זרחן בתאים נמוכות בהרבה ואז ספגו אותו בעוצמה כשהזינו אותן מחדש.
אינסולין אינו כל הסיפור
מכיוון שההזנה מחדש מעלה את סוכר הדם ואת הורמון האינסולין, רופאים האשימו זמן רב את האינסולין בדחיפת הזרחן לתאים. הצוות בדק רעיון זה על‑ידי דיכוי הפרשת האינסולין באמצעות ההורמון סומטוסטטין. כמצופה, סוכר הדם עלה, אך הצניחה בריכוז הזרחן בדם כמעט ולא השתפרה. במקביל עלו רמות חומצות אמינו חופשיות — אבני הבניין של חלבונים. בניסוי נפרד הוציאו את חומצות האמינו מההזלפה. כעת, רמות הזרחן נשמרו יציבות הרבה יותר והמכה החמורה נמנעה, אף על פי שרמות האינסולין היו דומות. ממצאים אלה מצביעים על אפקט משולב: גם אינסולין וגם חומצות אמינו, ולא האינסולין לבדו, דוחפים את התאים לקלוט כמות נוספת של זרחן במהלך ההזנה מחדש.
רשת בקרה נסתרת בכבד ובכליה
בהעמקה נוספת בחנו החוקרים חלבונים בכבד המעורבים בחישה של מזון, עם דגש על מסלול המכונה mTOR, המגיב לאינסולין ולחומצות אמינו. בחולדות בדיאטה דלה בחלבון, ההזנה מחדש הפעילה חזק מסלול זה והעלתה את רמותו של משנע זרחן בשם Pit2, שעוזר לתאי הכבד למשוך זרחן פנימה. התבנית התאימה להתנהגות שחזו במודל המתמטי שלהם, שקיבץ את הרשת הזו לאות בקרה יחיד שקראו לו "simTOR." המודל גם דרש גורם משוב נפרד כדי להסביר כיצד הכליות מתאמות את אובדן הזרחן בשתן. מדידות של הורמון מקור העצם, FGF‑23, התאימו לתפקיד זה היטב: רמותיו צנחו כאשר ההזנה החלה, מה שמגביל הפרשת זרחן, ואז הסתעפו בין החולדות הרגילות לאלו המחוסרות באופן שהשיק את אות המשוב המדומה.
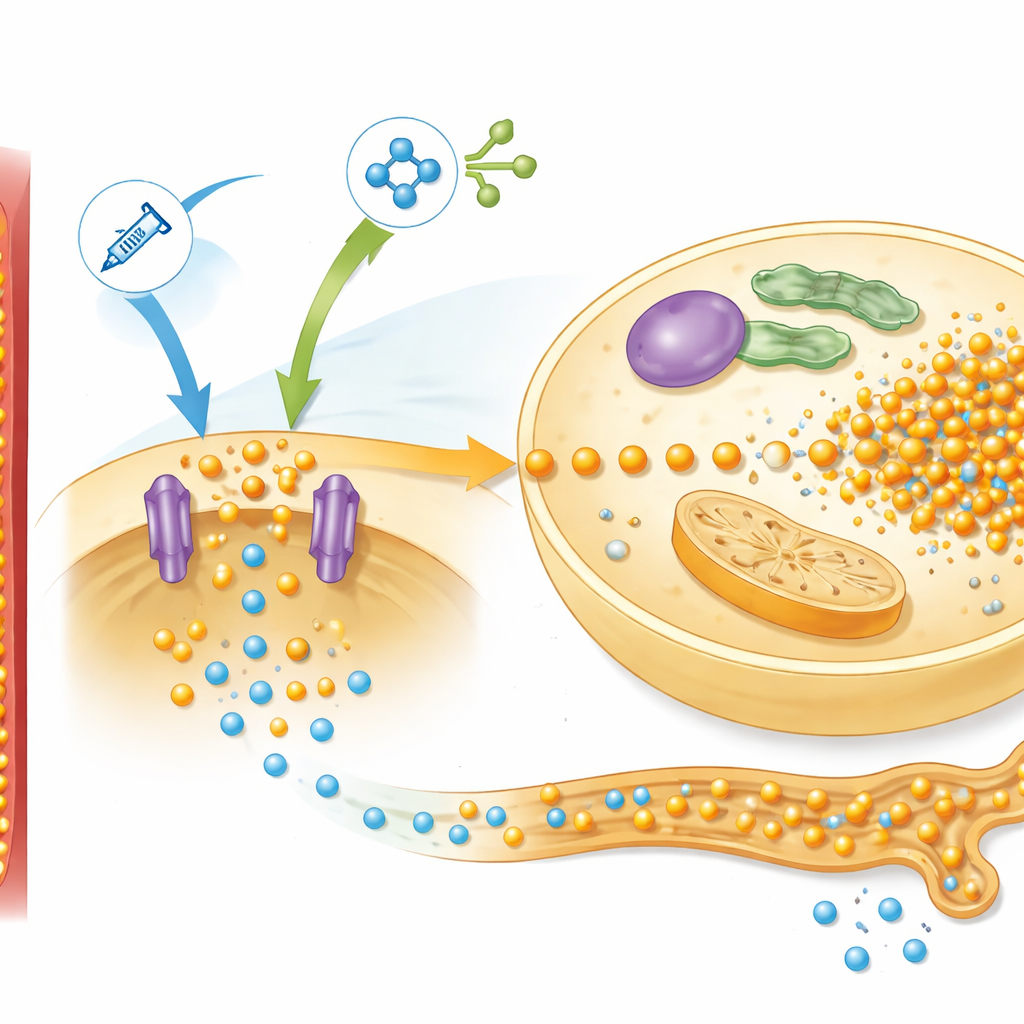
שימוש במתמטיקה לבחינת אסטרטגיות מניעה
על‑ידי כוונון פרמטרים שונים במודל הממוחשב שלהם, המחברים יכלו לשאול שאלות "מה אם" שקשה או מסוכן לבדוק ישירות בחולים. הניתוח הדגיש שלושה גורמים מרכזיים המשפיעים על עומק והחלמת צניחת הזרחן: רמות הזרחן התוך‑תאיות ההתחלתיות, עוצמת מערכת הקליטה המונעת על‑ידי mTOR, וקצב כניסת הזרחן מהתזונה. סימולציות הציעו כי הוספת כמות גדולה של פוספט במועד ההזנה מחדש תהיה קשה לאיזון בבטחה. עם זאת, מתן תוספת זרחן לפני ההזנה—שיאפשר לאיברים לבנות בשקט את מאגריהם הפנימיים—יכול להחליש את הקריסה מאוחר יותר ברמות הדם. הורדה בעומס חומצות האמינו, במיוחד אלה שמפעילות בעוצמה את mTOR והאינסולין, נראתה גם היא מגנית בניסויים על בעלי החיים.
מה משמעות הדבר עבור מטופלים
לאנשים בסיכון לתסמונת הזנה מחדש—כמו אלה עם הפרעות אכילה ממושכות או חולשה חמורה—העבודה הזו מצביעה שהסכנה נובעת מיותר מאשר רק קפיצה בסוכר הדם. איברים מושמזו נכנסים להזנה מחדש עם מכלי זרחן ריקים, ואז, תחת הדחיפה המשולבת של אינסולין וחומצות אמינו, סופגים במהירות את המינרל מהדם בעוד הכליות אוחזות בו לזמן קצר. התוצאה היא חוסר חמור וזמני במחזור הדם שעשוי לפגוע ברקמות חיוניות. המודל בחולדות והמסגרת המתמטית שפיתחו כאן מצביעים על מניעה ממוקדת יותר: שימוש מוקדם זהיר בתוספי זרחן, בקרה מדוקדקת של תזונה עשירה בחומצות אמינו, ותשומת לב להורמונים השולטים בהפרשת זרחן בכליות. ביחד, גישות אלה עשויות לסייע לרופאים להאכיל מטופלים פגיעים בצורה בטוחה יותר.
ציטוט: Kato, H., Yamaoka, I. & Kubota, H. Development of a severe rat refeeding syndrome model and mathematical modeling of the associated hypophosphatemia. npj Syst Biol Appl 12, 34 (2026). https://doi.org/10.1038/s41540-026-00658-7
מילות מפתח: תסמונת הזנה מחדש, היפופוספטמיה, מטבוליזם של זרחן, אותות mTOR, תזונה פראנטרלית