Clear Sky Science · he
FBA מרחבי חושף נישות וורבורג הטרוגניות בגידולי כליה וצריכת לקטט בסרטן המעי הגס
למה המטבוליזם של הגידול במרחב חשוב
תאי הסרטן אינם מתנהגים באותו אופן, גם בתוך אותו גידול. חלקם חיים קרוב לכלי דם, אחרים בעומק אזורים שניזונים מעט, והמיקומים האלה מעצבים כיצד הם משיגים ומשתמשים בדלק. המחקר הזה מציג שיטה חדשה לקרוא את ה"מפה המטבולית" החבויה מתוך נתוני ביטוי גנים מרחביים מתקדמים. בכך, המחברים חושפים דפוסים מפתיעים בדרך שבה גידולים שונים מתמודדים עם מולקולה מרכזית — לקטט — ואתגר לתפיסה הקלאסית שסוגי סרטן רק מופרשים לקטט כפסולת.
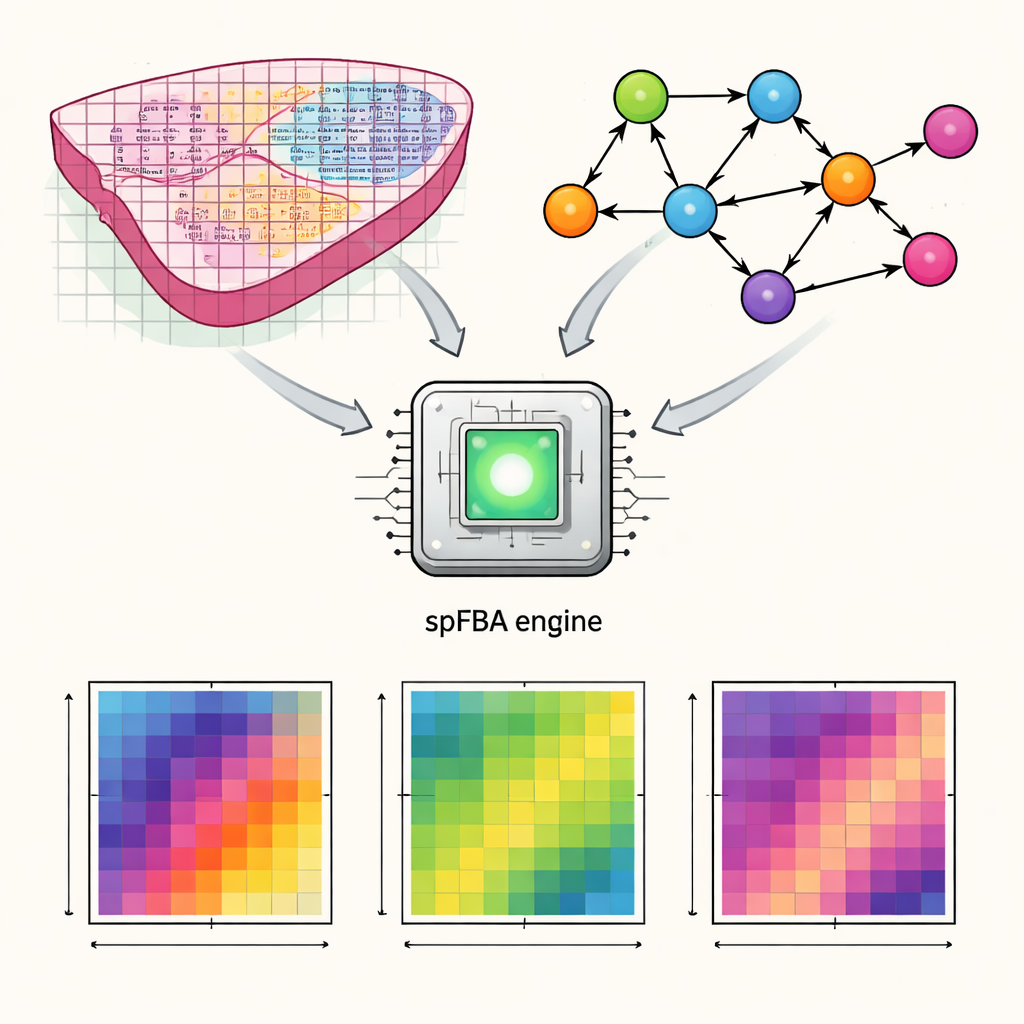
הפיכת מפות גנים לפעילות מטבולית
המחברים פיתחו מסגרת חישובית הנקראת spatial Flux Balance Analysis, או spFBA. טכנולוגיות טרנסקריפטומיקה מרחבית מודדות אילו גנים פעילים באלפי נקודות זעירות על פני חתך רקמה. spFBA משלבת את מפות פעילות הגנים המרחביות האלה עם מודלים מפורטים של מטבוליזם אנושי, שמתארים כיצד מזונות כמו גלוקוז, חמצן וחומצות אמינו מומרות בתוך התאים. במקום להניח שלכל אזור ברקמה יש את אותו מטרה מטבולית, spFBA מטפלת בכל נקודה בנפרד ובוחנת אילו דפוסי תגובה אפשריים שם על פי חוקי הכימיה ושימור המסה. הפלט הוא סט של "ציוני העשרת זרימה" שמצביעים, עבור כל מיקום, עד כמה תגובות מטבוליות שונות צפויות לזרום ובאיזו כיוון.
בדיקת השיטה בגידולי כליה
כדי לבדוק האם spFBA נותנת תוצאות ביולוגית הגיוניות, הצוות פנה תחילה לסרטן הכליה מסוג clear cell renal cell carcinoma, גידול כליה הידוע בתלותו המוגברת בפירוק סוכר (גליקוליזה) ובשחרור לקטט — תופעה המכונה אפקט וורבורג. באמצעות נתונים מרחביים מפורסמים מעשרה דגימות של גידולי כליה, הם בדקו האם הדפוסים המטבוליים החזויים תואמים את המבנה ההיסטולוגי של הרקמה. הם מצאו שנקודות שמקובצות לפי הזרמים המטבוליים שחזו מתיישבות היטב עם הארגון ההיסטולוגי שמתחת למיקרוסקופ וכן עם אשכולות המבוססים רק על ביטוי גנים. באופן חשוב, spFBA שחזרה את הקונטרסט המטבולי הצפוי בין רקמת הגידול לבין הכליה התקינה: אזורים סרטניים הראו שימוש גבוה יותר בגלוקוז, ייצור ביומסה חזק יותר (מעין מדד לגידול תאי), ושילוח לקטט בולט. יחד עם זאת, צריכת חמצן נשארה משמעותית, מה שמראה שחלקים שונים באותו גידול יכולים לשלב התסיסה והנשימה בהתאם לאספקת הדם המקומית.
סרטן המעי הגס מספר סיפור לקטט שונה
החוקרים אז החילו את אותה דרך עבודה על מערכי נתונים מרחביים ברזולוציה גבוהה מחולה עם סרטן המעי הגס הראשוני וגרורות כבד תואמות, וכן על ערכת נתונים ציבורית עצמאית של סרטן המעי הגס שנוצרה באמצעות טכנולוגיה אחרת. כאן התוצאות היו שונות באופן מרשים. במקום לייצא לקטט כפסולת, רוב אזורי סרטן המעי הגס — הן בגידול המקורי במעי והן בגרורות בכבד — חזו כיבואני לקטט מהסביבה. תאי הרקמה התומכת (stromal) סמוכים נטו לשחרר כמויות קטנות של לקטט, בעוד תאי הגידול פעלו כיוצאי צרכנים חזקים. באמצעות מעקב אחרי דפוסי זרימה ברמת התגובות, המחברים מראים כי התאים המתקדמים בגרורות אינם פשוט שורפים לקטט במחזור האנרגיה המיטוכונדריאלי הרגיל. במקום זאת, הם ממירים לקטט לחומרי גלם שנשזרים לנתיבים לבניית שומנים ורכיבים אחרים הדרושים לגידול תאי — "אפקט וורבורג הופכי־סמלי" שבו לקטט הופך לחומר גלם לביוסינתזה.
נישות מטבוליות וחזית הגידול-סטומה
מכיוון ש‑spFBA שומרת על הסידור המרחבי, היא יכולה למקם בדיוק היכן מתרחשים חילופי מטבוליטים מסוימים. בגידולי כליה השיטה גילתה "שכונות" מטבוליות שונות שחיות לצדם: ממשקים עשירי דם וחמצן שבהם תאי הסרטן גם נושמים וגם מתסיסים, וליבות עמוקות עם אספקת דם ירודה שתלויות יותר בהתססה. בגרורות כבד של סרטן המעי הגס, spFBA הדגישה קונטרסטים חדים בגבול בין גידול לסטומה, שם ניהולם של גלוטמט ולקטט השתנה כיוון, דבר שמעיד על חילוף אינטנסיבי בקדמת החדירה. בכל מערכי הנתונים חזו הזרמים הקשורים לצמיחה התאמתו למדידות עצמאיות מבוססות גנים של פרוליפרציה, תומכות בריאליזם הביולוגי של המודל. קריטי מכך — אותו אלגוריתם חזה הפרשת לקטט בסרטן הכליה אך קליטת לקטט בסרטן המעי הגס, מה שמעיד שההבדלים שנצפו נובעים מהנתונים ולא מהטיה מובנית של המודל.
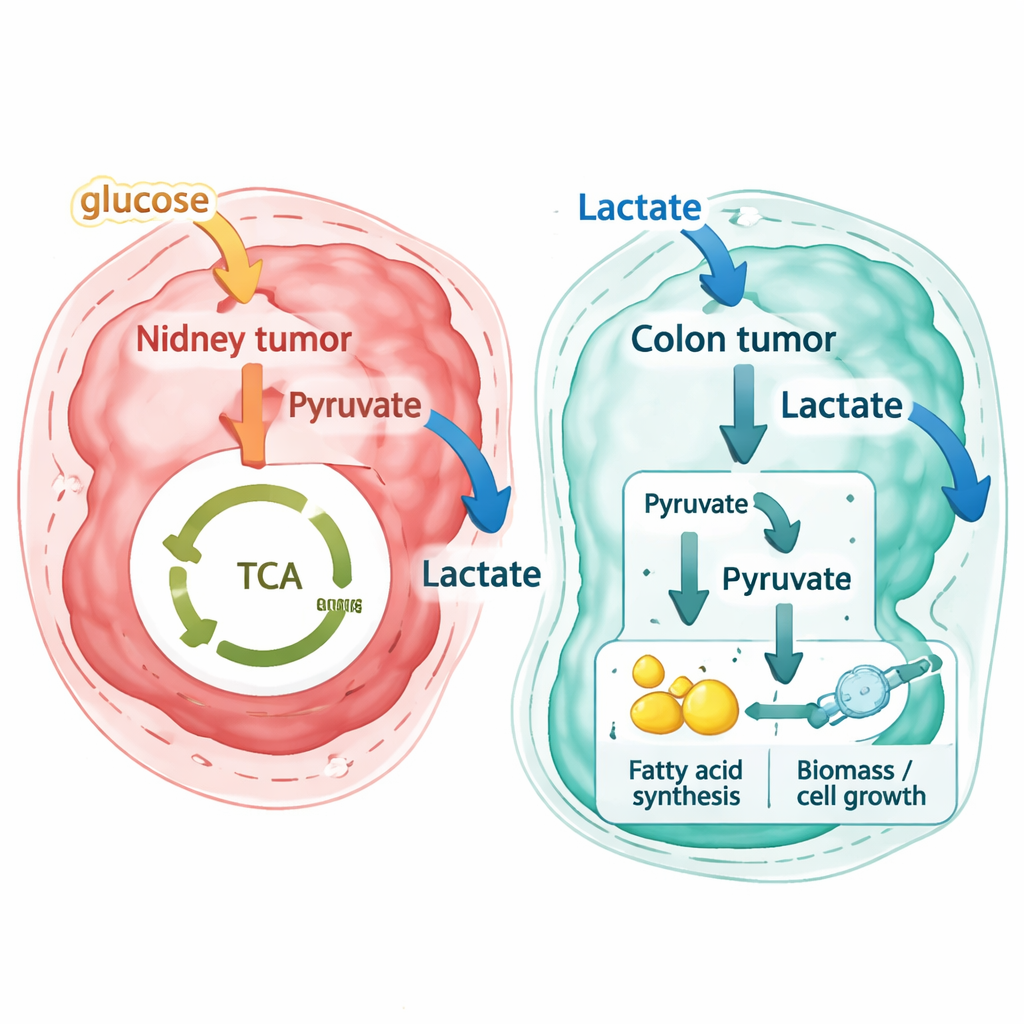
מה זה אומר להבנה וטיפול בסרטן
ללא־מומחים, המסר העיקרי הוא שמטבוליזם הגידול אינו רק חריג — הוא ממוקם מאוד. אותו גידול יכול להכיל נישות מטבוליות מרובות, וגידולים שנראים דומים באיברים שונים עשויים להשתמש באותן מולקולות בדרכים מנוגדות. עבודה זו מראה כי על ידי שיכבות של ביטוי גנים מרחבי מעל מודלים מטבוליים מפורטים, חוקרים יכולים להסיק היכן גידולים צפויים להיות רעבים לחומרי תזונה מסוימים כגון לקטט. בסרטן המעי הגס, גילוי שהתאים הסרטניים צורכים לקטט במידה נרחבת ומנתבים אותו לתהליכי צמיחה מעלה שאלות חדשות על האופן שבו תזונה, חיידקי המעי ומטבוליזם הכבד מעצבים התקדמות המחלה, והאם חסימת ניצול הלקטט עשויה להפוך גידולים אלה לפגיעים יותר לטיפולים.
ציטוט: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
מילות מפתח: מטבוליזם של סרטן, טרנסקריפטומיקה מרחבית, לקטט, אפקט וורבורג, סרטן המעי הגס