Clear Sky Science · he
ד‑מודולציה של התמחות האנדודרם הקדמי לכיוון זרעוני אפיתל הריאה
הפיכת תאי גזע לתאים שבונים ריאות
מדענים לומדים כיצד לעודד את תאי הגזע של המטופל עצמו להפוך לרקמה ריאתית חליפית, שעשויה יום אחד לתקן נזקים ממחלות כמו COPD, פיברוזיס או זיהומים חמורים. מאמר זה בוחן כיצד חוקרים השתמשו במודל ממוחשב כדי למפות ולכוון שלב חשוב במסע הזה: המרת סוג תווך של תאים, שנקרא אנדודרם קדמי, לזרעוני אפיתל ריאתי מוקדמים — התאים ההתחלתיים שיכולים בסופו של דבר להקים את דרכי הנשימה ושחלות האוויר של הריאה.
מדוע תאי התחלת ריאה חשובים
תאי גזע מושרים פלוריפוטנטיים אנושיים (iPSCs) ניתנים לתכנות מחדש מרקמות בוגרות ואז להיגרם לכיוונים של איברים שונים. כדי לבנות רקמת ריאה, תאים אלה עוברים תחילה מספר נקודות פיתוח. אחת מהן היא האנדודרם הקדמי, שכבת רקמה שבדרך כלל מתפתחת בחיידק לחלקים של מערכות הנשימה והעיכול בעובר. משם, באמצעות אותות כימיים נכונים, תאים יכולים להפוך לזרעוני אפיתל ריאתי, הנושאים סמני ריאה מוקדמים ויכולים בשלב מאוחר יותר לבגר לתאים ממוקדים של דרכי הנשימה או שלנאות האוויר. מאחר ותרפיות תאית עתידיות יידרשו מיליארדי תאים כאלה, החוקרים זקוקים לשיטות שיגדילו באופן אמין תשואות ויסתגלו לפרוטוקולים של קווי תאים שונים ללא ניסוי וטעייה בלתי נגמר במעבדה.
בניית גרסה וירטואלית של התמיינות תאית
הצוות הרחיב מסגרת מתמטית קודמת כדי לבנות, לפי ידיעתם, את המודל ברמת האוכלוסייה הראשון של המעבר הספציפי הזה מאנדודרם קדמי לזרעוני ריאה. הם שקלו שתי דרכים לייצג את התאים: גרסה פשוטה העוקבת רק אחרי המספר הכולל של תאים חיים, וגרסה מפורטת יותר העוקבת בנפרד אחרי תאי האנדודרם הקדמי וזרעוני הריאה. בשני המקרים המודל גם עוקב אחרי גלוקוז ולקטט במדיום התרבית, המייצגים מזון ופסולת. באמצעות כלים מביולוגיה מערכותית, החוקרים בנו מספר רב של משוואות מועמדות לאופנים שבהם תאים גדלים, מתים ומתמיינים, ואז השתמשו במבחני זיהוי פרמטרים כדי לפסול מודלים שהפרמטרים שלהם לעולם לא יכלו להיות מוגדרים אפילו עם נתונים מושלמים.
עיצוב ניסויים חכמים יותר בעזרת המודל
במקום רק להתאים את מה שנתונים זמינים במקרה, החוקרים אפשרו למודל להנחות כיצד יש לבצע ניסויים חדשים. הם השתמשו בנתונים מדומים כדי לשאול באיזו תדירות יהיה צורך למדוד מספר תאים ורמות מזון על מנת לאמוד נכון את פרמטרי המודל, תוך איזון בין דיוק סטטיסטי לבין עלות ועבודה של דגימה תכופה. זה הוביל לתוכנית מעשית: מדידות יומיות לגלוקוז וללקטט, וספירות תאים כל יום עד יומיים, בארבעה תנאים שהשתנו לפי קושי פיצול התרביות ביום העשירי והאם מדיום הגידול הוחלף יומיום. לאחר מכן הם ערכו ניסויים אלה, ומדדו גם את כל אוכלוסיית התאים וגם, באמצעות ציטומטריה בזרם, את החלקים שנותרו תאי אנדודרם או שהפכו לזרעוני ריאה.
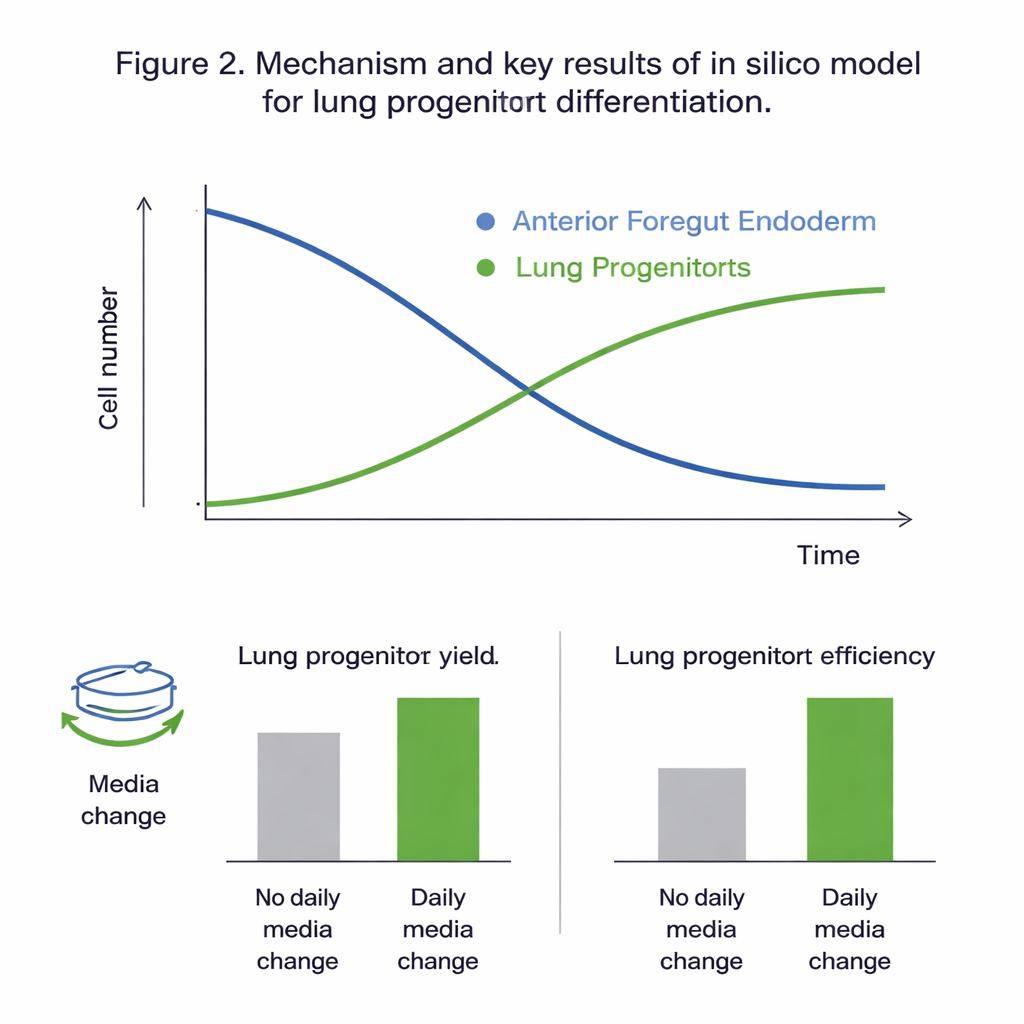
מה גילו הניסויים הווירטואליים
התאמת כל המודלים המועמדים לנתונים הניסיוניים הראתה שהמודל בעל שתי האוכלוסיות, שעוקב נפרד אחרי תאי אנדודרם וזרעוני ריאה, ניתן לכוונון באופן אמין ותיאר הכי טוב את ההתנהגות הנצפית. בדיקות סטטיסטיות הצביעו שבחלון הזמן הנחקר (ימים 11 עד 15 בפרוטוקול), הדינמיקה הונעתה בעיקר על ידי התרבות והתמיינות תאי האנדודרם, בעוד שהתרבות של הזרעונים עצמם תרמה מעט. ניתוח רגישות גלובלי חיזק תמונה זו, והבליט את שיעורי הגידול, המוות וההתמיינות של תאי האנדודרם — וכן את השפעת הגלוקוז — כידיות העיקריות השולטות בתוצאה. המודל הכיול שיחזר נתונים שלא נצפו בעבר עם שגיאות השוות עד למידת התזוזה הטבעית של הניסויים, מה שמרמז שהוא מדויק דיו כדי לחקור תרחישי "מה-אם" באופן in silico.
אופטימיזציה של החלפות מדיום ופיצול תאים
עם מערכת וירטואלית מהימנה ביד, הצוות בחן כיצד שתי בחירות פרוטוקול מעשיות משפיעות על התוצאות: כמה התרבית מדוללת (שיעור הפיצול) ביום העשירי, והאם מדיום הגידול מוחלף מדי יום. הסימולציות חזו שהחלפות מדיום יומיות מכפילות כמעט את מספר תאי הזרעון ואת התשואה לכל תא התחלתי, בעיקר על ידי מניעת פילוח המזון והצטברות פסולת ומולקולות איתות לא יציבות. הניסויים הסכימו בקירוב עם תחזיות אלה. המודל גם הציע ששיעורי פיצול גבוהים יותר — פיזור צמיחה דליל יותר ביום העשירי — משפרים את "התשואה לכל תא קלט" בכحوּר של כרבע, אף על פי שהם מקטינים את המספר המוחלט של התאים. בשני המקרים שינויים אלה השפיעו מעט על האחוז הסופי של זרעוני הריאה בתרבית, והם בעיקר זזו את כמות התאים שניתן לייצר ביעילות.
מה משמעות הדבר לתרפיות ריאה בעתיד
עבור קורא שאינו מומחה, המסר המרכזי הוא שהמחברים בנו מעין סימולטור טיסה לשלב קריטי בגדילת תאי ריאה מתאי גזע. באמצעות שילוב של ניסויים מתוכננים בקפידה עם מודלים מתמטיים מחמירים, הם מראים כיצד בחירות פרוטוקול פשוטות — כמו תדירות החלפת המדיום והצפיפות בה נזרעים התאים — יכולות להשפיע באופן דרמטי על כמות התאים שבונים ריאה שיוצרו, מבלי לשנות את איכותם. סוג זה של מודלינג in silico יכול לסייע בייעול פרוטוקולים עתידיים, לצמצם ניחוש ניסויי, ולבסוף לתמוך בייצור אמין וניתן להרחבה של זרעוני ריאה למחקר, להדמיית מחלות, ובסופו של דבר להשחזית שיקומית.
ציטוט: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
מילות מפתח: תאי אבות ריאתיים, תאי גזע מושרים פלוריפוטנטיים, מודלינג במחשב (in silico), התמיינות תאית, רפואה שחזורית