Clear Sky Science · he
עיכוב CDK8 מציל ריפוי שברים איסכמי מוחלש
למה אספקת הדם חשובה כשעצמות נשברות
ברוב המקרים שברים בעצמות מתאחה בהדרגה, אך אצל מיליונים מדי שנה התהליך נעצר. אספקת דם לקויה סביב השבר — מצב המכונה איסכמיה — מגדילה משמעותית את הסיכון שהשבר יתאחה לאט, בצורה לקויה או כלל לא. במחקר זה נבדק מדוע זה קורה ברמה התאית ונבחן כדור ניסיוני שנראה כמכוון את הגוף הרחק מתיקון בצורת צלקת וחזרה אל שיקום עצם אמיתי.
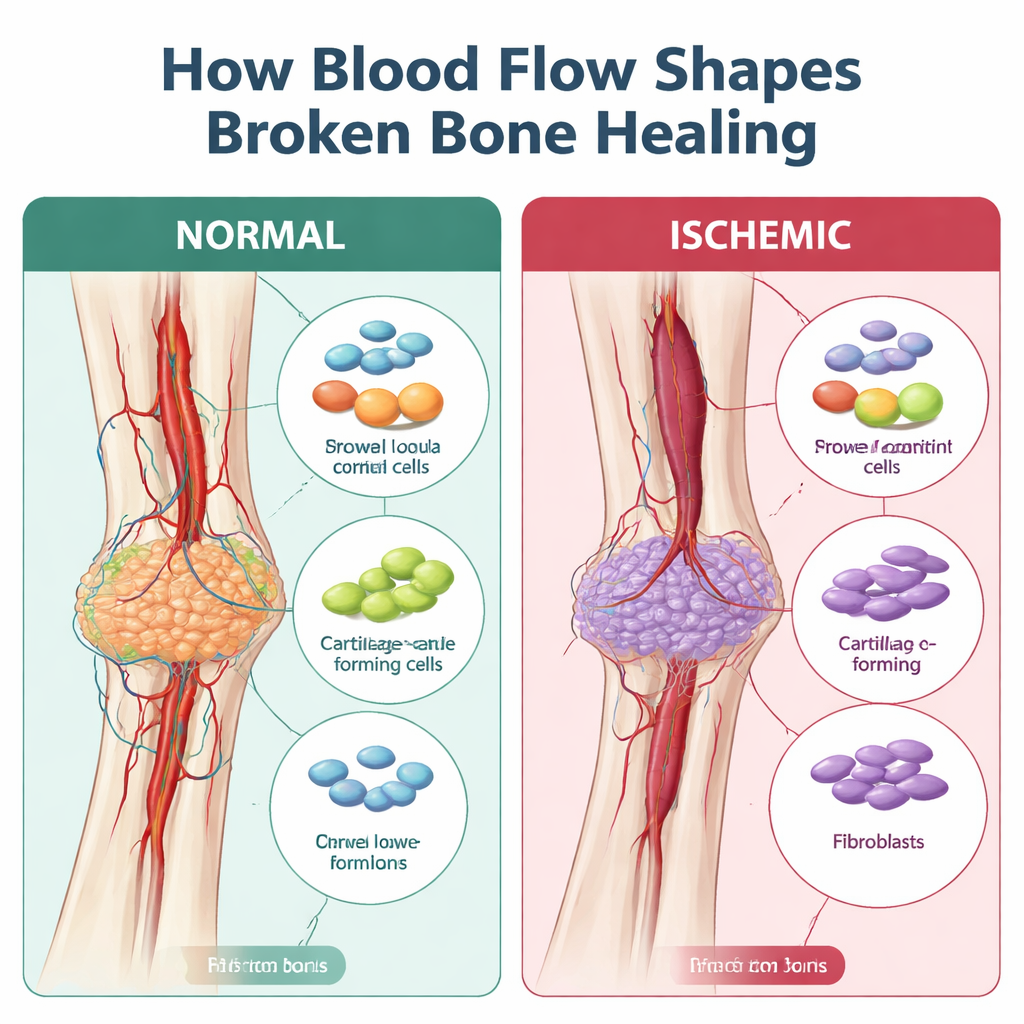
כשריפוי הופך לצלקת במקום לבנייה מחדש
במצב תקין העצם מתרפאת על ידי בניית גשר רך של סחוס שמוחלף בהדרגה בעצם קשה. גשר זה, שנקרא קלוס, מסתמך על אספקה של תאי תמך דמויי-עמוד שדרה (stem-like), תאי חיסון וכלי דם שמתואמים לתהליך התיקון. בשברים איסכמיים מחקרים מוקדמים הראו שהקלוס נוטה להיות קטן יותר, חלש יותר ומלא ברקמה סיבית, יותר כמו צלקת ופחות כמו טלאי חדש וחזק של עצם. מה שהיה חסר הוא מפת פירוט של אילו תאים משתבשים, ומתי, במהלך הסטייה הזו מריפוי תקין.
תאים בודדים חושפים סטייה לצלקתיות
החוקרים השתמשו במודל עכבר שבו עורק ברגל מוציאים ממנו דם בניתוח בזמן השבר, מה שמחקה מקרוב את אובדן אספקת הדם הנראה בפציעות חמורות או באנשים עם מחלות כלי דם או מעשנים. לאחר מכן הם יישמו רצף RNA בתא בודד, טכניקה שקוראת את הגנים הפעילים באלפי תאים בודדים, על קלוסים של השבר ארבע ושבעה ימים לאחר הפציעה. בשברים עם אספקת דם תקינה, הקלוס המוקדם היה מלא בתאי חיסון שלימים נתנו מקום להתרחבות תאי סטרומה — תאי התמיכה שהופכים לסחוס ועצם. בתנאי איסכמיה, לעומת זאת, היו הרבה פחות תאים שיוצרים סחוס ועצם והרבה יותר פיברובלאסטים, התאים שמניחים רקמה סיבית. ניתוח מסלול חישובי הראה שבתוך כך, במקום להתפתח בצורה חלקה ממחוללי תאים מוקדמים לסחוס, תאי הסטרומה בעצם איסכמי לעתים סטו דרך מצב דמוי-פיברובלאסט, תואם את הקלוס הדמוי-צלקת שנראה במיקרוסקופ.
בלם מולקולרי על תאי בניית העצם
בחינת פעילות הגנים בתאים אלה חשפה אות חזקה של מתח תאי בקלוסים איסכמיים, כולל רמות גבוהות של חלבוני חום (heat shock). אחד השינויים הבולטים היה עלייה בפעילות של גן בשם Cdk8, המקודד אנזים רגולטורי שנמצא במורכבות שעתוק מרכזית ויכול להאט או להפנות מחדש את אופן תגובת התאים לאותות. ידוע ש-Cdk8 חוסם התמיינות תאים בהקשרים אחרים. כאן הוא היה מוגבר במיוחד במחוללי סטרומה מוקדמים בעצם איסכמית. תאי סטרומה מזנכימליים אנושיים שגודלו במעבדה בתנאי חמצן נמוך — המדמים אספקת דם לקויה — גם העלו את רמות CDK8, וקישרו את חוסר החמצן ישירות ל"בלם" האפשרי הזה על יצירת סחוס ועצם.
כיבוי CDK8 לשיקום התיקון
החוקרים שאלו האם חסימת CDK8 יכולה לאפשר לתאי הסטרומה לשוב ולשקם כראוי. בתרבית תאים, טיפול בתאי מחולל עכבר ואדם עם מעכבים סלקטיביים של CDK8 הגביר גנים מרכזיים של סחוס והגביר את ייצור מטריצת הסחוס, וכמו כן שיפר הסתיידות כאשר אותם תאים הוכוונו להפוך לעצם. הצוות גם בדק מעכב CDK8/19 נלקח דרך הפה בשם SNX631-6 בעכברים עם שברים איסכמיים. כאשר ניתן במהלך החלון המוקדם של יצירת הסחוס, התרופה הגדילה את כמות הסחוס בקלוס. כאשר הטיפול הוארך לשלב המאוחר של המעבר מסחוס לעצם, הקלוסים הראו יותר עצם כולל, תוכן מינרלי גבוה יותר וגודל כולל גדול יותר בסריקות מיקרו-CT ובחתכי רקמה, דבר שמעיד על שיקום מבני חזק יותר.
מידע ממעבדה לטיפולים אפשריים בעתיד
במכלול, התוצאות מצביעות על כך שאיסכמיה מנווטת את תאי הריפוי לגורל לחוץ וצלקתי בחלקו על ידי הגברת CDK8, שמגבילה את יכולתם להפוך לסחוס ולעצם. חסימת האנזים הזה נראית משחררת את ה"הבלם", ומאפשרת יצירת סחוס שיותר בשלב המוקדם ונדידת עצם רבה יותר בשלב המאוחר, גם כאשר אספקת הדם פגועה. מכיוון שמעכבי CDK8 כבר נבדקים אצל חולי סרטן, יתכן שיום אחד יימצא שימוש מחודש בהם כדי לסייע לאנשים בסיכון גבוה לריפוי לקוי של שברים — כגון קשישים, מעשנים או חולי מחלות כלי דם — לגדל עצם חזקה במקום רקמת צלקת שבירה.
ציטוט: Capobianco, C.A., Song, M.J., Farrell, E.C. et al. Inhibition of CDK8 rescues impaired ischemic fracture healing. npj Regen Med 11, 12 (2026). https://doi.org/10.1038/s41536-026-00456-z
מילות מפתח: ריפוי שבר בעצם, איסכמיה, מעכב CDK8, תאי מזנכימה סטרומליים, צלקתיות