Clear Sky Science · he
המוטציה LRRK2R1627P מגדילה גורמי סיכון סביבתיים הגורמים לדלקת כרונית והצטברות α-סינוקלאין במעיים של חולדות
מדוע המעי חשוב במחלת מוח
מחלת פרקינסון ידועה בעיקר ברעידות ובעיות בתנועה, אך עדויות מתגברות מצביעות על כך שהשורשים שלה עשויים להתחיל רחוק מהמוח, עמוק במעי. מחקר זה בוחן כיצד שינוי גנטי ספציפי מקושר לפרקינסון באוכלוסיות אסייתיות יכול, יחד עם הזדקנות וחשיפה לרעלים, לפגוע בהדרגה במעי של חולדות. על ידי מעקב אחרי האירועים במעי לאורך חיי הח الحيوانات, החוקרים מציירים כיצד מנגנוני הגנה חיסוניים שגרתיים עלולים להיסחף לדלקת כרונית, וליצור קרקע להצטברות חלבונים הקשורים למחלה שעשויה בסופו של דבר לאיים על המוח.
גֵן מסכן במערכת העיכול
המדענים התמקדו בגרסה של גן בשם LRRK2, המזוהה מזה זמן עם מחלת פרקינסון ומצבים דלקתיים של המעי. הם יצרו חולדות הנושאות את המוטציה המקבילה, שנקראה LRRK2R1627P, והשוו בינן לבין חולדות תקינות לאורך החיים. על אף שלא נמצא שינוי בכמות ה-mRNA של LRRK2 במעי, חלבון LRRK2 הכולל ואחד הסמנים המרכזיים לפעילותו ירדו, מה שמעיד שהמוטציה מחלישה את תפקוד החלבון במעי. שינוי מולקולרי עדין זה לא גרם לנזק דרמטי מוקדם, אך שינה באופן שקט את האופן שבו תאי המעי מתחדשים ומסודרים ככל שהחיות התבגרו.
מעי מזדקן תחת עומס איטי ומתמשך
ככל שעברו חודשים, בחולות עם המוטציה התפתחותהן סימנים ברורים של מבנה מעי מופרע. המעי הדק התקצר, והבליטות הדקות והאצבעיות (ווילים) והשקעים (קריפטים) שסופגים חומרים מזינים התקצרו. תאים מיוחדים ברירית המייצרים ריר וחומרים אנטי-מיקרוביאלים — תאי גבלט ותאי פנאת — ירדו במספרם, בעוד שחלבונים המסייעים לתאים שכנים ליצור צמתי הדוק חסיני דליפה גם הם פחתו. תחת המיקרוסקופ צמתי ההדוק הללו נעשו קצרים יותר או רחבים יותר, דבר שמרמז על מחסום מוחלש. חשוב לציין שהאדריכלות הכוללת לא התמוטטה; במקום זאת, המעי הציג דפוס מתגנב של חידוש והגנה מופחתים, מה שעלול להפוך אותו לפגיע יותר לגירוי ולהדבקה. 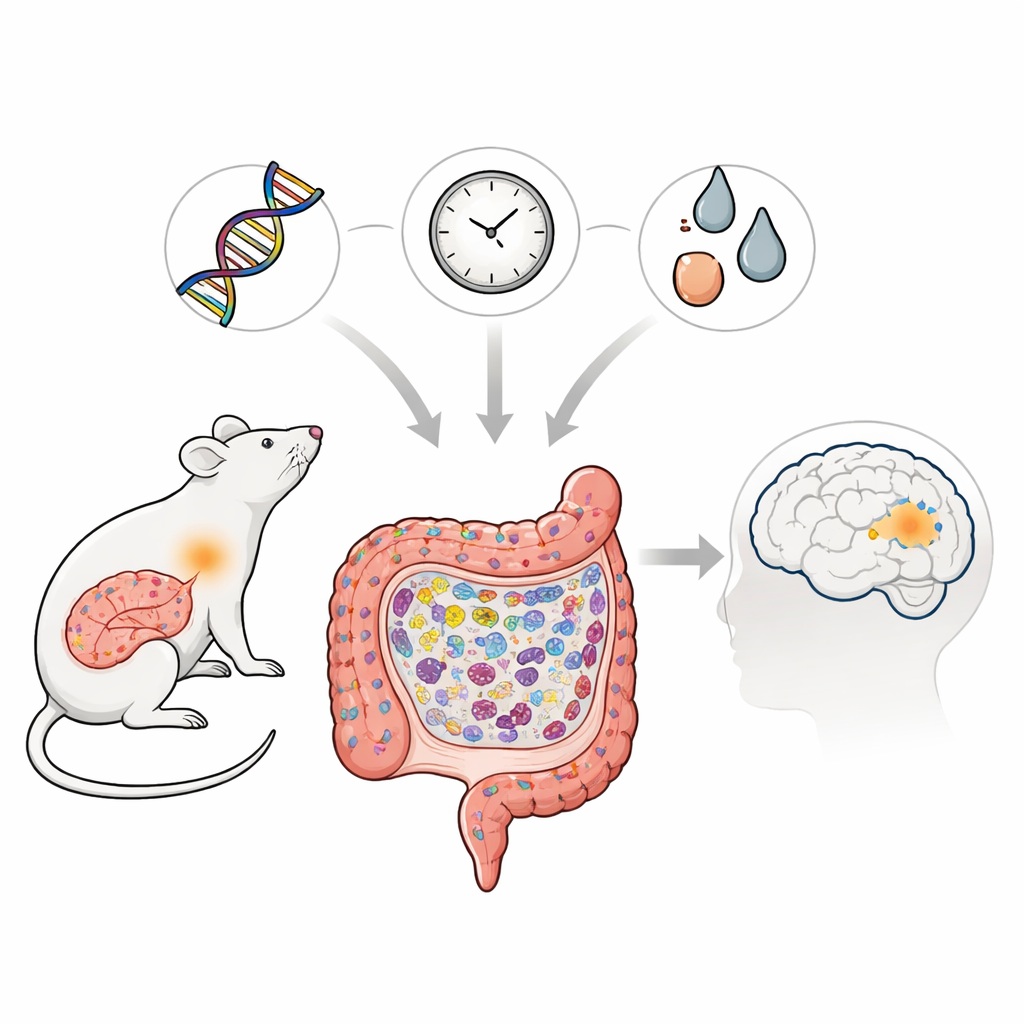
מערכת החיסון על קצה הגירוי
כדי להבין מדוע המעי איבד את האיזון, הקבוצה בדקה פעילות גנים ותאי חיסון בדופן המעי. הם מצאו כי דרכי איתות הקשורות לחיישן שנקרא TLR4 ולבן זוגו NF-κB היו פעילות יתר בחולדות בוגרות עם המוטציה. חיישנים אלה בדרך כלל עוזרים לגוף לזהות מיקרובים מזיקים, אך כאן הם הובילו להצטברות של תאים חיסוניים מסוג "הלחם-ראשון" הידועים כמקרופאגים M1. תאים אלה ייצרו מולקולות דלקתיות, והפכו את המעי לסביבה מגרה כרונית. באופן בולט, החלבון הקשור לפרקינסון α-סינוקלאין, בצורתו המופוספורלת הקשורה למחלה, החל להצטבר לא בתאי עצב במעי אלא בתוך מקרופאגים פעילים אלו במעי הדק, במיוחד בחיות מבוגרות.
רגישות מוגברת לפגיעות סביבתיות
המוטציה הגנטית לבדה לא הייתה הסיפור השלם. כאשר חולדות צעירות חשופות לזמן קצר לרעלני חיידקים (LPS), המפעילים את TLR4, חיות עם המוטציה ב-LRRK2 פיתחו דלקת מעיים חמורה הרבה יותר מאשר מקביליהן התקינות. הרירית המעי שלהם השליכה יותר תאים, חלבוני המחסום ירדו עוד יותר, ומקרופאגים פרו-דלקתיים צצו בשפע, שוב מצטברים עם α-סינוקלאין בלתי תקין. ממצאים אלה מרמזים שאנשים הנושאים מוטציות דומות עלולים להיות רגישים במיוחד לפגיעות סביבתיות שמטרידות את המעי, כגון זיהומים או רעלנים מסוימים, וכך להגביר את הסיכון שלהם בטווח הארוך.
כיבוי אות האזעקה
מאחר ש-TLR4 עמד במרכז הסערה הדלקתית הזו, הקבוצה בדקה תרופה, TAK-242, שמעכבת באופן ספציפי את איתות TLR4. במתן במשך כמה חודשים לחולדות בגיל בינוני, המעכב שיחזר ברובו את אורך המעי הדק, את גודל הווילים והקריפטים, את תאי המייצרים ריר וחלבוני המחסום. הוא הקטין את המקרופאגים הפעילים, הוריד מולקולות דלקתיות והפחית בצורה חדה את הצטברות α-סינוקלאין הבלתי תקין במעי. במקביל, הטיפול תקן קהילת חיידקים מוטה: המגוון חזר לעלות, גדילה מופרזת של Lactobacillus פחתה, וקבוצות חיידקים מועילות התאוששו, בעוד שתפקודים מיקרוביאלים צפויים זזו הרחק מדפוסים הקשורים למחלה. 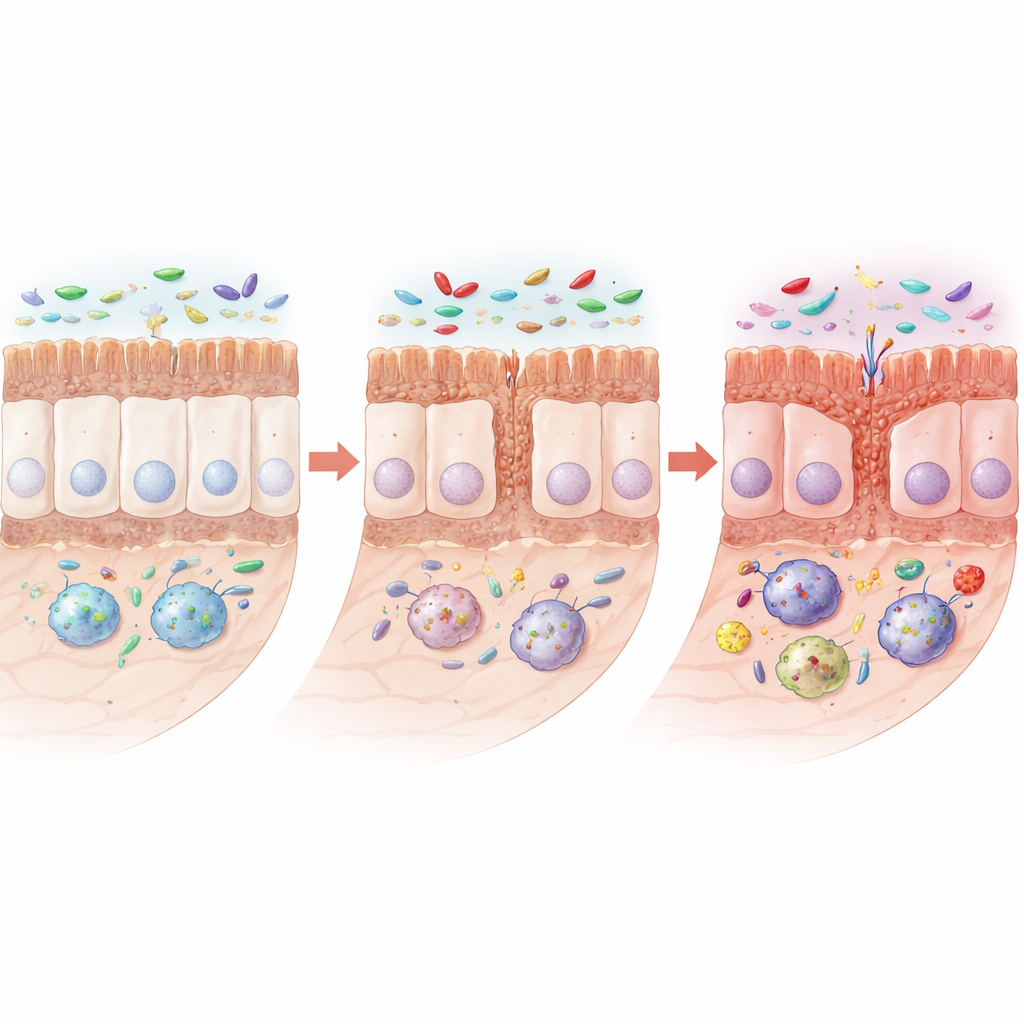
מה משמעות הדבר לגבי סיכון לפרקינסון
לאיש שאינו מומחה, המסר הוא ש"גן לפרקינסון" יכול לעצב בשקט את הגנות החיסון של המעי לאורך זמן, במיוחד בנוכחות הזדקנות ולחץ סביבתי. בחולדות אלו, התוצאה היא דלקת כרונית ברמה נמוכה שמחלישה את מחסום המעי, מחריגה את המיקרוביוטה המקומית וגורמת לחלבון הקשור לפרקינסון להצטבר בתאים חיסוניים — לא פרקינסון בשלב מלא, אך סביבה ביולוגית שעשויה להעדיף מחלת מוח בהמשך. בכך שהם מראים שעיכוב של מסלול חיסוני יחיד במעי יכול להסתיר שינויים רבים אלה, המחקר מדגיש את המעי כמטרה פרקטית מוקדמת: הגנה על בריאות המעי וכיבוי הדלקת בו עשויים לסייע בעיכוב או מניעת פרקינסון באנשים הנושאים סיכונים גנטיים.
ציטוט: Pang, S., Lu, J., Wang, Y. et al. LRRK2R1627P mutation amplifies environmental risk factors induced chronic inflammation and α-synuclein aggregation in the gut of rats. npj Parkinsons Dis. 12, 68 (2026). https://doi.org/10.1038/s41531-026-01281-3
מילות מפתח: מחלת פרקינסון, דלקת מעיים, מוטציה ב-LRRK2, מיקרוביום, חיסון מולד