Clear Sky Science · he
הערכה מערכתית של מבקרי המורפולוגיה המיטוכונדריאלית לשיפור אלפא‑סינוקלינופתיה נוירונלית
למה תחנות הכוח הקטנות חשובות במחלות מוח
המיטוכונדריה, "תחנות הכוח" של התא, חיוניות לשמירה על חיי התאים העצביים ועל תפקוד הקשרים ביניהם. בהפרעות מוחיות כמו מחלת פרקינסון, מבנים זעירים אלה לעתים קרובות נראים פגועים או מפורקים, אך קשה היה להבחין אילו שינויים מזיקים ואילו מהלכים אפשר לשנות בבטחה כדי להגן עליהם. מחקר זה בוחן באופן שיטתי רגולטורים מרכזיים של "צורת" המיטוכונדריה במודל מעבדה של הצטברות חלבון הקשורה לפרקינסון, תוך שימוש בכלי בינה מלאכותית למדידת צורת המיטוכונדריות בחלקים שונים של נוירונים. הממצא מצביע על רגולטור מסוים, הנקרא Fis1, כיעד מבטיח לשמירה על בריאות המיטוכונדריות — וכן על בריאות הסינפסות — מבלי ליצור תופעות לוואי חדשות.
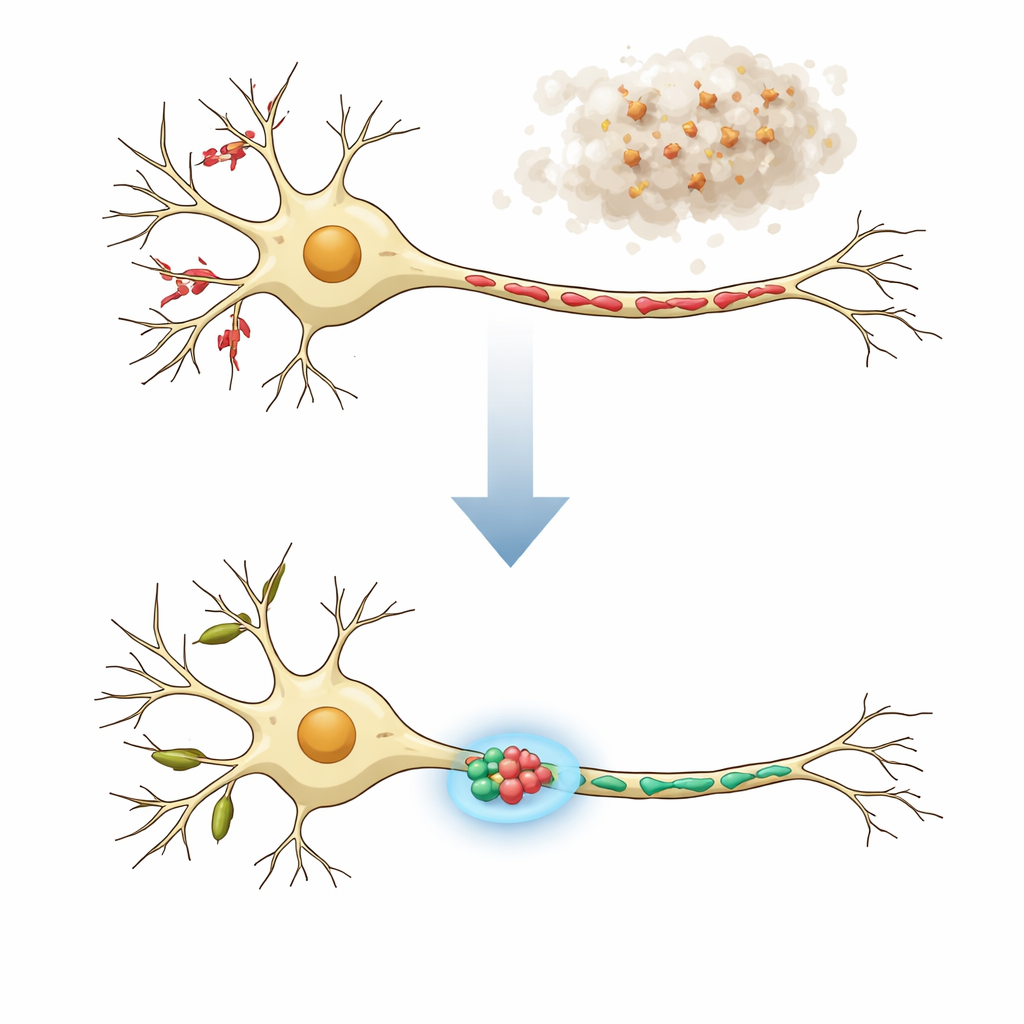
שני השכונות של תא מוח
נוירונים אינם אחידים: הענפים שלהם הדמויי עץ (דנדריטים) והכבלים הארוכים (אקסונים) מבצעים תפקידים שונים ומכילים מיטוכונדריות בצורות שונות מאוד. בתאים בריאים, בדנדריטים יש לרוב מיטוכונדריות ארוכות וצינוריות המסייעות בתמיכה בייצור חלבונים מקומי ובתקשורת גמישה בנקודות הקליטה הקרויות קוצים דנדוריטים. באקסונים, שמעבירים אותות, נמצאות לעומת זאת מיטוכונדריות רבות וקצרות המספקות אנרגיה ועוזרות לשלוט ברמות הסידן בטרמינלים הפרה‑סינפטיים. במחלות נוירודגנרטיביות, גם התפקוד וגם המבנה של מיטוכונדריות אלה יכולים להיפגע, והן מופיעות כקטעים, בצורות נפוחות או כמחרוזות גרגריות. המחברים ניחשו שטיפולים יעילים באמת חייבים להשיב את המיטוכונדריות בדנדריטים ובאקסונים לצורה התקנית המתאימה לכל מדור.
בניית מבחן־עומס בסגנון פרקינסון
כדי לחקות תכונה מרכזית של מחלת פרקינסון והפרעות קשורות, החוקרים חשפו נוירונים קורטיקליים של עכברים בתרבית לסיבי אלפא‑סינוקלין שעברו קיפול מראש (preformed fibrils), חלבון שיכול להצטבר וליצור אגגרגטים מזיקים. בתוך ימים ספורים, סיבים אלה זרעו הצטברות בלתי־נורמלית של אלפא‑סינוקלין בתאים והובילו לפיצול מיטוכונדריאלי בולט הן בדנדריטים והן באקסונים. באמצעות MitoVis, מערכת ניתוח תמונות מבוססת למידה עמוקה, הצליחה הקבוצה להפריד באופן אוטומטי דנדריטים מאקסונים בתמונות מיקרוסקופ ולמדוד את האורך, השטח והצורה של מאות מיטוכונדריות בתמונה — בקצב מהיר בערך פי עשר מציור ידני. גישה זו בקנה־מידה גבוה אישרה שהמצב הדמוי‑מחלה קיצר את המיטוכונדריות והפך אותן לעגולות יותר, בהתאם לדיווחים ממודלים של בעלי חיים ורקמות מטופלים.
בדיקת מתגי הצורה המיטוכונדריאלית
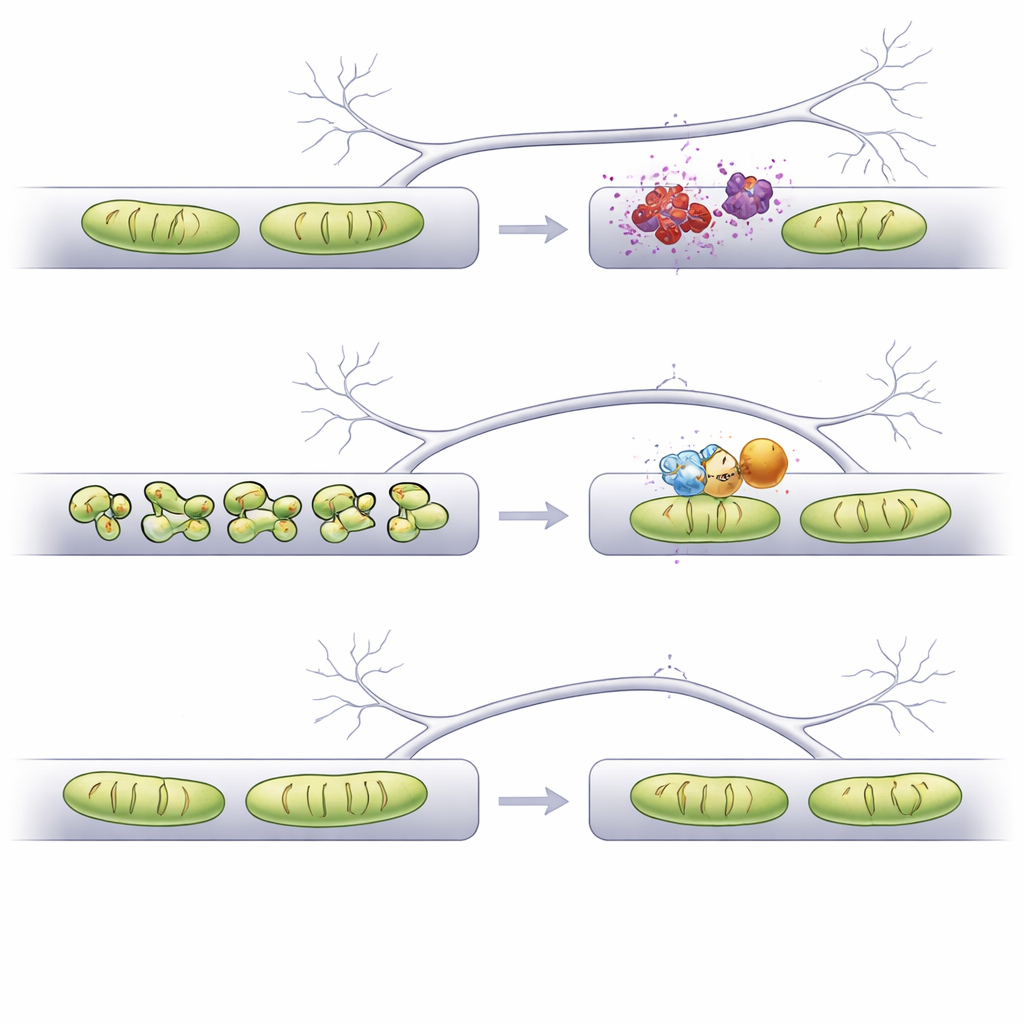
הקבוצה שאלה האם דחיפה של חלבוני מיזוג ופיצול ספציפיים תוכל למנוע את הנזק. הגברה של שני חלבוני מיזוג (Mfn1 ו‑Mfn2) או השתקה של חלבון פיצול (Mff) אכן הגנו על מיטוכונדריות דנדריטיות מפני התקצרות שנגרמה על‑ידי אלפא‑סינוקלין ושמרו גם על קוצי הדנדריטים שלא יאבדו. עם זאת, מניפולציות אלה גרמו לכך שמיטוכונדריות האקסון נעשו ארוכות מדי, מה שהעבודה הקודמת קישרה לבעיות בשחרור סימנים והסתעפות אקסונים. לעומת זאת, הפחתה של חלבון פיצול אחר, Fis1, השיבה את אורך המיטוכונדריות הן בדנדריטים והן באקסונים לערכים קרובים לנורמליים מבלי לגרום להארכה מופרזת. חשוב לציין שבמערך זה צמצום Fis1 לא גרם למוות של הנוירונים, וכמו ההתערבויות האחרות — שמר על צפיפות קוצי הדנדריטים שאחרת הייתה מצטמצמת תחת לחץ אלפא‑סינוקלין.
שמירה על איזון הסידן
מכיוון שמיטוכונדריות באקסונים מסייעות באיזון סידן במהלך פעילות חשמלית, החוקרים בדקו האם שינוי צורתן ישנה את האיזון העדין הזה. הם השתמשו בחיישן פלואורסצנטי לסידן המכוון למיטוכונדריות בבוטונים פרה‑סינפטיים וגירו את האקסונים בפרצי פוטנציאלי פעולה קצרצרים. במצב האלפא‑סינוקלין, הטיפול בסידן במיטוכונדריות האקסונליות הקצרות במקצת נראה דומה לנורמלי. אבל כאשר מיטוכונדריות האקסון הוגדלו יתר על המידה על־ידי הבעת יתר של Mfn1 או השתקת Mff, הן ספגו יותר סידן מהרגיל לאחר גירוי. אחיזה מוגברת זו עלולה להפריע לתפקוד הפרה‑סינפטי. לעומת זאת, השתקת Fis1, שהנורמלה אבל לא הגזימה באורך המיטוכונדריות, שמרה על תגובות הסידן המיטוכונדריאליות שהתיישבו במידה רבה עם הבקרה הבריאה, ומרמזת על פחות פשרות נסתרות.
מה משמעות הדבר לטיפולים עתידיים
לסיכום, המחקר מדגים שלהפוך מיטוכונדריות פשוט לארוכות אינו מספיק — חשוב להשיב את צורתן לגודל המתאים בכל יחידה תאי. באמצעות זרימת עבודה דימותית בסיוע בינה מלאכותית, מזהים המחברים את Fis1 כיעד אטרקטיבי במיוחד: הקטנת ביטויו משמרת את היציבות המבנית של המיטוכונדריות בדנדריטים ובאקסונים, מונעת אובדן קוצי דנדריטים וממנעת טיפול־סידן חריג בטרמינלים פרה‑סינפטיים. ממצאים אלה תומכים ברעיון כי כיוונון מדוד של צורת המיטוכונדריה, אולי בעזרת תרופות או מולקולות אנטיסנס המכוונות ל‑Fis1, עשוי לעזור להגן על סינפסות פגיעות באלפא‑סינוקלינופתיה הקשורה לפרקינסון ואולי גם במחלות מוח נוספות שבהן מיטוכונדריות מסלידות.
ציטוט: Kim, S.Y., Choi, J., Jang, D.C. et al. Systematic evaluation of mitochondrial morphology regulators for amelioration of neuronal α-synucleinopathy. npj Parkinsons Dis. 12, 58 (2026). https://doi.org/10.1038/s41531-026-01277-z
מילות מפתח: מחלת פרקינסון, מיטוכונדריה, אלפא‑סינוקלין, תפקוד סינפטי, נוירודגנרציה