Clear Sky Science · he
עיכוב של הסינתזה החדשה של צרמידים מקל על פתולוגיית אלפא-סינוקאין במודל עכבר של מחלת פרקינסון
למה שומנים במוח חשובים לפרקינסון
מחלת פרקינסון מוכרת בעיקר בזכות רעד בידיים והתנועה המואטת, אבל עמוק במוח מתרחש דרמה שקטה יותר. תאי עצב האחראים על תנועה מתים בהדרגה כאשר חלבון בשם אלפא‑סינוקאין מצטבר לגושים דביקים. המאמר הזה מראה שמשפחה מיוחדת של שומנים, שנקראת צרמידים, מסייעת לקדם את הנזק הזה — ושחסימת ייצורם יכולה להגן על תאים מוחיים בעכברים ובדגמי תאים אנושיים. העבודה מצביעה על מסלול לא צפוי, שניתן אולי ליעד בתרופות, שעשוי בעתיד להאט או למנוע פרקינסון ולא רק להקל על הסימפטומים.
רמזים ממוחות לאחר המוות
כדי להבין האם צרמידים מעורבים בפרקינסון ומצבים קשורים, החוקרים בדקו תחילה רקמות מוח לאחר המוות מאנשים שסבלו מדמנציה מסוג לואי בודי, מחלה שמשתפת את אותם גושי חלבון רעילים שנמצאים בפרקינסון. באמצעות מדידות כימיות רגישות הם מצאו שמספר סוגי צרמידים היו גבוהים יותר במידה משמעותית באזור המידבריין לעומת מוח בריא, במיוחד צורות עם זנבות שומניים ארוכים. לאחר מכן ניתחו מחדש מאגרי נתונים גנטיים גדולים מתאים מוח אנושיים וגילו שהגנים שבונים ומעבדים צרמידים היו פעילים יותר בתאי דופמין של חולי פרקינסון, וגם בתאי תמיכה מסוימים כמו אסטרוציטים ואוליגודנדרוציטים. ביחד, ממצאים אלה מציעים כי איזון הצרמידים מופר במספר סוגי תאים במוח החולה.
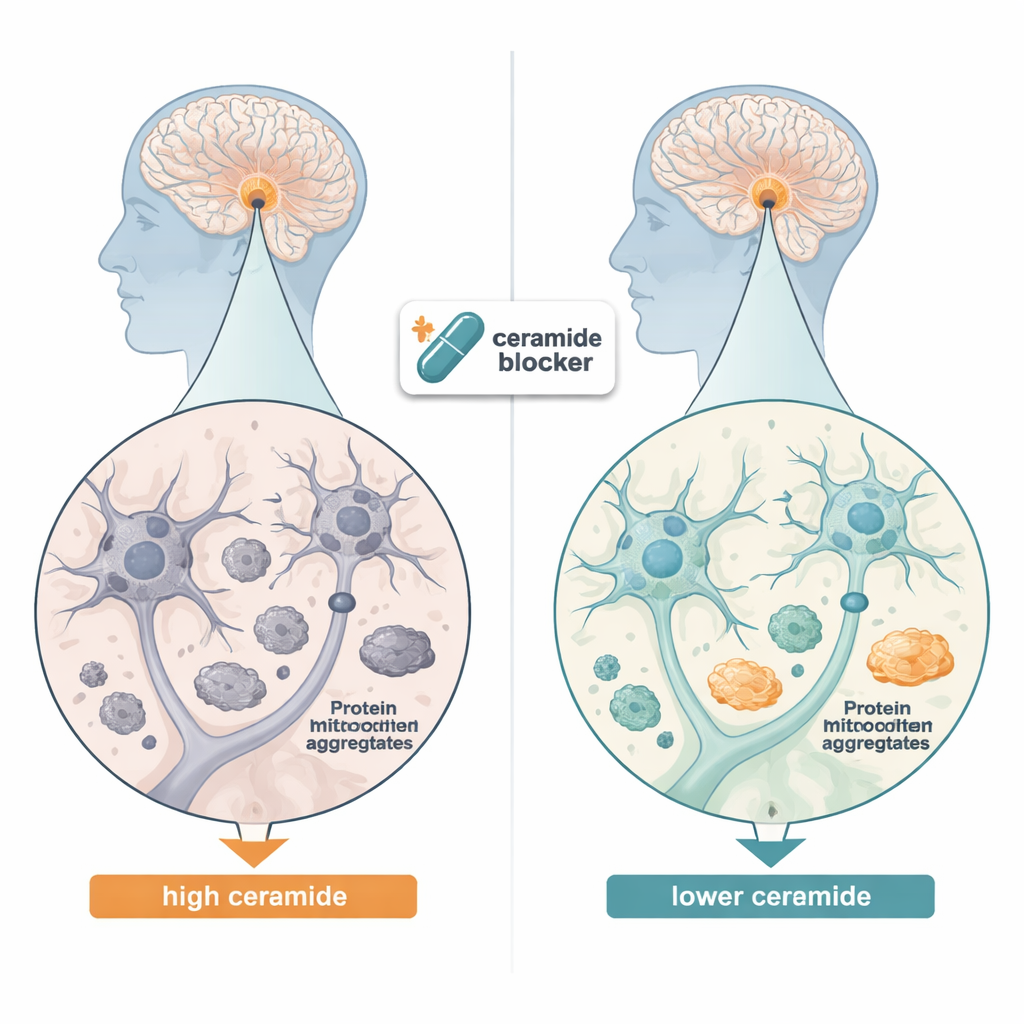
ניקוי גושי חלבון בתאים
הקבוצה המשיכה ובחנה האם הורדת רמות צרמידים יכולה להפחית הצטברות חלבון בתאים דמויי-עצב שגודלו במעבדה. הם השתמשו בתאי נוירובלסטומה אנושיים שהונדסו לייצר בכמות גבוהה צורת אלפא‑סינוקאין מוטנטית שנוטה להצטבר. כאשר עצרו את השלב הראשון בייצור הצרמידים — או על ידי השתקת הגן של אנזים מפתח או על ידי הוספת תרופה בשם מיריוצין — כמות האגרגטים של אלפא‑סינוקאין הבלתי מסיסה ירדה באופן חדה. במקביל, סמנים של מיטופאגיה, מערכת ייחודית של התא למציאת ומחזור מיטוכונדריה פגומה, עלו, והמכונות שמסמנות חלבונים לא רצויים לפירוק הפכו לפעילות יותר. השינויים הללו מרמזים שצרמיד עודף בדרך כלל חוסם את צוותי הניקיון התאים, וכי הסרת העומס השומני הזה מאפשרת לתא לפנות מיטוכונדריות פגומות וגושי חלבון ביעילות רבה יותר.
הגנה על תפקוד המוח בעכברים
המבחן הקריטי ביותר היה האם אסטרטגיה זו עוזרת במוח חי. החוקרים טיפלו במודל עכבר מבוסס שמייצר בכמות גבוהה אלפא‑סינוקאין מוטנטי אנושי ומתפתח בהדרגה לבעיות תנועה וזיכרון. החל באמצע החיים, חלק מהעכברים קיבלו זריקות מיריוצין למשך כמה חודשים, בעוד אחרים קיבלו תמיסת בקרה חסרת השפעה. מיריוצין הורידה בבירור את רמות הצרמידים בדם ובאזור המידבריין של החיות. מבחני התנהגות הראו שהעכברים המטופלים הלכו מרחק רב יותר וביצעו טוב יותר במבוך פשוט התלוי בזיכרון עבודה מרחבי. חתכי מוח מהחיות הללו חשפו שיותר תאי דופמין שרדו באזורים מרכזיים, וכי כמות האלפא‑סינוקאין המזורחן והנוטה להצטבר פחתה. פרופיל הבעה גנטית רחב של המידבריין הראה שמיריוצין דיכא מסלולים דלקתיים תוך שחזר גנים הקשורים לתקשורת סינפטית ולתחזוקה מיטוכונדריאלית בריאה.
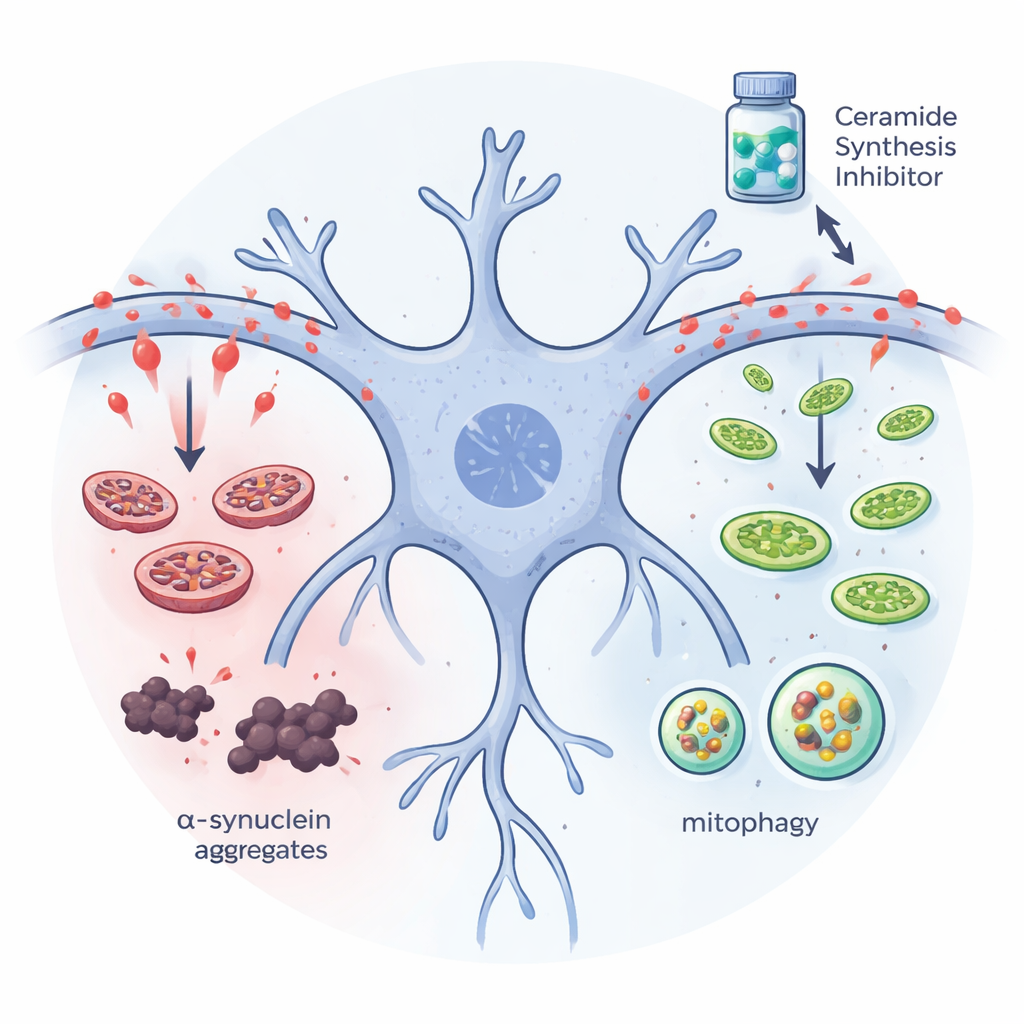
תאומים אנושיים ומיני־מוחות תומכים בממצא
כדי לקרב את התוצאות לחולים, הקבוצה השתמשה בניורונים ו"אורגנואידים" תלת‑ממדיים של המידבריין שגודלו מתאי גזע פלוריפוטנטיים מושרים שמקורם באנשים עם פרקינסון. בניורונים ממטופלים שנשאו חיישן זוהר למיטופאגיה, הטיפול במיריוצין הגביר את האות שמסמן העברת מיטוכונדריות פגומות למרכזי מיחזור של התא ושיפר את ארכיטקטורת רשת המיטוכונדריה. באורגנואידים של המידבריין, מיריוצין שמר על תאי יוצרי דופמין והפחית אגרגטים מזיקים של אלפא‑סינוקאין. כאשר החוקרים הוסיפו צרמידים נוספים לאותם מיני‑מוחות, קרה ההיפך: נוצרו יותר גושי חלבון ותאי דופמין אבדו, במיוחד באורגנואידים ממקורות חולי פרקינסון. ניסויים אלה תומכים בתפקיד מזיק ישיר של הצטברות צרמידים ברקמות הרלוונטיות לאדם.
מה זה עשוי לסמן לגבי טיפולים עתידיים
לבני אדם שאינם מומחים, המסר המרכזי פשוט: בדגמי פרקינסון מרובים, כמות מופרזת של סוג מסוים של שומן מוחי נראית כמרעילה לתאים על ידי קידום גושי חלבון, מיטוכונדריות פגומות ודלקת כרונית. חסימת המסלול הראשי שמייצר שומנים אלה, באמצעות התרופה הניסיונית מיריוצין, הקלה על הבעיות הללו, שמרה על נוירונים פגיעים ושיפרה התנהגות בעכברים, ובו בזמן הצילה נוירונים אנושיים בתרבית. המחברים מדגישים כי בטיחות מינון ומשך טיפול בבני אדם אינם ידועים, ומחלת פרקינסון נובעת מסיבות רבות מעבר לצרמידים. עם זאת, העבודה פותחת קו תקיפה חדש: במקום רק לחזק את איתות הדופמין שהולך ופוחת, טיפולים עתידיים עשויים גם לאזן את מטבוליזם השומנים ואת מנגנוני הניקיון התאים, ולתת לתאי המוח סיכוי טוב יותר להתנגד למעבר האיטי של הנוֹרוֹדֶגֶנֶרָצְיָה.
ציטוט: Lee, E., Park, My., Park, M. et al. Inhibition of de novo ceramide synthesis mitigates alpha-synuclein pathology in a Parkinson’s disease mouse model. npj Parkinsons Dis. 12, 49 (2026). https://doi.org/10.1038/s41531-026-01263-5
מילות מפתח: מחלת פרקינסון, צרמיד, אלפא-סינוקאין, מיטופאגיה, נוֹרוֹדֵגֶנֶרַצְיָה