Clear Sky Science · he
חוסר UQCRC1 פוגם במיטופאגיה דרך מנגנונים התלויים ב-PINK1 במחלת פרקינסון
מדוע המחקר הזה חשוב לציבור הרחב
מחלת פרקינסון ידועה בעיקר בבעיות התנועה—רעד, נוקשות ואיטיות—אבל מתחת לסימפטומים האלה מתנהלת מאבק בתוך תאי המוח לייצור ולניקיון האנרגיה. המחקר בוחן כיצד חלבון פחות מוכר, UQCRC1, מסייע לתאי המוח לשמור על "תחנות הכוח" שלהם בריאות, וכיצד כשל שלו עשוי לפתוח את הדרך לפרקינסון. הבנת המכונה החבויה הזו עשויה להצביע על טיפולים שמאטו או אפילו ימנעו את המחלה, ולא רק על הקלה בסימפטומים.
בעיה בכוח בתוך תאי המוח
תאי המוח שלנו תלויים במיטוכונדריה, מבנים זעירים שמתוארים לעתים קרובות כתחנות כוח תאיות, כדי לייצר את האנרגיה שהם צריכים. UQCRC1 הוא חלק חיוני במנוע מיטוכונדריאלי אחד שמבצע את העבודה הזו. עבודות קודמות הראו שמוטציות תורשתיות נדירות ב-UQCRC1 יכולות לגרום למחלה הדומה לפרקינסון על ידי עומס על המנועים האלה. במחקר זה שאלו החוקרים שאלה רחבה יותר: האם רמות מופחתות של UQCRC1 מעורבות גם בצורות הנפוצות בהרבה, הלא-תורשתיות ("אידיופטיות") של מחלת פרקינסון?
ממצאים משותפים בנתוני מוח של חולים
כדי לענות על כך, החוקרים קיבצו 19 מאגרי נתונים ציבוריים של רקמות מוח מאנשים שנפטרו עם ובלי מחלת פרקינסון. הם התרכזו ב-substantia nigra, האזור העמוק במוח שבו תאים מייצרי הדופמין מתנוונים בפרקינסון. בקרב 150 מקרים מבוקרים ו-185 מקרים של פרקינסון או מחלות קשורות, הם מצאו בהתמדה רמות נמוכות יותר של פעילות גן UQCRC1 במוחות של חולי פרקינסון—כחצי ירידה של כ-20% בממוצע, ללא סימנים חזקים לכך שהתוצאה נבעה במקרה או בהטיית פרסום. הם איששו זאת על ידי מדידת חלבון UQCRC1 בדגימות מוח משני מקורות עצמאיים ובתאים דמויי עצב אנושיים הנושאים מוטציה קשורה למחלה ב-UQCRC1; בכל מקרה, רמות UQCRC1 היו נמוכות באופן ברור במצב הפרקינסון. 
כשצוותי הניקיון נכשלים
מיטוכונדריה לא רק מייצרות אנרגיה; הן גם דורשות בדיקה סדירה והסרה כשהן פגומות. תאים משתמשים בתהליך בקרת איכות שנקרא מיטופאגיה כדי לתייג מיטוכונדריות שחוקות ולשלוח אותן למחלקת מיחזור. הצוות השתמש בדיווחי פלואורסנציה בתאים אנושיים ובזבוב הפירות כדי לצפות בתהליך בפעולה. תחת לחץ שבאופן רגיל מפעיל מיטופאגיה, תאים עם מוטציות ב-UQCRC1 או רמות UQCRC1 מופחתות ייצרו הרבה פחות "מיטוליזוזומים", המבנים שמציינים טיפול מוצלח במיטוכונדריות פגומות. בניורונים המייצרי דופמין בזבוב הפירות, הפחתת UQCRC1 הובילה באופן דומה לפחות מיטוכונדריות ממוחזרות, מה שמשקף ליקויים שנראו כאשר גן ליבה באוטופאגיה נחסם. ממצאים אלה מראים שאובדן UQCRC1 אינו רק מחליש ייצור אנרגיה—הוא גם מחריף את הניקיון של תחנות הכוח התקולות.
מתג חסר ומטרה מבטיחה
לאחר מכן פנו החוקרים ל-PINK1, חלבון המשמש כחיישן ומתג במערכת המיטופאגיה. כאשר מיטוכונדריה בלחץ, PINK1 מצטבר על המשטח שלהן, משכן חלבון נוסף בשם Parkin ומניע את תהליך התיוג שמוביל למחזור. מטה-אנליזה של נתוני מוח של חולים גילתה שגם PINK1, אך לא Parkin, היה מופחת במוח הביניים של חולי פרקינסון, בכ-22% בקירוב. הן בתאים אנושיים והן בזבובים עם בעיות UQCRC1, רמות PINK1 ירדו, ושלבי ההפעלה הראשוניים של מסלול PINK1–Parkin—העברת Parkin למיטוכונדריה ותיוגן—הושפעו. באופן מובהק, הגברת PINK1 בזבובים החזירה את יכולתם לטפס ונירמלדה מיטופאגיה, מה שמרמז שכיבוי המתג חזרה למעלה יכול לפצות על אובדן UQCRC1. 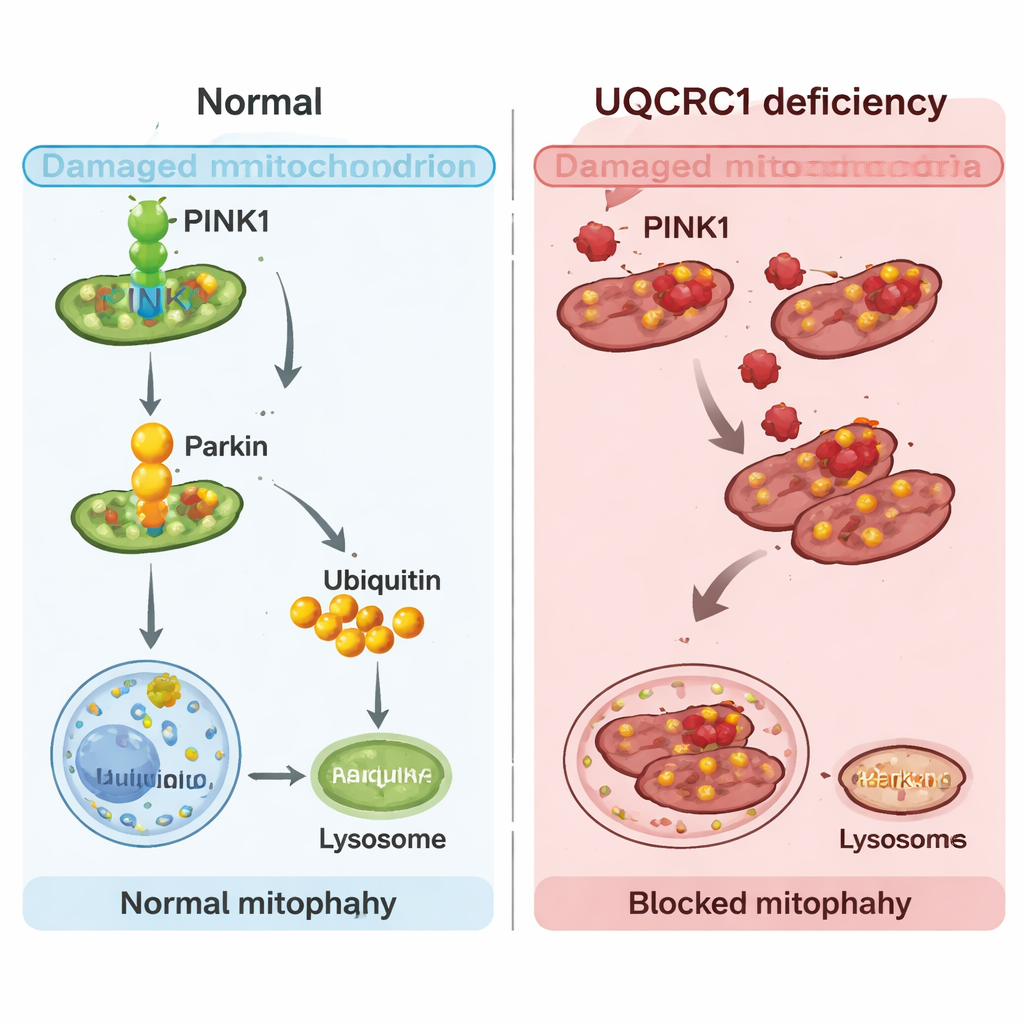
בדיקת פעילי תרופה של מסלול הניקיון
מכיוון שהוספת PINK1 ישירות אינה מעשית בחולים, הקבוצה בדקה מולקולות קטנות הידועות כמגבירות את פעילות PINK1: קינטין ו-MTK458. בזבובי פירות עם חוסר ב-UQCRC1, האכלה בתרכובות האלה שיפרה תנועה והגנה על נוירוני הדופמין הפגיעים. בתאים דמויי עצב אנושיים עם UQCRC1 מופחת, MTK458 האריכה השלוחות העצביות המוקטנות והחיה מיטופאגיה פגומה. יתרונות אלה היו תלויים ב-PINK1, ותומכים ברעיון שהפעלת מסלול זה באופן ממוקד יכולה לעזור לתאים להתמודד עם לחץ מיטוכונדריאלי הנגרם מרמות נמוכות של UQCRC1.
מה משמעות הדבר עבור טיפולים עתידיים בפרקינסון
בסך הכל, המחקר מקשר ירידה ב-UQCRC1 לריאקציה שרשרתית: מיטוכונדריות בלחץ, ניקיון מונע על ידי PINK1 חלש יותר, ולבסוף אובדן תאי דופמין. עבור קורא שאינו מומחה, המשמעות היא שחלק מהמקרים של פרקינסון עשויים לנבוע מתחנות כוח שלא רק עובדות גרוע אלא גם מצטברות כפסולת שהתא אינו יכול לפנות. בעוד שנדרש עוד מחקר כדי למפות כל שלב ולבדוק בטיחות באנשים, התוצאות מדגישות את פעילי PINK1 כמועמדים לתרופות מדויקות לחולים שסימן מחלתם הוא ליקוי מיטוכונדריאלי כמו חוסר UQCRC1. במקום רק להסוות את הסימפטומים, טיפולים כאלה שואפים לשקם את היכולת הטבעית של התא לתחזק ולחדש את תחנות האנרגיה שלו.
ציטוט: Li, JL., Huang, SY., Huang, PY. et al. UQCRC1 deficiency impairs mitophagy via PINK1-dependent mechanisms in Parkinson’s disease. npj Parkinsons Dis. 12, 48 (2026). https://doi.org/10.1038/s41531-026-01262-6
מילות מפתח: מחלת פרקינסון, מיטוכונדריה, מיטופאגיה, PINK1, UQCRC1