Clear Sky Science · he
שינויים ב-MTNAP1 עומדים בבסיס הפרעה נוירודגנרטיבית על ידי פגיעה ביציבות המיטוכונדריה
מדוע הסיפור הזה חשוב לבריאות המוח
משפחות רבות חוות את יאוש הצפייה בילד שמאבד בהדרגה כישורים התפתחותיים ללא אבחנה ברורה. המחקר הזה חושף גורם גנטי חדש למצבים כאלה, ועוקב אחריו מהגֵן התקול הבודד דרך נזק ל"תחנות הכוח" בתוך תאי המוח ועד להתכווצות רקמת המוח. הבנת שרשרת האירועים הזו לא רק מביאה תשובות למשפחות המושפעות, אלא גם מחדדת את התמונה הרחבה יותר של כמה שבריריים באמת מערכות האנרגיה במוח.
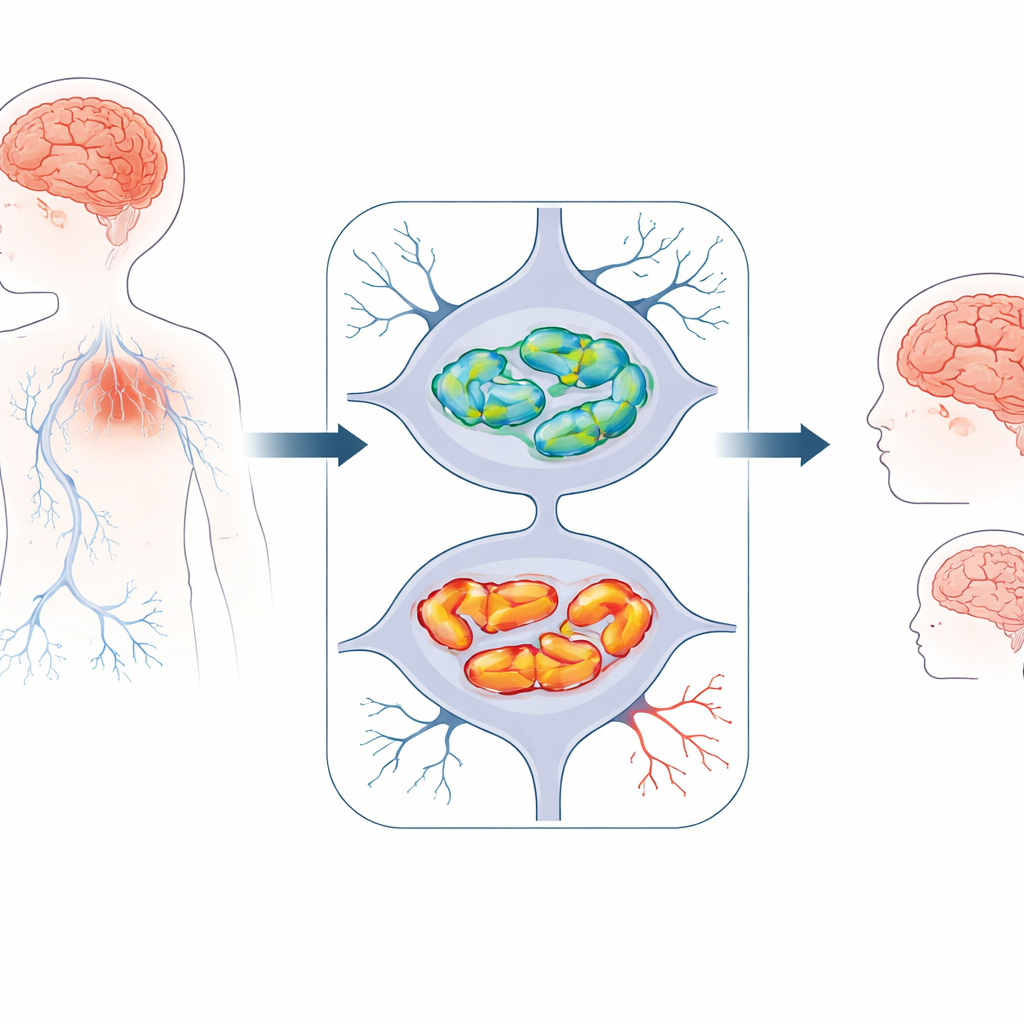
הפרעה מוחית ילדותית שזוהתה לאחרונה
החוקרים חקרו שלוש ילדות משתי משפחות שאינן קשורות, שהציגו בעיות התפתחות מוקדמות. כולן היו קטנות לגילן, שימשו מאוחר יותר לשבת, ללכת ולדבר מאשר המצופה, ואז בהדרגה איבדו חלק מהיכולות הללו. כולן פיתחו קשיי תנועה כגון הליכה לא יציבה, נוקשות שרירים או טונוס שרירים נמוך, והתפרצויות אפילפטיות. סריקות מוח הראו תמונה עקבית: רקמת המוח הגדול וה"מוח הקטן" בגב הייתה מדללת לאורך זמן, וגשר סיבים מרכזי — קורפוס קולוזום — היה דק מן הרגיל. מאפיינים אלה הצביעו על ירידה התקדמותית בתאי העצב ולא על פגיעה חד־פעמית בלידה.
גן זעיר עם השלכות גדולות
על־מנת לחפש סיבה תורשתית, הצוות רצף את כל הגנים המקודדים לחלבון אצל הילדים הנפגעים והוריהם. הם זיהו גן בשם MTNAP1, שעוזר לארגן את ה-DNA בתוך המיטוכונדריה, תחנות האנרגיה של התא. אצל כל ילד נמצאו שתי עותקות פגומות של MTNAP1, אחת מכל הורה נשא תקין. בשני האחים החלפה של "אות" גנטית אחת החליפה מרכיב חומצי אמיני אחד בשני, ועיוותה במידה עדינה את צורת החלבון. בילד השלישי אות עצירה מוקדמת בגן ככל הנראה מנעה יצירת החלבון לחלוטין. השינויים הללו לא הופיעו בבסמכי אוכלוסייה נרחבים, מה שמחזק את הטיעון שהן וריאנטים נדירים ומזיקים ולא תכונות תורשתיות פסיביות בלבד.
תחנות הכוח תחת לחץ
בהמשך בחנו המדענים תאי עור שנלקחו מהילדים והשוו אותם לתאים של אנשים בריאים. במיקרוסקופ, תאים תקינים הציגו מיטוכונדריות ארוכות ודמויי־חוט היוצרות רשת מקושרת, בעוד בתאי הילדים נראו מיטוכונדריות קצרות, שבורות ומקובצות. כשהחוקרים הפחיתו באופן ניסיוני את רמות MTNAP1 בקו תאים דמוי־עצבי אנושי, נצפה אותו התפרקות של רשת המיטוכונדריה, ואושר שאובדן חלבון זה כשלעצמו יכול להפריע למבנה שלהן. מדידות פעילות מיטוכונדריאלית הראו כי שלבים מרכזיים בייצור אנרגיה החלשים, והתאים הפיקו כמות עודפת של מולקולות חמצון תגובתיות — תוצרי חמצון מזיקים הפועלים כמו חלודה מולקולרית. התאים המופעלים נפסקו ממחזור חלוקה תקין, הצטברו בשלב מנוחה והפעילו סימנים של הזדקנות מוקדמת.
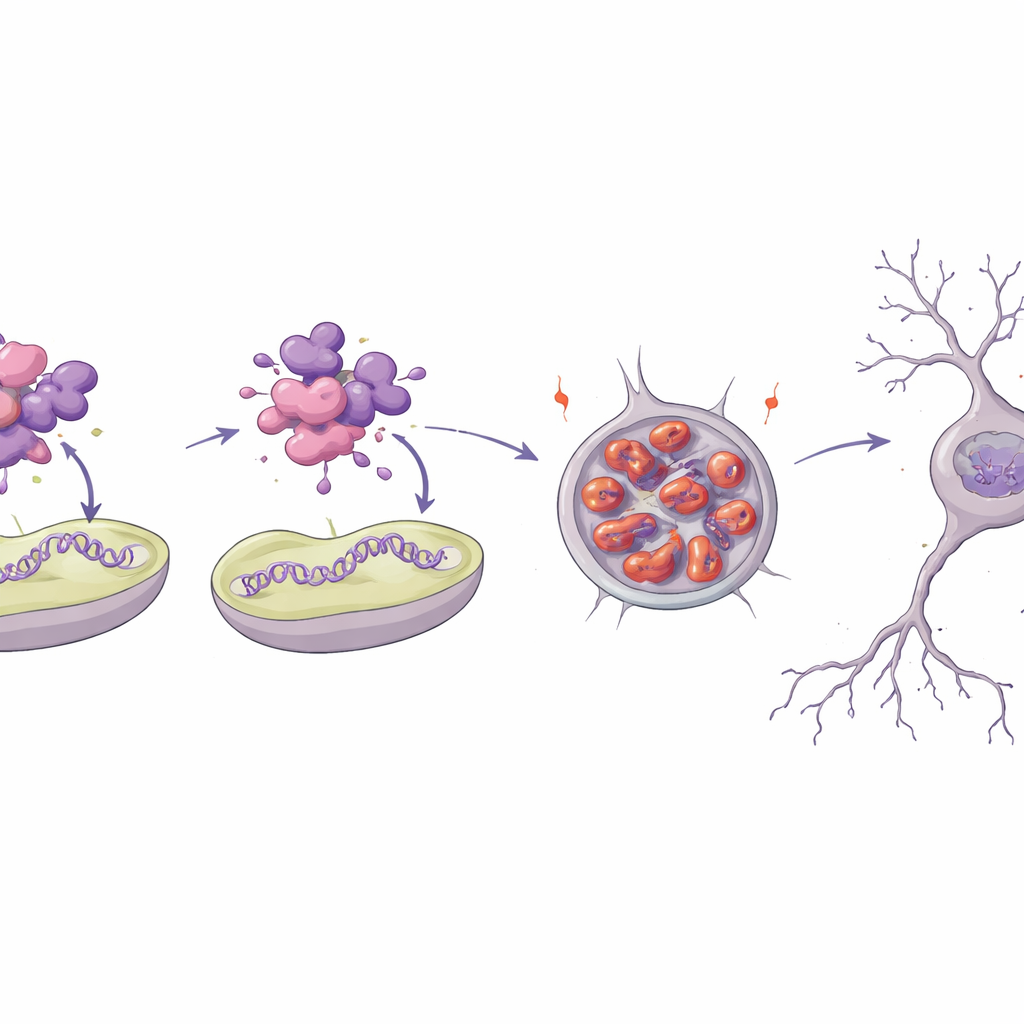
כיצד שינוי יחיד מפרק חלבון חיוני
כדי להבין מדוע אחד הווריאנטים כה משבש, הצוות דגם את המבנה התלת־ממדי של חלבון MTNAP1 ושיחזר אותו במעבדה. החומצה האמינית המוחלפת יושבת באזור ספירלי דחוס שלרוב מסייע לחלבון באינטראקציה עם ה-DNA המיטוכונדריאלי והממברנה הפנימית. סימולציות מחשב ובדיקות ביופיזיקליות הראו שהחלבון המוטנטי פחות יציב, מאבד רבות מצורתו המסודרת, ומאסף בקלות לגושים. בניסויים בצינור הבדיקה החלבון התקין התחבר בחוזקה לחתיכות קצרות של DNA מיטוכונדריאלי ולמשטחים ממברנליים מלאכותיים, בעוד המוטנט כמעט ולא התקשר ובמקום זאת הרכיב אגגרגטים בדומים לאמילואיד. כשהוכנס לתאים דמויי עצב, המוטנט הצטבר לאורך זמן בגושים גדולים סביב הגרעין — סימן שמערכות בקרת איכות החלבון מוצפות.
ממיטוכונדריה פגועה למוח כושל
בהרכבת התמונה, המחקר מציג מודל של שלבים: MTNAP1 פגום מחליש את השלד המסייע לארגן את ה-DNA המיטוכונדריאלי ולעגן אותו לממברנה הפנימית; זה מייצב את המיטוכונדריה בצורה לקויה, גורם להן להתפרק ולאבד את יכולתן לייצר אנרגיה ביעילות; עליית הלחץ החמצוני ואותות ה"הזדקנות" התאית הופכים תאי עצב לפגיעים במיוחד, שכן דרישות האנרגיה שלהם גבוהות וקבועות והיכולת לחידוש נמוכה. במוח המתפתח, משבר אנרגיה איטי ומתמשך זה מתורגם לעיכוב בהתפתחות, אובדן כישורים נרכשים והתכווצות הדרגתית של אזורי מוח חשובים. בעוד שיש צורך בחולים נוספים ובמחקר חיות כדי למפות את התסמונת במלואה, עבודה זו מציבה באופן מוצק את MTNAP1 כשומר מרכזי של יציבות המיטוכונדריה ומדגישה את ארגון ה-DNA המיטוכונדריאלי כעמוד תווך בהתפתחות מוח בריאה.
ציטוט: Kumar, A., Saha, S., Nasir, N. et al. Variants in MTNAP1 underlie a neurodegenerative disorder by impairing mitochondrial stability. npj Genom. Med. 11, 19 (2026). https://doi.org/10.1038/s41525-026-00554-3
מילות מפתח: מיטוכונדריה, נוירודגנרציה, גנטיקה של ילדים, DNA מיטוכונדריאלי, קיפול חלבון שגוי