Clear Sky Science · he
ניתוח טרנסקריפטומי לחשיפת המנגנון של רגישות רדיו מוגברת בסרטן השד משולש שלילי החיובי לקולטן אנדרוגן באמצעות עיכוב הקולטן
מדוע מחקר זה חשוב עבור אנשים המתמודדים עם סרטן השד
טיפול בקרינה הוא מרכיב מרכזי בטיפול ברבים מהמקרים של סרטן שד אגרסיבי, אך ישנם גידולים שקשה יותר להשביתם באמצעות קרינה מאשר אחרים. המחקר שואל שאלה מעשית עם השלכות קליניות ממשיות: האם קבוצה של תרופות החוסמות אותות הורמונליים זכריים, שכבר בשימוש בסרטן הערמונית, יכולה להפוך תת־סוג של סרטן השד המשולש השלילי לפגיע יותר לקרינה — ולמה זה עובד במקרים מסוימים אך לא באחרים?
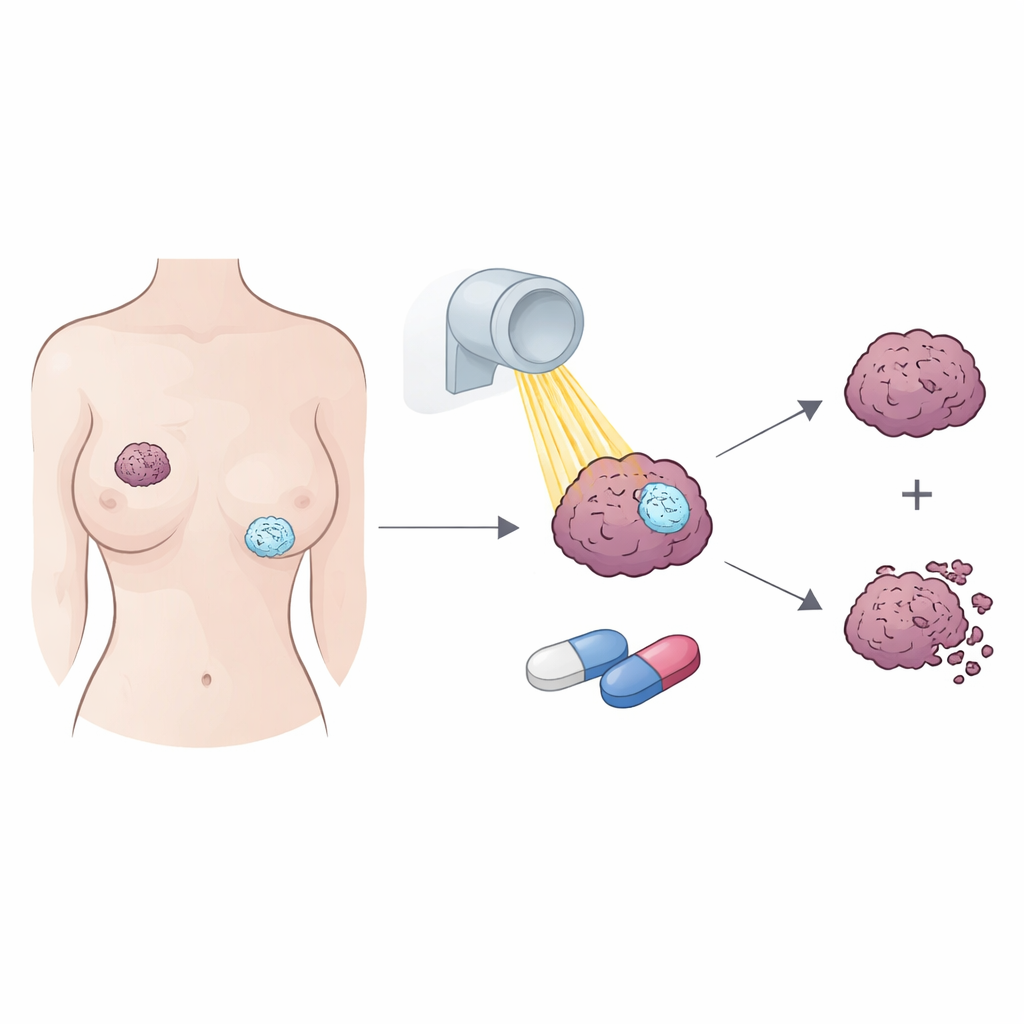
צורה קשה לטיפול של סרטן השד
סרטן השד המשולש השלילי חסר שלושה מטרות מולקולריות שכיחות — קולטן האסטרוגן, קולטן הפרוגסטרון ו‑HER2 — ולכן החולים לעתים קרובות נאלצים להישען בעיקר על ניתוח, כימותרפיה וקרינה. עם זאת, חלק מהגידולים הללו כן מבטאים את קולטן האנדרוגן, חלבון המשתמש באותות הורמונליים דומים לטסטוסטרון ויכול לקדם גדילת גידול. מחקרים קודמים הראו שעיכוב הקולטן יכול להאט את הגידולים הללו ואולי לשפר את השפעות הקרינה, אך לא היה ברור כיצד זה קורה ובאילו תרופות וגידולים התועלת נגלה ביותר.
בדיקת חוסמי הורמונים מודרניים עם קרינה
החוקרים חקרו מספר מודלים מעבדתיים של תאי סרטן שד משולש שלילי שהצטיינו בעיקר ברמות שונות של ביטוי קולטן האנדרוגן. הם התמקדו בשתי תרופות אנטי‑אנדרוגניות חדשות יותר, אפאלוטמיד ודארולוטמיד, ושילבו חשיפות קצרות לתרופות אלו עם מינונים סטנדרטיים של קרינת רנטגן. בתאים עם רמות גבוהות של קולטן האנדרוגן, אפאלוטמיד הגדיל בבירור את נזק הקרינה, והשאיר פחות תאים המסוגלים ליצור מושבות חדשות. דארולוטמיד, לעומת זאת, הראה השפעה מועטה או לא הייתה לו השפעה על הרגישות לקרינה באותם תאים, ולא אף אחת מן התרופות עזרה בתאים שהביעו מעט מאוד את הקולטן. ממצאים אלה מצביעים על כך שלא כל התרופות החוסמות אנדרוגן פועלות באופן זהה בסרטן השד, וכי הגידול חייב להסתמך במידה רבה על הקולטן כדי שהשילוב יעבוד.
מעקב אחרי תזוזת חלבון מפתח בתוך התא
כדי להבין מה קורה בתוך תאי הסרטן לאחר אותות הורמונליים או קרינה, הצוות עקב אחרי מיקום קולטן האנדרוגן עצמו. כאשר התאים נחשפו לאנדרוגן סינתטי, הקולטן עבר לגרעין — מרכז הבקרה שבו גנים נדלקים וכבים. קרינה לבדה לא גרמה לכך שהקולטן יעזוב את הגרעין; למעשה, הוא נשאר שם לאחר הטיפול, מוכן להשפיע על פעילות הגנים. עם זאת, כאשר התאים קיבלו את התרופה האנטי‑אנדרוגנית אנזאלוטמיד לפני הקרינה, רמות הקולטן בגרעין ירדו ועוד ממנו נשאר בנוזל החוץ‑גרעיני של התא. זה מחזק את הרעיון שעיכוב כניסת הקולטן לגרעין מפריע ליכולתו להפעיל תוכנית גנטית מגן לאחר קרינה.
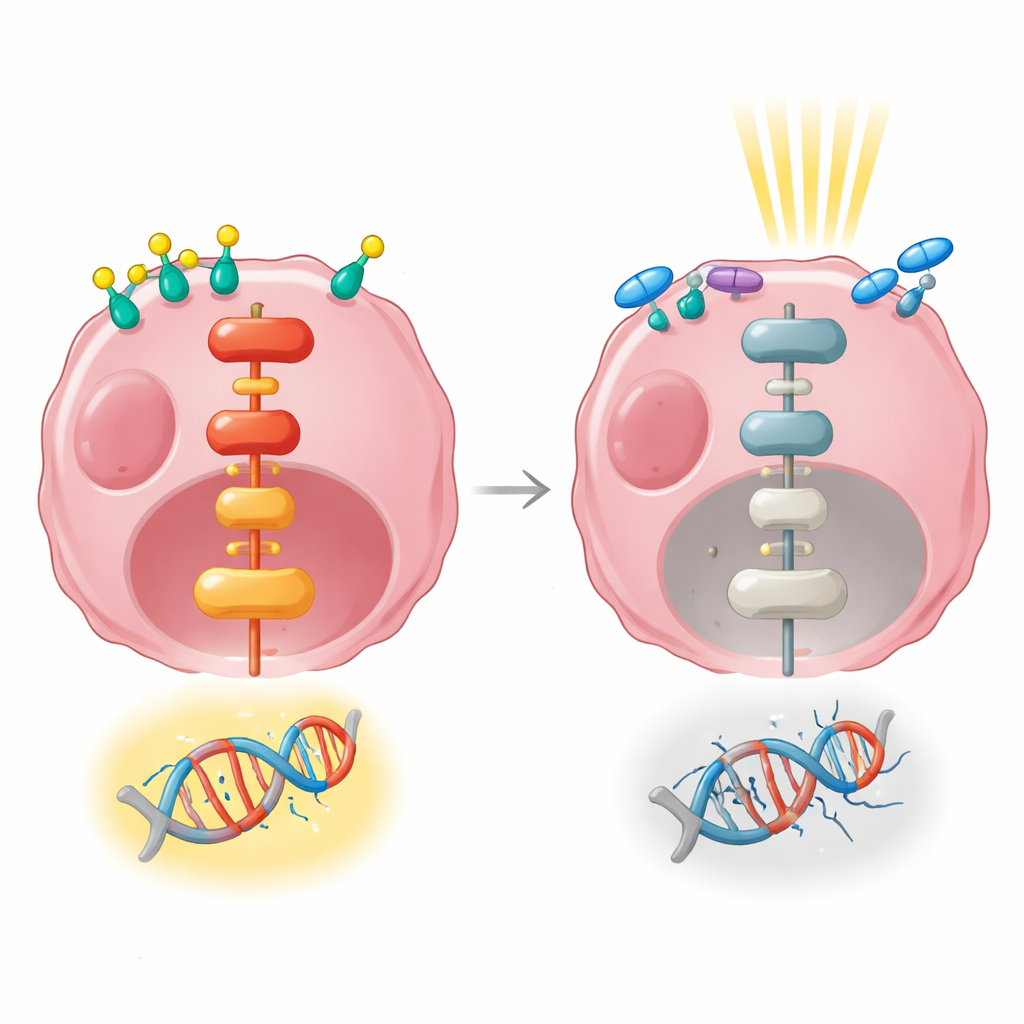
אותות גנטיים המקשרים בין הורמונים לעמידות
החוקרים השתמשו לאחר מכן בריצוף RNA כדי לקבל תמונת מצב רחבה של אילו גנים הוגברו או הושתקו אחרי גירוי הורמונלי, קרינה, או שניהם יחד. טיפול הורמונלי לבדו שינה את הפעילות של מאות גנים והשפיע בעוצמה על מסלולים השולטים בצמיחה תאית, הצמדות ותקשורת עם הסביבה. קרינה שניתנה לבדה, בנקודת זמן מוקדמת, שינתה הרבה פחות גנים. כאשר גירוי הורמונלי וקרינה שולבו, הופעלו רבים מאותם מסלולים הקשורים לצמיחה, כולל נתיב איתות מרכזי הנודע כ‑MAPK/ERK, שמעביר אותות ממטֻח התאים לגרעין. נתיב זה ידוע כתומך ביכולת התאים לשרוד ולתקן נזק בדנ״א.
בחינת מסלול הישרדות שמגן על הדנ"א
מכיוון שאיתות MAPK/ERK חזר והופיע בניתוחיהם, החוקרים בדקו האם חיזוק נתיב זה יכול לבטל את היתרון של חסימת אנדרוגן במהלך קרינה. הם מהנדסים תאים סרטניים להפיק בכמות גבוהה גרסה תמיד־פעילה של ERK, רכיב מפתח של הנתיב, ואז חזרו על הטיפול בקרינה בצירוף אפאלוטמיד. בהקשר זה, אפאלוטמיד כבר לא הגביר את הרגישות לקרינה: האות המוגבר של ERK נראה כמגן על התאים. יחד עם מדידות חלבוניות, תוצאות אלו מצביעות על אותות MAPK/ERK כקשר קריטי בין פעילות קולטן האנדרוגן ויכולת התא לתקן שברים בדנ״א הנגרמים על ידי קרינה.
מה המשמעות של זה לטיפול בסרטן השד בעתיד
במונחים פשוטים, עבודה זו מצביעה על כך שחלק מסרטני השד המשולש השלילי שורדים קרינה על ידי שימוש באותות הקשורים לאנדרוגנים כדי להפעיל מעגל הישרדות פנימי המסייע להם לתקן דנ״א פגוע. תרופות כמו אפאלוטמיד ואנזאלוטמיד יכולות לשבש מעגל זה בגידולים שתלויים בחוזקה בקולטן האנדרוגן, ולהפוך את הקרינה ליעילה יותר, בעוד שגידולים עם רמות נמוכות של הקולטן או דרכים חלופיות להישרדות עשויים שלא להפיק תועלת. על ידי מיפוי מסלולי הגנים המעורבים — ובעיקר נתיב MAPK/ERK — מחקר זה מספק בסיס לשילובים מדויקים יותר של חוסמי הורמונים, מעכבי מסלולים וקרינה שעשויים לשפר תוצאות לחולים עם צורה זו של סרטן השד שקשה לטפל בה.
ציטוט: McBean, B., Hauk, B., Michmerhuizen, A.R. et al. Transcriptomic analysis to uncover the mechanism of radiosensitization of AR-positive triple-negative breast cancers with AR inhibition. npj Breast Cancer 12, 50 (2026). https://doi.org/10.1038/s41523-026-00916-1
מילות מפתח: סרטן השד משולש שלילי, קולטן אנדרוגן, טיפול בקרינה, הגברת רגישות לקרינה, אותות MAPK ERK