Clear Sky Science · he
רשתות JAK/STAT1–אינטרפרון–ISGylation בעמידות סרטן השד בפני מעכבי FOXM1 ו-CDK4/6
מדוע זה חשוב לטיפול בסרטן השד
רבות מהנשים עם סרטן שד חיובי לקולטן אסטרוגן (ER+) מקבלות כיום תרופות ממוקדות המאטות את גדילת הגידול על ידי עצירת מחזור התא. עם זאת, כמעט באופן בלתי נמנע, הגידולים מתאימים את עצמם לטיפולים אלה ומתחילים לגדול שוב. המחקר הזה שואל שאלה דחופה: כאשר סרטן השד ER+ מפתח עמידות לשני סוגי תרופות עיקריים — מעכבי FOXM1 ומעכבי CDK4/6 — אילו שינויים בתוך תאי הסרטן מאפשרים להם להימלט, והאם שינויים אלה יכולים גם לחשוף דרכים חדשות לעצור אותם?
חיווט הישרדות משותף בגידולים עמידים
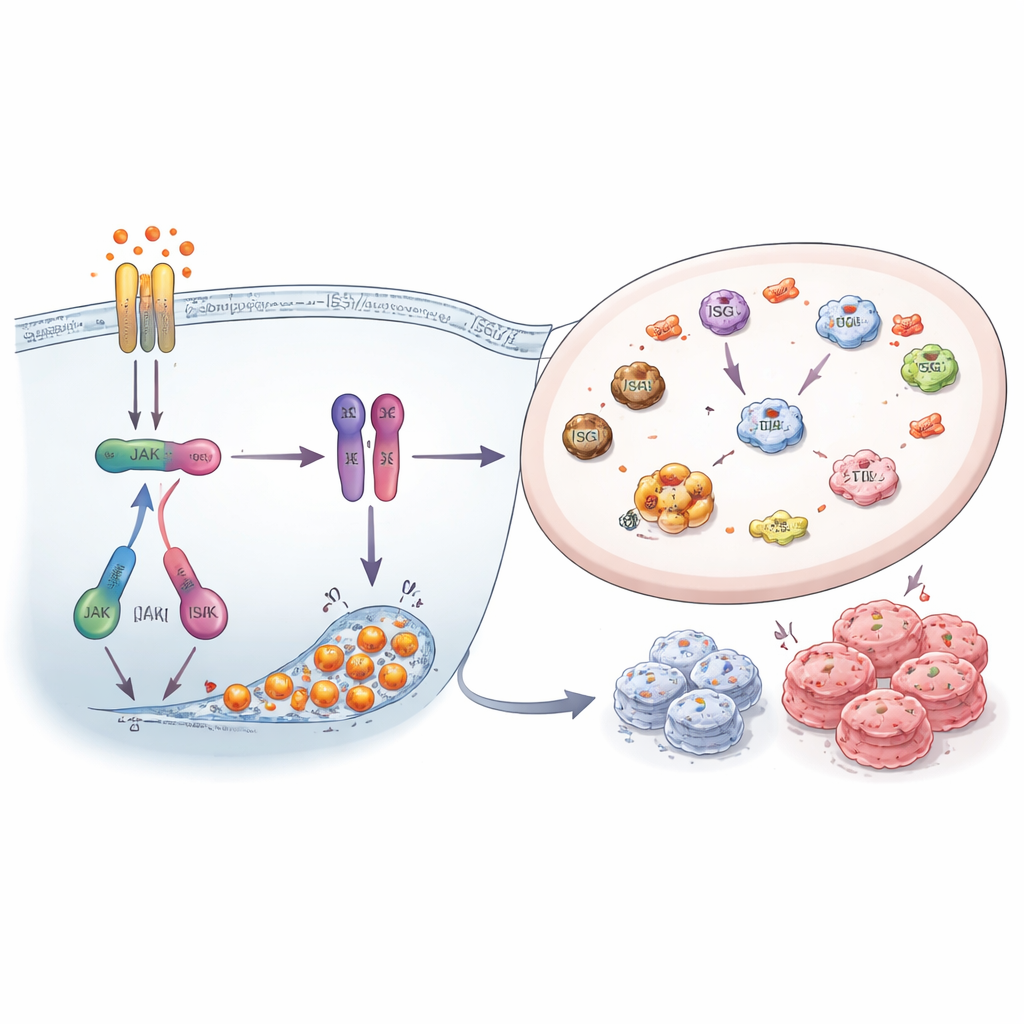
החוקרים התמקדו בתאי סרטן שד ER+ שגודלו במעבדה עד שלא הגיבו עוד או למעכבי FOXM1 או למעכבי CDK4/6 כגון פלבציקליב ואבמאציקליב. הם מצאו שלמרות שפיתחו עמידות לתרופות שונות, תאים אלה הפעילו מערכת אזעקה פנימית דומה הממוקדת סביב אותות אינטרפרון וחלבון בשם STAT1. מערכת זו מובילה לייצור של מספר רב של "גני מתעוררי אינטרפרון" וחלבון קטן בשם ISG15, שניתן לצמידו לחלבונים אחרים כתג מולקולרי. בתאים עמידים נמצאו רמות גבוהות יותר של STAT1, STAT1 מופעל, ISG15 חופשי וחלבונים המסומנים ב‑ISG15 לעומת התאים הלא‑עמידים, מה שמעיד שהרשת הזו מהווה ציר משותף של עמידות לתרופות.
מעיל מגן של תגים מולקולריים
בהסתכלות מקרוב יותר, הקבוצה ראתה שהתאים העמידים לא רק ייצרו יותר ISG15 אלא גם הגבירו אנזימים שמצמידים את ISG15 לחלבונים אחרים, תהליך הידוע כ‑ISGylation. אנזימים אלה — HERC5, HERC6 ו‑UBE2L6 — היו משמעותית מוגברים, במיוחד בתאים עמידים למעכבי FOXM1. חלבונים רבים בתא, כולל STAT1 עצמו, נשאו תגי ISG15 בתאים עמידים, לעיתים ברמות גבוהות יותר מאשר בתאים הרגישים לדרג. משום שהצמדת תגי ISG15 יכולה לשנות את מולחיות החלבונים ואת התנהגותם, הצטברות חלבונים מסומני ISG15 נראית כחלק מהאופן שבו תאי הסרטן מתחזקים כנגד הטיפול.
כיבוי האזעקה מחליש את התאים העמידים
החוקרים לאחר מכן בדקו האם כיבוי רשת האזעקה הזו יהפוך את התאים העמידים לפגיעים יותר. הם השתמשו בתרופות החוסמות קינאזות JAK — מתגים מרכזיים מעלה ל‑STAT1 — וב‑siRNA כדי להפחית ISG15, HERC5 ו‑HERC6. חסימת איתות JAK1/2 הורידה משמעותית את פעילות STAT1, צמצמה את רמות ISG15 ואת ה‑ISGylation, והקטינה את הקולוניות שהכילו תאים עמידים, במיוחד אלה העמידים למעכבי FOXM1. באופן דומה, השתקה ישירה של ISG15 וסתמי החיבור שלו הפחיתה את דפוס ה‑ISGylation והקשתה על הישרדות התאים. ניסויים אלה מראים שמערכת האינטרפרון–STAT1–ISG15 אינה רק צופה מן הצד אלא תומכת באופן פעיל בצמיחה ובהתמדה של תאי סרטן עמידים לתרופות.
תקווה חדשה באסטרטגיות טיפול רצפטיביות
אחת הממצאים המעודדים ביותר היא שהתאים העמידים לא היו תקועים במצב בלתי מנוצח יחיד. תאים של סרטן שד שפתחו עמידות למעכבי CDK4/6 עדיין הגיבו למעכבי FOXM1, ותאים עמידים למעכבי FOXM1 הצליחו עדיין להאט תחת פלבציקליב או אבמאציקליב. בשכבות תא דו‑ממדיות ובתרביות תלת‑ממדיות במטריג'ל שמדמות טוב יותר גידולים, החלפת מחלקת התרופה צמצמה באופן חד את צמיחת התאים והורידה את הביטוי של גנים המניעים שכפול DNA וחלוקת תאים. במקביל, נתוני מטופלות הראו שרמות גבוהות של ISG15 והאנזימים המשויכים אליו בגידולים ER+/HER2− נקשרו להישרדות גרועה יותר, דבר המדגיש את הרלוונטיות הקלינית של חיווט העמידות הזה.
מה זה אומר למטופלות ולטיפולים עתידיים
לקריאה ציבורית, התמונה שעולה היא שתאי סרטן שד ER+ עמידים מחזירים לעצמם חיווט סביב מעגל תגובת־מתח משותף, משתמשים באותות אינטרפרון ובתגי ISG15 כסוג של שריון מגן. החדשות הטובות הן שהשריון הזה חושף נקודות תורפה חדשות. תרופות החוסמות את מסלול JAK–STAT1–ISG15 ותכניות טיפול שמסדרות מעכבי FOXM1 אחרי מעכבי CDK4/6 (או להפך) עשויות לעזור לעקוף את העמידות במקום להיכנע לה. למרות שהממצאים האלה עדיין דורשים אימות בניסויים קליניים, הם מציעים מפת דרכים ברורה יותר להפוך צומת טיפול שנראה לרבים כסיומת-דרך להזדמנות חדשה לשליטה במחלה.
ציטוט: Ziegler, Y., Kumar, S., Saeh, C.M. et al. JAK/STAT1-interferon-ISGylation networks in breast cancer resistance to inhibitors of FOXM1 and CDK4/6. npj Breast Cancer 12, 44 (2026). https://doi.org/10.1038/s41523-026-00911-6
מילות מפתח: סרטן שד חיובי לקולטן אסטרוגן (ER+), עמידות לתרופות, מעכבי CDK4/6, מעכבי FOXM1, אותות אינטרפרון