Clear Sky Science · he
כימותרפיה-אימונולוגית מקומית מתוכנתת לסרטן שד טריפל-שלילי באמצעות שחרור מרחבי-זמני של אוליגודאוקסינוקליאוטידים CpG, גמציטאבין ופאצ׳יטקסל
להפוך סרטן שד קשה למטרה מקומית
סרטן שד טריפל-שלילי הוא אחת הצורות הקשות ביותר של סרטן השד לטיפול, מכיוון שחסר לו את המתגים המולקולריים הרגילים שעליהם נצמדים תרופות מודרניות רבות. המטופלות לעתים קרובות חייבות להסתמך על כימותרפיה חזקה שמשתוללת בכל הגוף, מביאה תופעות לוואי משמעותיות ולעתים קרובות לשליטה ארוכת טווח מאכזבת. המחקר הזה חוקר רעיון שונה מאוד: במקום להציף את הגוף בתרופות, האם אפשר למקם מאגר תרופות מתכנת קטן לצד הגידול, ולשחרר סירופ כימותרפי וממריצי חיסון ברצף מתוזמן בקפידה בדיוק במקום שבו הם נדרשים?
מאגר זעיר עם שאיפות גדולות
החוקרים יצרו פלטפורמה שהם קוראים לה כימותרפיה-אימונולוגית מקומית מתוכנתת, או PLICT. אפשר לדמיין אותה כגרגיר רך שניתן להזריקו שישב לצד גידול בשד ומשחרר טיפול באיטיות לאורך שבועות. הגרגיר משלב ג'ל הידרופילי שמשחרר במהירות מעורר חיסוני ואחת מתרופות הכימותרפיה, גמציטאבין, עם מיקרו-כדורים פלסטיים זעירים שמשחררים לאט תרופה שנייה, פאצ'יטקסל. הממריץ החיסוני, רצף קצר של DNA שנקרא CpG, מתוכנן להעיר תאי חיסון מקומיים, בעוד הכימותרפיות הפונות ישירות תוקפות את תאי הגידול ומשנות את סביבת הגידול כך שתאי חיסון יוכלו להיכנס ולעשות את עבודתם.
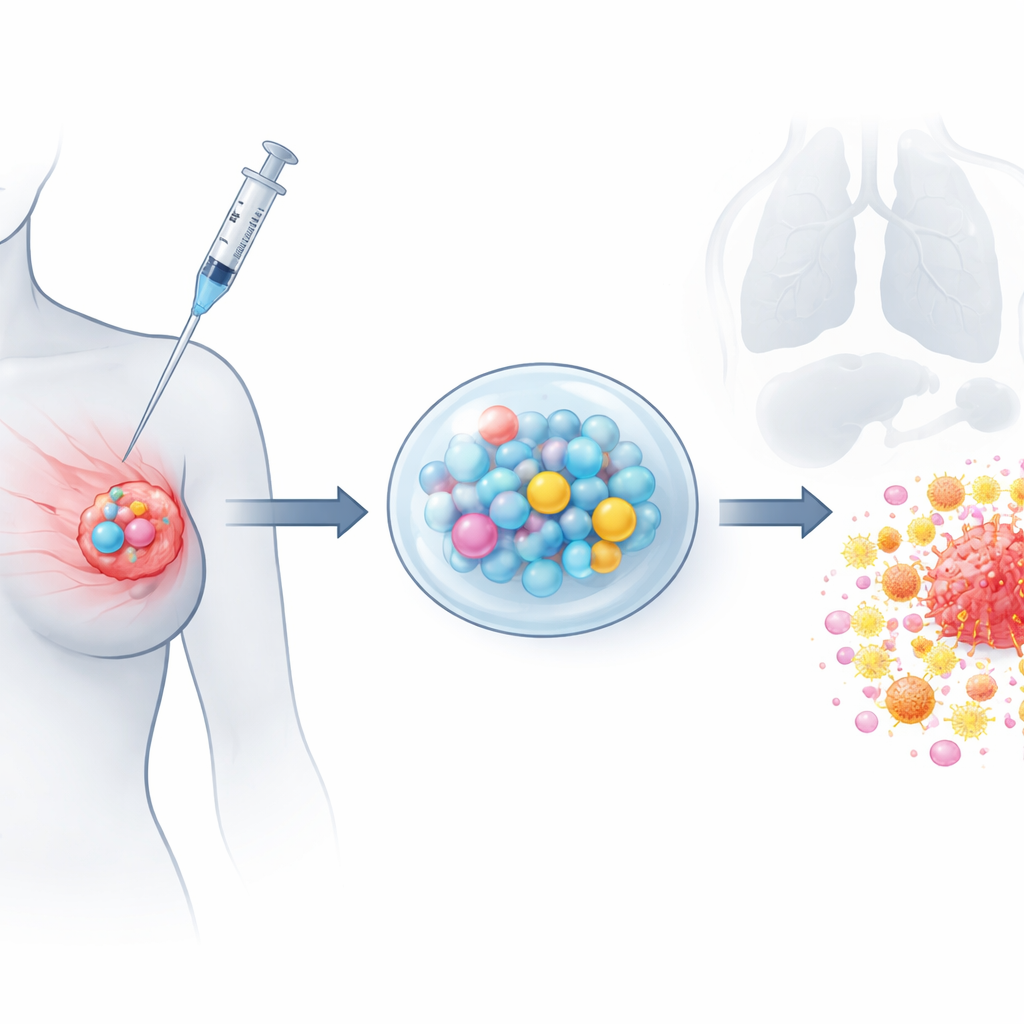
הנדסה של התקפה מוחשבת בשחרור מתוזמן
לבניית המערכת השתמשו בקבוצת החוקרים בשיטה חשמלית־גבוהה־מתח בשם “אלקטרוספריי” ליצירת מיקרו-כדורים אחידים טעונים בפאצ'יטקסל מפולימר ביודגרדבילי. דימות הראה חלקיקים חלקים וסילוניים בקוטר של כמאה־חמישית רוחב שערה אנושית, ובדיקות מעבדה אישרו שפאצ'יטקסל דלף בקביעות למשך לפחות חודש ללא שחרור פתאומי מוקדם. בנפרד, הם הטמיעו גמציטאבין ו‑CpG בג'ל רגיש לטמפרטורה שהוא נוזל כשהוא מקורר והופך לחצי-מוצק בטמפרטורת הגוף. טביעת אצבע כימית אישרה ששתי התרופות נשארו שלמות בתוך הנשאים שלהן. כאשר משולבים, הג'ל מספק מנת פתיחה מהירה של גמציטאבין ו‑CpG, בעוד המיקרו-כדורים מציעים טפטוף ממושך של פאצ'יטקסל, המדמה את היתרונות של כימותרפיה במינון נמוך לאורך זמן מטיפול מקומי יחיד.
מבחן האסטרטגיה המקומית בעכברים
הצוות בדק את PLICT במודל עכבר של סרטן שד טריפל-שלילי. בעכברים נוצרו תחילה גידולים קטנים בשד, ואז קיבלו או זריקות סטנדרטיות של פאצ'יטקסל בלבד, פאצ'יטקסל יחד עם גמציטאבין, או שתל מקומי יחיד של PLICT בסמוך לגידול. לאורך ארבעה שבועות, הגידולים בקבוצת הביקורת גדלו במהירות, אלה שקיבלו כימותרפיה סטנדרטית גדלו לאט יותר, אך הגידולים שטופלו ב‑PLICT היו קטנים בהרבה הן בגודל והן במשקל. דימות של כל בעל החיים ושל האיברים שנשלפו הראה ש‑PLICT גם צמצם את התפשטות הסרטן לאתרים מרוחקים, במיוחד לריאות, באופן אפקטיבי יותר מהזרקות תרופה קונבנציונליות. מדידות של ריכוזי תרופות הסבירו זאת: פאצ'יטקסל היה בריכוז גבוה בתוך גידולים שטופלו ב‑PLICT אך נמוך ברקמת שומן מרוחקת ודומה בזרם הדם, מה שמרמז על כליאה מקומית חזקה עם חשיפות פחותות לאתרים לא מיועדים.
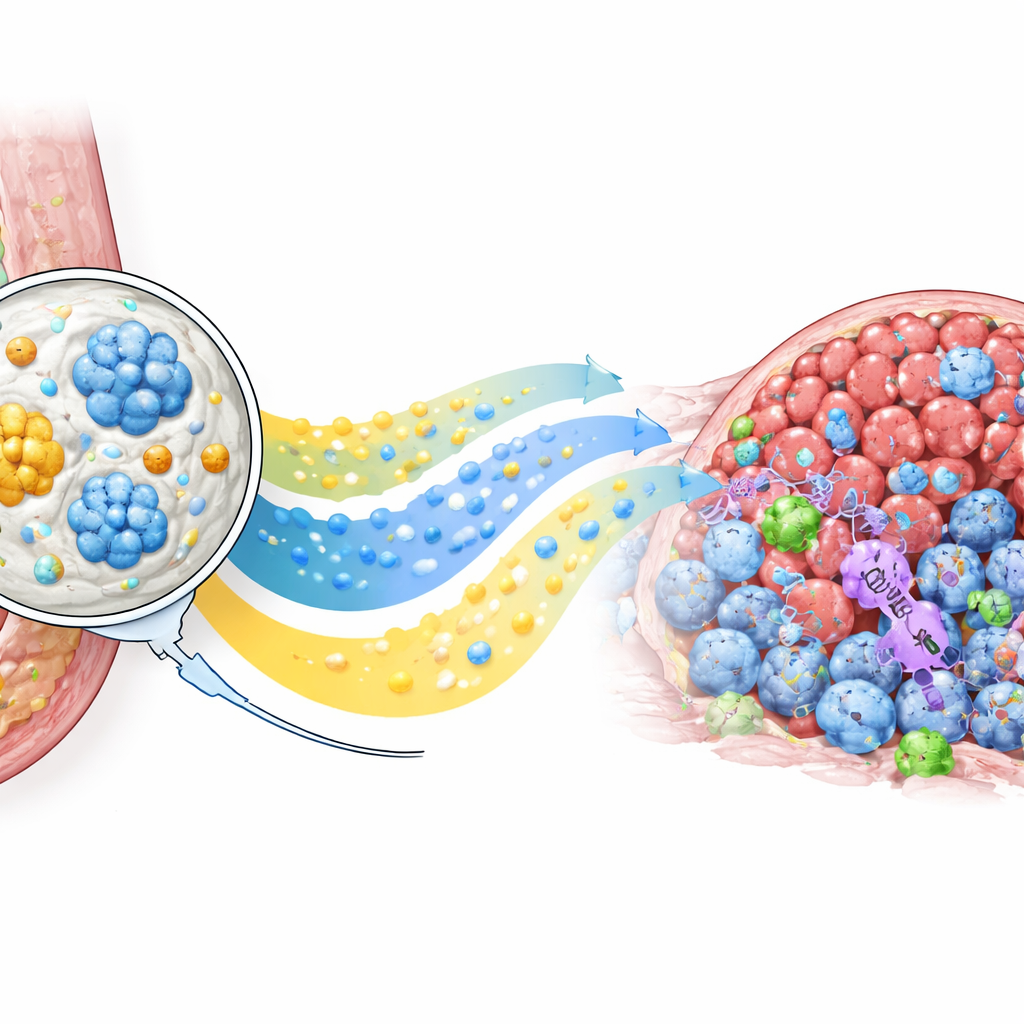
גיוס המגנים הטבעיים של הגוף
מעבר להקטנת הגידול, PLICT שינה את הנוף החיסוני בתוכו. ניתוחים תאיים מפורטים הראו עלייה חדה בתאי T CD8 הרוצחים סרטניים בגידולים שטופלו ב‑PLICT בהשוואה לכל הקבוצות האחרות, לצד ירידה בסוגי תאי T ויסותיים שמטבעם מדכאים התקפות חיסוניות. צביעת רקמות עבור CD69, סמן לתאי T שהופעלו לאחרונה, אישרה שרבים מהתאים שחדרו היו במצב פעיל ומוכנים לפעול. במקביל, כימותרפיה סטנדרטית גרמה לנזק ניכר לרקמת הכבד, בעוד שאיברים מעכברים שטופלו ב‑PLICT נראו כמעט תקינים במיקרוסקופ. יחד, הממצאים מצביעים שהמאגר המקומי לא רק מגביר את החשיפה הישירה של התרופות בגידול אלא גם מצית תגובה חיסונית נוחה יותר ופחות מדוכאת מבלי להוסיף עומס לאיברי מפתח.
מה זה עלול להשפיע על טיפולי סרטן בעתיד
ללא צורך בהתמחות עמוקה, המסר פשוט: על ידי הפיכת הכימותרפיה והגירוי החיסוני לטפטוף איטי ומופעל בשלבים, המובא ישירות לצד הגידול, הגישה הזאת השיגה שליטה חזקה יותר על הגידול ופחות תופעות לוואי מערכתיות בבעלי חיים לעומת הזרקות תרופה סטנדרטיות. העבודה עדיין נמצאת בשלב פרה-קליני, ונשארות שאלות לגבי איך מערכת כזו תתנהג בבני אדם או בהקשרים טיפוליים שונים. עם זאת, הקונספט של "מאגר תרופות" הניתן להזרקה ומתוכנת לשחרור שקט של סוכנים מרובים ברצף עלול לפתוח דרכים חדשות לטיפול בסרטן אגרסיבי כמו סרטן השד הטריפל-שלילי — לכוון את המאבק בדיוק במקום שבו הוא חשוב ביותר ובו בזמן לחסוך לשאר הגוף.
ציטוט: Hsieh, CH., Hsu, MY., Lin, CF. et al. Programmable local immunochemotherapy for triple-negative breast cancer via spatiotemporally controlled release of CpG oligodeoxynucleotides, gemcitabine, and paclitaxel. npj Breast Cancer 12, 45 (2026). https://doi.org/10.1038/s41523-026-00910-7
מילות מפתח: סרטן שד טריפל-שלילי, העברת תרופות מקומית, אימונותרפיה, שחרור מבוקר, מיקרושכיות הידרוג'ל