Clear Sky Science · he
אחבול משותף של כימוקין CXCL9 וליגנד קוסטימולרי TNFSF9 על ידי תאי גזע מזנכימליים משנה את המיקרו‑סביבה החיסונית בסרטן השד המשולש-שלילי
מדוע הגישה החדשה הזו בסרטן השד חשובה
סרטן השד המשולש‑השלילי הוא אחת הצורות המסוכנות ביותר של סרטן השד, משום שהוא גדל במהירות, מתפשט מוקדם ומחסיר את היעדים ההורמונליים הרגילים שעליהם נשענים תרופות רבות. אימונותרפיה העלתה תקוות, אך אצל מטופלים רבים תאי המגן של הגוף פשוט אינם חודרים אל הגידול בכמויות מספקות כדי לשנות את המצב. המחקר חוקר אסטרטגיה חדשנית: שימוש בתאי נשא חיים כ"משאיות מסירה" מודרכות שמביאות אותות מחזקי חיסון ישירות אל גידולים קשים לטיפול, מה שעשוי להפוך יותר מטופלים לבעלי זכאות לטיפולים אימונולוגיים רבי עוצמה.
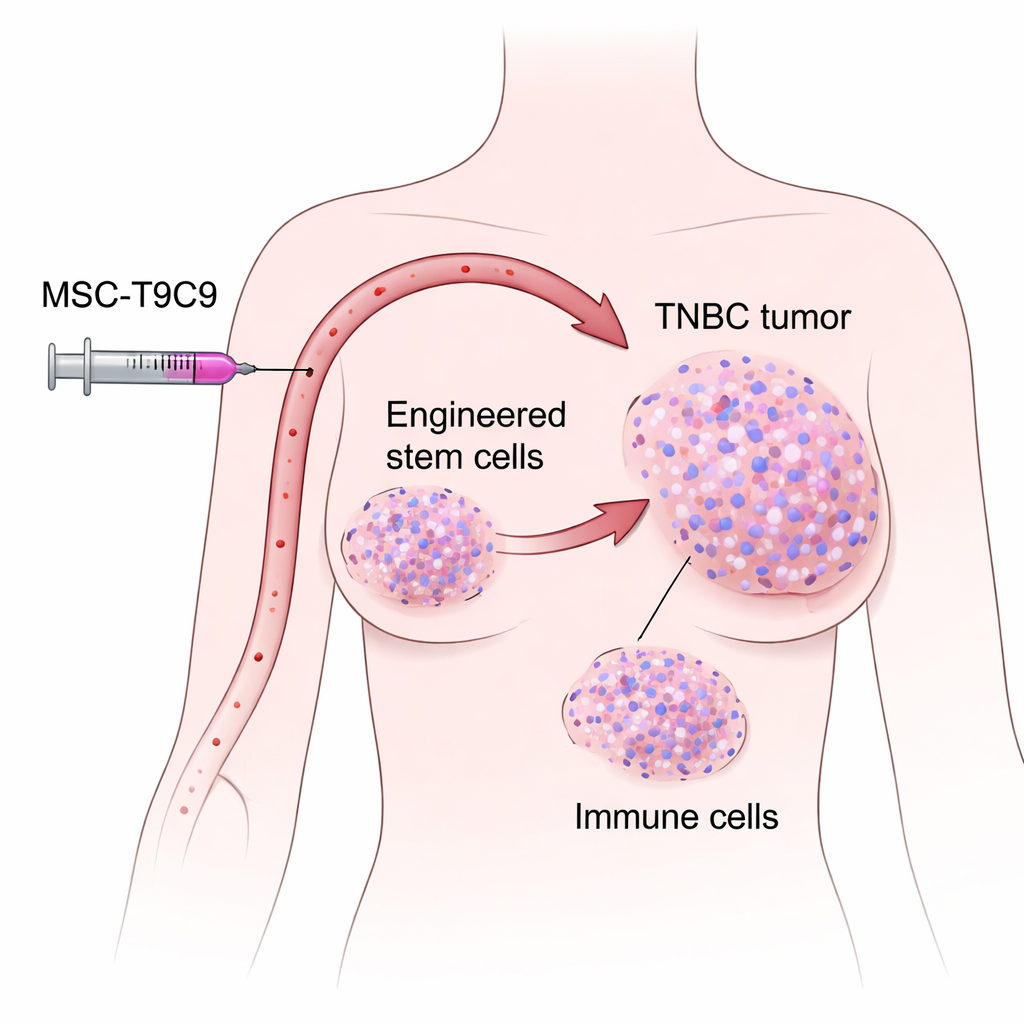
גידול קשה שמקבל מעט סיוע חיסוני
הטיפולים הסטנדרטיים בסרטן השד המשולש‑השלילי — ניתוח, כימותרפיה וקרינה — לעתים קרובות אינם מונעים הישנות, והתוחלת לחיים במצב מתקדם נותרת פחות משנתיים בממוצע. סיבה מרכזית לכך היא שרבים מהגידולים האלה הם "קרים", כלומר הם מכילים מעט תאי חיסון לוחמי סרטן. מאגרי נתונים גדולים של מטופלים הראו שאצל אנשים שהגידולים שלהם מייצרים באופן טבעי כמויות גבוהות יותר של שני המולקולות הקשורות לחיסון, CXCL9 ו‑TNFSF9, יש מגמה לחיים ארוכים יותר ולנוכחות רבה יותר של תאי T ותאי NK בתוך הגידול. CXCL9 הוא אות כימי שמזמין תאי חיסון לרקמה, בעוד TNFSF9 פועל כמו מתג "הפעל" נוסף שעוזר לתאים הללו לתקוף בעוצמה רבה יותר. הדפוס הציע שהגבהת שני האותות ישירות בתוך הגידולים עשויה להטות את המאזן לטובת מערכת החיסון.
הפיכת תאי גזע למשאיות מסירה חכמות
החוקרים התמקדו בתאי גזע מזנכימליים שנלקחו מחבל טבור אנושי נתון. לתאים אלה תכונה שימושית: כאשר מוזרקים למחזור הדם של עכברים הנושאים גידולי שד, הם נוטים באופן טבעי למקם עצמם באתרי הגידול ולשכון שם למשך ימים, בעוד שהם נמנעים ברובם מאיברים בריאים. הצוות הנדס גנטית את תאי הגזע האלה כך שישחררו CXCL9 ויציגו על פני שטחם את TNFSF9, ויצרו טיפול תאי דו‑תכליתי שהם קוראים לו MSC‑T9C9. ניסויים במעבדה הראו שהתאים המותאמים שחררו רמות גבוהות של CXCL9 והפעילו בעוצמה תאי T ותאי NK של עכברים, מבלי לשנות את התנהגות הגדילה שלהם או לגרום לגידולים בעצמם. זה הפך אותם למועמדים מבטיחים כתומכי חיסון ממוקדים.
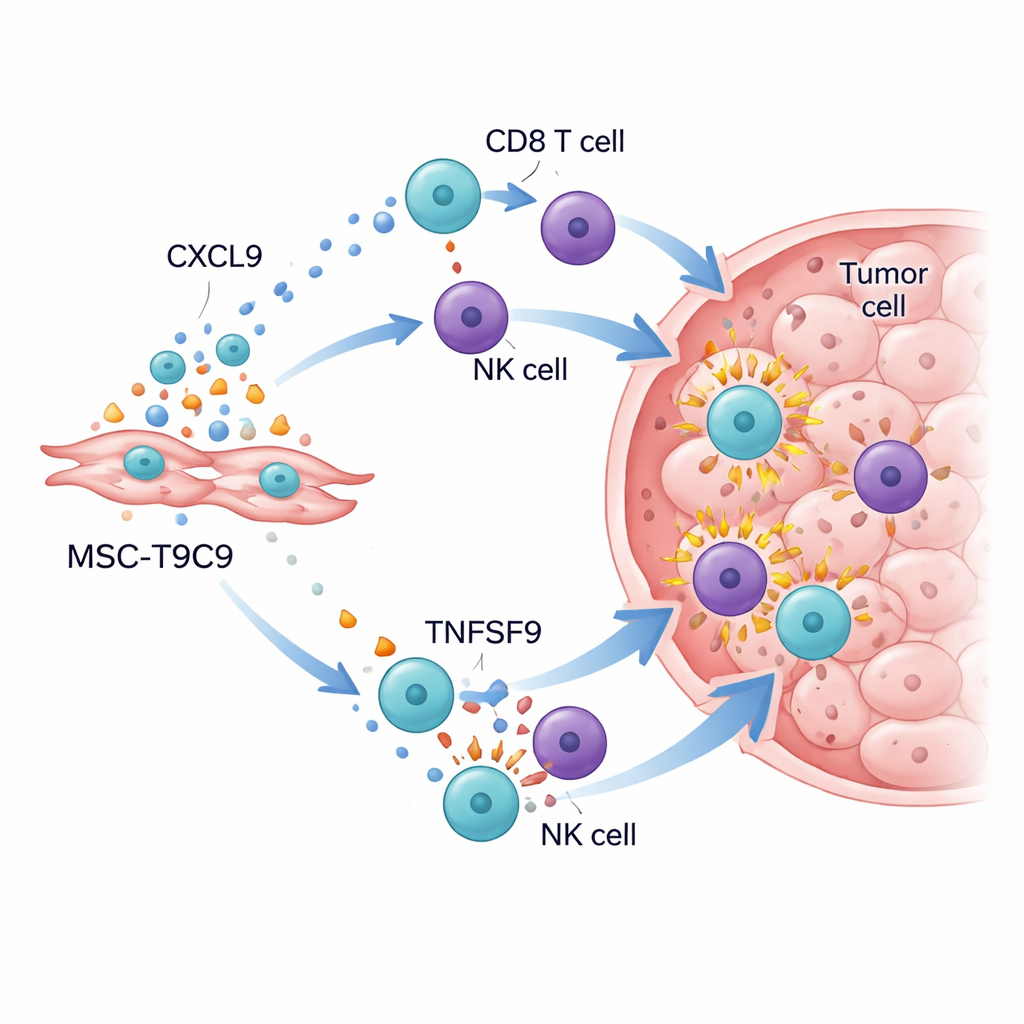
העירה את שדה הקרב החיסוני של הגידול
כאשר התאים המהונדסים ניתנו לעכברים שסבלו מגידולי שד משולש‑שליליים, התוצאות היו מרשימות. בעכברים בעלי מערכת חיסון פועלת, זריקות חוזרות של MSC‑T9C9 האטו במידה ניכרת את גדילת הגידול והעלו את תמותת תאי הסרטן, בעוד שתאי גזע בקרה לא הראו אפקט משמעותי. ניתוח מפורט של הגידולים הראה עלייה דרמטית במספר תאי T "רוצחים" מסוג CD8 ובתאי NK, לצד רמות גבוהות יותר של מולקולות התקפה עוצמתיות כגון גרנזים B, אינטרפרון‑γ, פקטור נמק הגידול‑α ואינטרלוקין‑2. במקביל, סביבת הגידול התרחשה הרחק ממצב מדכא: מאקרופאגים דלקתיים תורמים עלו במספרם, ולמרות שתאי T רגולטוריים היו עדיין נוכחים, הם הובסו מבחינת יחס על‑ידי גל הלוחמים החדש. בעכברים חסרי מערכת חיסון, שבהם תאי T ותאי NK חסרים, MSC‑T9C9 לא האטה את גדילת הגידול, מה שאישר שהמועילות שלה תלויה בגיוס ההגנות של הגוף עצמו.
הכנת גידולים לטיפולי נקודות בדיקה
תרופות אימונותרפיות מודרניות כמו נוגדנים נגד PD‑1 משחררות "בלמים" מולקולריים על תאי T, אך הן עובדות טוב יותר כאשר כבר קיימים מספיק תאי T בתוך הגידול. המחקר מצא ש‑MSC‑T9C9 לא רק משכה יותר תאי CD8 אל הגידולים, אלא גם דחפה אותם למצב פעיל מאוד, אך רגיש לבלמים, המסומן על‑ידי הקולטן PD‑1. במודל עכבר, שילוב של MSC‑T9C9 עם תרופה אנטי‑PD‑1 הניב את כיווץ הגידולים החזק ביותר וההישרדות הארוכה ביותר בהשוואה לכל טיפול בנפרד. ניתוחים של מאגרי נתוני סרטן אנושיים תמכו ברעיון זה: מטופלים עם רמות משולבות גבוהות יותר של TNFSF9 ו‑CXCL9 נטו להפיק תועלת רבה יותר מטיפולי חסימת נקודות בדיקה, מה שמעיד כי הביולוגיה הזו עשויה לחול גם בבני אדם.
בטיחות ותקווה לעתיד
כל טיפול שמגביר את החיסון מעלה חששות מתופעות לוואי מסוכנות כגון דלקת מפושטת או נזק לאיברים. לעומת זאת, בעכברים שקיבלו MSC‑T9C9 נשמרו משקל והתנהגות תקינים, לא נצפו פגיעות ברורות באיברים עיקריים ותוצאות בדיקות דם ותפקודי כבד‑כליה היו תקינות. חשוב מכך, גל הפעילות החיסונית היה מוגבל ברובו לגידול עצמו, ואותות דלקתיים במחזור הדם לא עלו. בעוד שיש עוד עבודה לפני ניסויים בבני אדם — כולל בדיקות במודלים ריאליסטיים יותר ומציאת מינון מדויקת — מחקר זה מציע כי הנחיית תאי גזע מהונדסים אל הגידולים כדי לזמן ולהפעיל תאי חיסון יכולה להציע דרך ממוקדת ובטוחה יותר להפוך גידולים "קרים" של סרטן השד המשולש‑השלילי ל"חמים" שיגיבו טוב יותר לאימונותרפיה.
ציטוט: Ye, P., Wen, Y., Liu, R. et al. Co-delivery of chemokine CXCL9 and costimulatory ligand TNFSF9 by mesenchymal stem cells reprograms the immune microenvironment for triple-negative breast cancer. npj Breast Cancer 12, 30 (2026). https://doi.org/10.1038/s41523-026-00893-5
מילות מפתח: סרטן השד המשולש-שלילי, אימונותרפיה, תאי גזע מזנכימליים, מיקרו‑סביבת הגידול, חסימת נקודות בדיקה