Clear Sky Science · he
אינטרלוקין-1α שמקורו במארח מייצר דיכוי חיסוני של הגידול על‑ידי תכנות מחדש של תאים מיאלואידיים מקושרי גידול
מדוע מחקר זה חשוב לחולות ולחולי סרטן
אימונותרפיה שינתה את הנוף הטיפולי עבור כמה סוגי סרטן, אך גידולי שד רבים עדיין מתחמקים ממערכת החיסון. המאמר חוקר עבריין פחות מוכר: מולקולת איתות בשם אינטרלוקין‑1 אלפא (IL‑1α) המיוצרת לא על‑ידי תאי הסרטן עצמם אלא על‑ידי תאים נורמליים בגוף. המחברים מראים כי IL‑1α שמגיעה מהמארח יכולה בשקט להפוך תאי חיסון לבעלי ברית של הגידול, וחסימת האות הזה בעכברים עשויה להוביל לכיווץ או להיעלמות של גידולי שד. הבנת המתג הזה עשויה לסייע לרופאים לעצב טיפולים שעושים את האימונותרפיה ליעילה יותר בסרטן השד.
משפיע מוסתר בשכונת הגידול
גידולים אינם גדלים בבידוד; הם חיים ב"שכונה" עמוסה של תאי חיסון, כלי דם ורקמה חיבורית המכונה מיקרו‑סביבת הגידול. בין התושבים החשובים ביותר נמצאים תאים מיאלואידיים, ובמיוחד מאקרופאגים, היכולים להילחם בגידול או להגן עליו. ספרי לימוד קלאסיים מחלקים מאקרופאגים ל‑M1 (נלחמים בגידול) ול‑M2 (תומכים בגידול), אך בגידולים אמיתיים יש הרבה גוונים ביניהם. המחברים התמקדו ב‑IL‑1α, מולקולה שמיוצרת בדרך כלל על־ידי רקמות לא סרטניות, כדי לבדוק האם האות הזה מהמארח מוביל תאים מיאלואידיים תוקפים או תומכים בתוך גידולי שד.
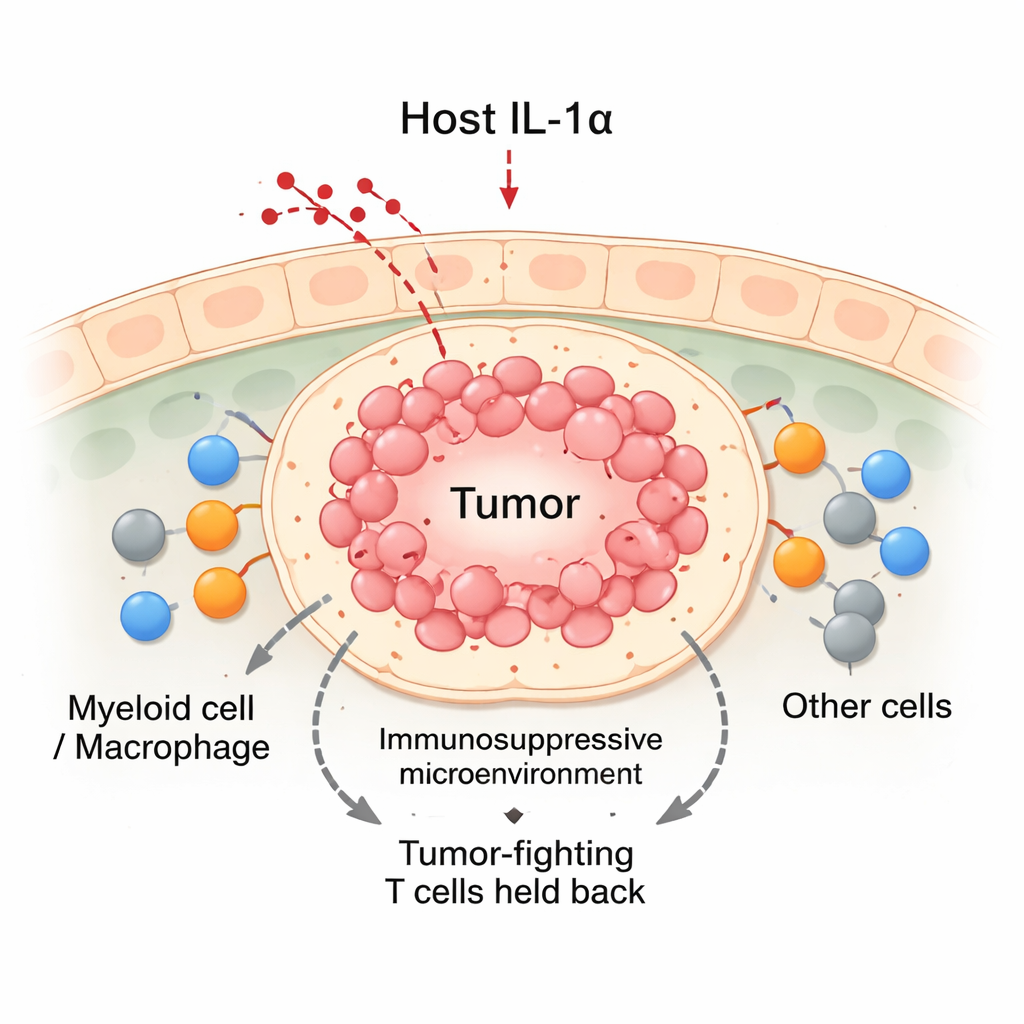
כיבוי IL‑1α מזיז את האיזון נגד הגידול
באמצעות דגמי עכבר של סרטן השד השוו החוקרים בעלי חיים רגילים לאחרים מהונדסים גנטית שלא מייצרים IL‑1α. כאשר תאי סרטן השד הושתלו בבלוטות החלב, הגידולים בעכברים רגילים גדלו בהתמדה. לעומת זאת, בגידולים בעכברי חסרי IL‑1α הצמיחה נמשכה ככישבועיים ואז לעתים קרובות נרשמה נסיגה. גידולים אלה שכחנוו הכילו בסך הכל יותר תאי חיסון, כולל גל ציטוטוקסי של תאי T מסוג CD8 ותאים מיאלואידיים. אף על פי שלעכברי IL‑1α חסר היו פחות תאי דם לבנים במחזור הדם, הם ריכזו הרבה יותר תאי חיסון באתר הגידול. ניתוחים מפורטים הראו שתאי CD8 שחדרו לגידולים חסרי IL‑1α היו פעילים יותר, ייצרו רמות גבוהות יותר של מולקולות ההורגות גידול והפגינו פחות סימני תשישות.
כיצד IL‑1α מעצבת את התאים המיאלואידיים המקושרים לגידול
כדי להבין מה עושה IL‑1α ברמת התאים, החוקרים השתמשו בריצוף RNA של תא בודד כדי לבחון אלפי תאים בודדים מהגידולים. הם גילו שרק תת‑קבוצה קטנה של מאקרופאגים מקושרי גידול — אלה המסומנים בקולטן הנקרא CX3CR1 — ייצרו IL‑1α. בעכברים רגילים מונוציטים נכנסים רבים התמיינו למאקרופאגים החיוביים ל‑CX3CR1, הקשורים להתנהגות מדכאת חיסון. בעכברים חסרי IL‑1α נתיב ההבשלה הזה השתבש. במקום זאת, תאים מיאלואידיים נטו יותר להפוך למאקרופאגים דלקתיים חיובי iNOS, פרופיל המקושר לפעילות אנטי‑גידולית. מבחינה פונקציונלית, תאים מיאלואידיים מגידולים חסרי IL‑1α היו פחות מסוגלים לגרום להגברה של מעצורים כמו PD‑1 ו‑CTLA‑4 על תאי T, והראו יכולת חלשה יותר לדכא פרוליפרציית תאי T.
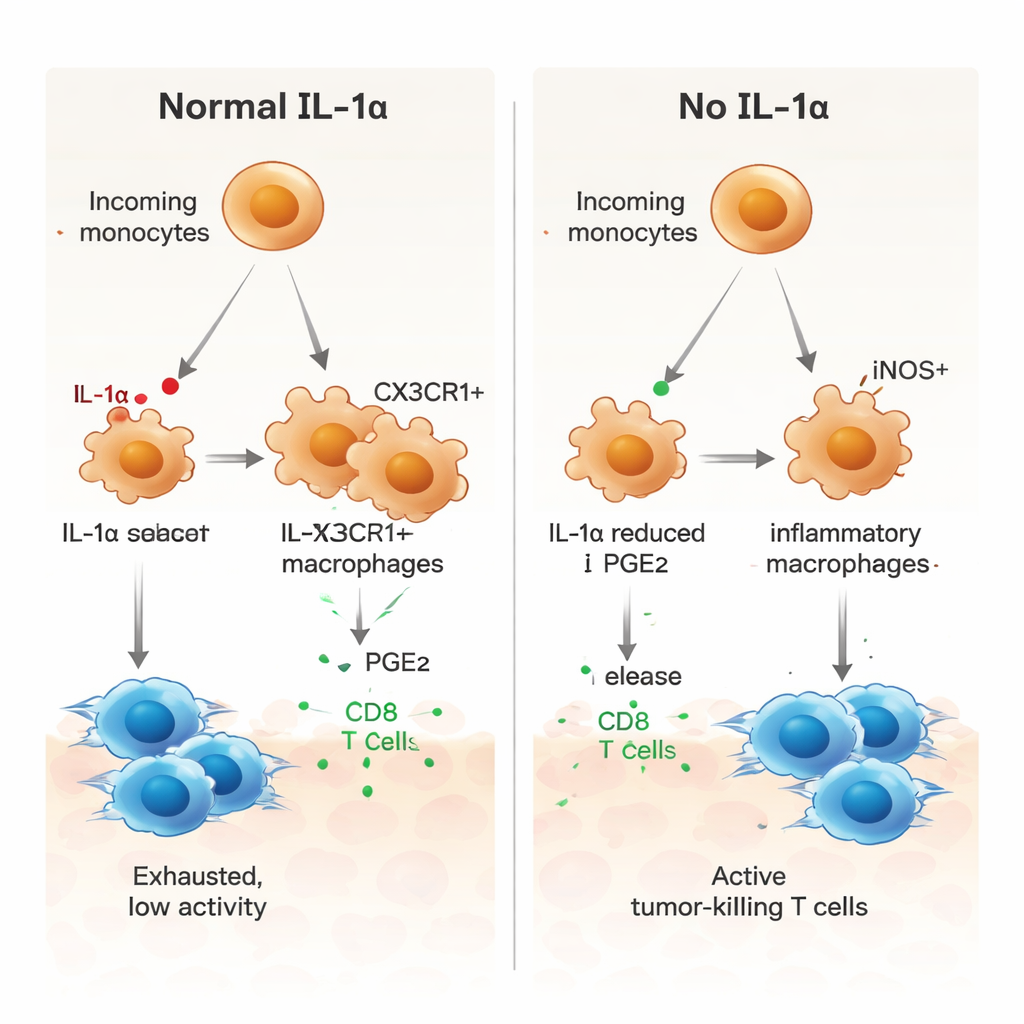
תפקיד מפתח של שליח שומני, PGE2
המחברים שאלו אז כיצד IL‑1α דוחפת תאים מיאלואידיים למצב תומך‑גידול. ניתוח התקשורת של נתוני התא היחיד הצביע על מספר מסלולי איתות, כולל אחד הכולל פרוסטגלנדין E2 (PGE2), מוליך שומני הידוע בקידום דיכוי חיסוני. בגידולים חסרי IL‑1α, מאקרופאגים הראו ביטוי נמוך יותר של קולטנים לגורם גדילה של מאקרופאג' (M‑CSF), לקולטני TGF‑β ולקולטן ל‑PGE2, ותאי סטרומה סמוכים ייצרו פחות מהאנזימים שמייצרים PGE2. בתרביות מעבדה, מאקרופאגים שמקורם במח עצם של עכברי IL‑1α חסר הציגו פרופיל דלקתי יותר, עם iNOS גבוה יותר ו‑CX3CR1 נמוך יותר. הוספת PGE2 הפכה את השינוי הזה והחזירה דפוס מדכא יותר, בעוד חסימת PGE2 במאקרופאגים רגילים דחפה אותם למצב פרו‑דלקתי. מאקרופאגים ללא IL‑1α גם גירו חזק יותר פרוליפרציה של תאי CD8 ספציפיים לגידול, השפעה שנחלשה כאשר הוסיפו מחדש PGE2.
גשר בין ממצאים בעכברים לחיסון אנושי
כדי לבדוק האם נתוני העכבר משקפים ביולוגיה אנושית, הצוות השווה חתימות גנטיות מהתתי‑אוכלוסיות השונות של מאקרופאגים בעכברים ללוח גדול של תאים מיאלואידיים אנושיים שמולאו למצבים שונים במעבדה. אשכולות המאקרופאגים בגידולים של עכברים רגילים הדמו תאים אנושיים שנדחפו למצב דמוי M2 המדכא חיסון על‑ידי מולקולות כגון IL‑10, IL‑4 וגלוקוקורטיקואידים. לעומת זאת, אותם אשכולות מגידולים חסרי IL‑1α תיאמו תאים אנושיים במצבים דלקתיים יותר ופחות מדכאים. באופן בולט, דפוסים גנטיים הקשורים לאיתות PGE2 הורבו באשכולות התלויים ב‑IL‑1α אך נעדרו כאשר IL‑1α חסר, מה שמחזק את הרעיון ש‑IL‑1α ו‑PGE2 פועלים יחד לבניית נישה מדכאת חיסון.
מה המשמעות של זה עבור טיפולים עתידיים בסרטן השד
באופן פשוט, המחקר מציע שמולקולה שמקורה במארח, IL‑1α, יכולה בשקט לומר למאקרופאגים מסוימים להגן על הגידול ולשמור על תאי ה"הורגים" CD8 במצב פחות פעיל, בחלקה באמצעות איתות PGE2. כשמסירים IL‑1α בעכברים, המאקרופאגים נוטים יותר למצב דלקתי התוקף גידול, תאי CD8 נעשים פעילים יותר וגידולי שד שהושתלו לעתים נדחים עם דחייה. מאחר שאימונותרפיות קיימות כבר שואפות להחזיר כוח לתאי T מותשים, שילוב שלהן עם גישות החוסמות את IL‑1α או את מסלול ה‑PGE2 היורד עשוי להטות עוד יותר את מיקרו‑הסביבה של הגידול לטובת מערכת החיסון של המטופל. למרות שדרוש עוד מחקר כדי לבדוק בטיחות ויעילות בבני אדם, הממצאים מצביעים על IL‑1α כיעד מבטיח להפוך את סרטן השד לפגיע יותר להתקפה חיסונית.
ציטוט: Keerthi Raja, M.R., Gupta, G., Atkinson, G. et al. Host-derived interleukin-1α drives tumor immunosuppression by reprogramming tumor-associated myeloid cells. npj Breast Cancer 12, 26 (2026). https://doi.org/10.1038/s41523-026-00890-8
מילות מפתח: אימונותרפיה של סרטן השד, מיקרו‑סביבת הגידול, תאי מאקרופאג', אינטרלוקין‑1 אלפא, פרוסטגלנדין E2