Clear Sky Science · he
דימות מטבולי בזמן אמת וברזולוציה גבוהה של חיידקים חיים ללא תיוג
צפייה במיקרובים מגיבים בזמן אמת
חיידקים נמצאים בכל מקום על ובתוך גופנו, ומשפיעים בעדינות על הבריאות שלנו. הם מסייעים לעיכול, מגנים על העור ולעתים גורמים לזיהומים עקשניים שמגיבים בקושי לאנטיביוטיקה. המחקר מציג שיטה לצפייה בחיידקים חיים מגיבים ללחץ ולתרופות בזמן אמת, ברמת תא יחיד, ללא הוספת צבעים או תגיות. היכולת הזו עשויה בעתיד לסייע לרופאים לבחור טיפול נכון מהר יותר ולעזור למדענים להבין מדוע חלק מהזיהומים קשים לריפוי.
האור כחלון לחיי החיידק
במקום להוסיף צבעים או תויות גנטיות, החוקרים נשענים על העובדה שחיידקים זוהרים באופן חלש כשהמולקולות מסוימות בתוכם נרגשות מאור לייזר. שתי מולקולות אלה, הידועות כ‑NAD(P)H ו‑FAD, הן שחקניות מרכזיות באופן שבו תאים ממירים מזון לאנרגיה. באמצעות מיקרוסקופיית לייזר מהירה ובעלת רזולוציה גבוהה, הצוות יכול למדוד גם את העוצמה וגם את העיכוב הקטן של הזוהר הזה, ולחשוף כמה פעיל המטבוליזם של התא. מאחר שהשיטה אינה דורשת תיוג ואינה הרסנית, ניתן לעקוב אחר אותם חיידקים חיים במשך שניות ודקות כשהסביבה שלהם משתנה. 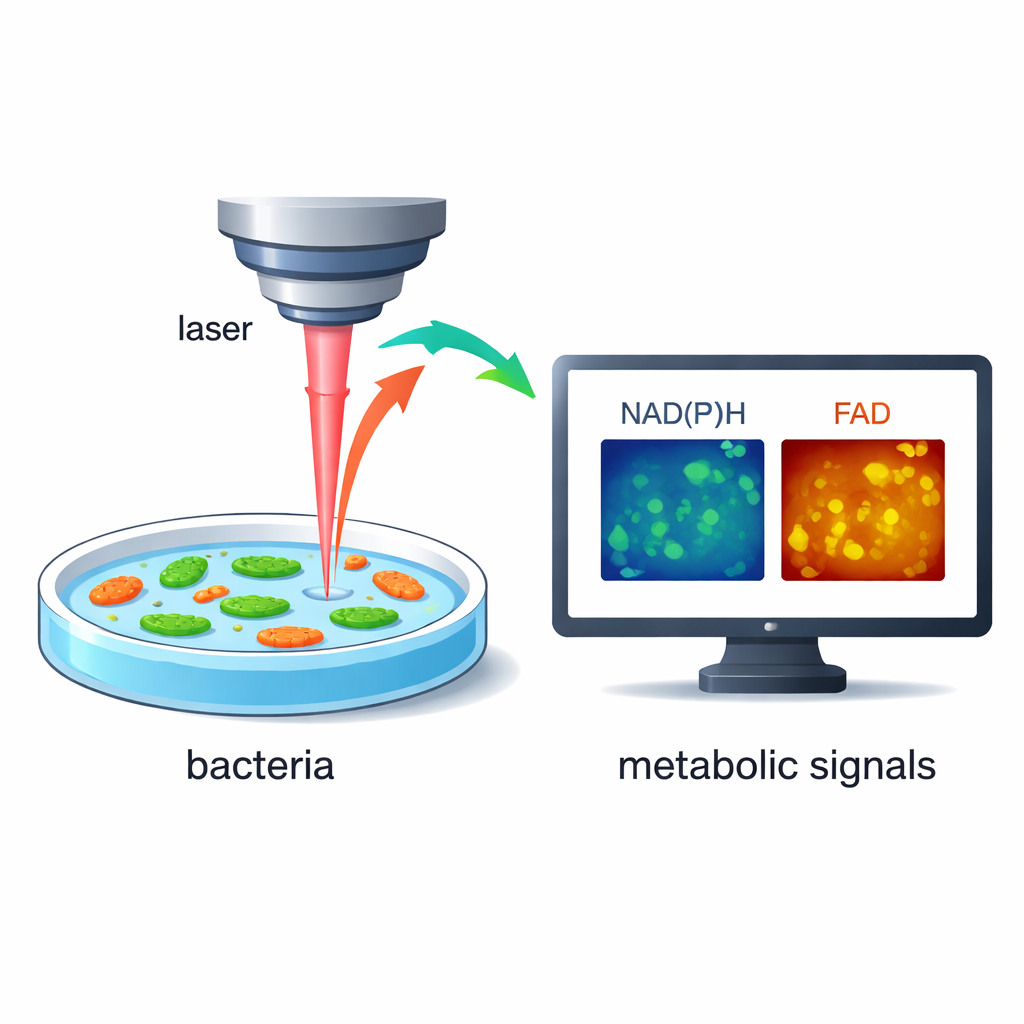
זיהוי הבדלים בין חיידקים בודדים
רוב הבדיקות המעבדה הסטנדרטיות מאחדות מיליוני חיידקים ומדווחות רק על תגובה ממוצעת. כאן מראים המחברים ששיטת הדימות שלהם יכולה לאתר תאי Staphylococcus aureus בודדים בתרבית נוזלית ולנתח כל אחד מהם בנפרד, אפילו בצפיפויות תאים גבוהות. כאשר השוו בין שתי מושבות S. aureus שגודלו בתנאים זהים, אות מרכזי אחד (מ‑FAD) השתנה בין המושבות, והייתה גם שונות של ערכים בתוך כל מושבה. משמעות הדבר היא שאפילו חיידקים דומים גנטית באותו בקבוק יכולים להיות במצבים מטבוליים מאוד שונים — שונות נסתרת שבדיקות מסה עשויות לפספס אך שלעיתים חשובה לתגובת הזיהום לטיפול.
צפייה במתקפת אנטיביוטיקה בתוך שניות
הצוות עקב אחר תאי S. aureus בודדים בזמן שנחשפו למספר טיפולים אנטיבקטריאליים, כולל אנטיביוטיקות נפוצות וחומר הלבנה ביתי. באמצעות מערך הדימות המהיר שלהם, הם תיעדו שינויים מהרגע שבו תמיסת התרופה נגעה בתאים ועד 30 הדקות הבאות. טיפולים חזקים גרמו לירידה באותות NAD(P)H ועלייה באותות FAD, לעיתים בתוך שניות, מה שמשקף עצירת ייצור אנרגיה והסטה למצב מחמצן יותר בתא. הזמנים והדפוסים המדויקים של השינויים הללו תלויים בסוג התרופה ובמינון: למשל, אנטיביוטיקות החוסמות חלבונים או תוקפות את דופן התא הראו ירידה קצרה והתאוששות חלקית, בעוד שחומר הלבנה הניע שינוי חד ומתמשך. "חתימות האור" המובחנות הללו מציעות שהשיטה יכולה לזהות לא רק האם התאים לחוצים או מתים, אלא גם כיצד הם ניזוקים. 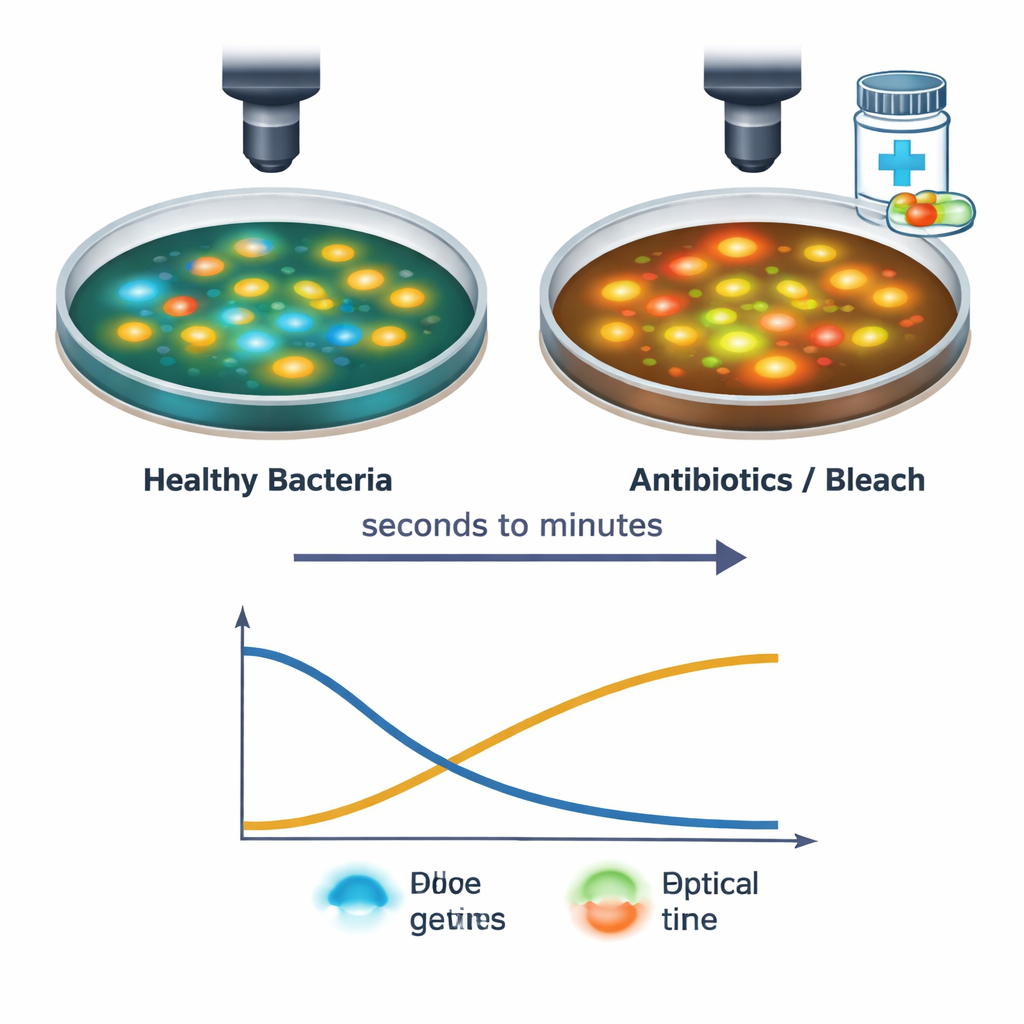
מציצים לעולם הנסתר של ביופילמים
חיידקים כמעט אף פעם לא חיים לבדם בטבע; במקום זאת הם בונים קהילות דביקות ומגוננות הנקראות ביופילמים על פני שטחים שמתחילים מהשתלים רפואיים ועד השיניים. בשכבות צפופות אלה, חלק מהתאים עשויים להיות מאוד פעילים בעוד אחרים רדומים — תערובת שמסייעת לקהילה לשרוד אנטיביוטיקה. באמצעות תמונות תפורות רחבות, החוקרים מיפו את הנוף המטבולי בתוך ביופילמים של S. aureus והשוו זאת לתאים שחיים חופשי. הם מצאו כיסים בוהקים ופעילים מטבולית מוקפים באזורים פחות פעילים והראו כי, במספר מינים, חיידקי ביופילם נוטים לפרופיל מטבולי מחומצן יותר מאשר עמיתיהם החופשיים. אותות אופטיים נוספים הצביעו על שומנים וחלבונים נוספים, בהתאם לחומר הדביק שמחזיק את הביופילם יחד.
מדוע זה חשוב לרפואה העתידית
ביחד, התוצאות מראות שדימות מטבולי אופטי ללא תיוג יכול לספק תמונות מהירות, מפורטות ולא חודרניות של האופן שבו חיידקים חיים, מתאימים ומתים. לקורא כללי, המסר המרכזי הוא שמדענים יכולים כעת "להאזין" לשימוש האנרגיה של חיידקים בזמן אמת, ללא הפרעה לתאים, בעזרת אור מכוון בקפידה. בטווח הארוך, סוג טכנולוגיה זה יכול לסייע לזהות חיידקים שקשה לגדל, לחשוף כיסים של תאים עמידים בתוך ביופילמים, או לבחון במהירות כיצד זיהום של מטופל מגיב לאנטיביוטיקות שונות. זה עשוי לתמוך בטיפולים מהירים ומותאמים יותר ולהעמיק את הבנתנו את העולמות המיקרוביאליים הבלתי נראים שמשפיעים על בריאותנו מדי יום.
ציטוט: Sorrells, J.E., Yang, L., Iyer, R.R. et al. Real-time, high-resolution metabolic characterization of live bacteria using label-free optical metabolic imaging. npj Biofilms Microbiomes 12, 55 (2026). https://doi.org/10.1038/s41522-026-00920-0
מילות מפתח: מטבוליזם חיידקי, דימות אופטי, ביופילם, תגובה לאנטיביוטיקה, מיקרוביום