Clear Sky Science · he
אינטראקציה של אצטילציה של חומצה סיאלית בגולג'י התלויה ובעלת-עצמאות מ‑SLC33A1 בקטליזה של CASD1
איך שינויים זעירים בסוכרים מעצבים בריאות ומחלה
התאים שלנו מכוסים בשרשרות סוכר מורכבות המשמשות כמו תעודות זהות מולקולריות, ומכוונות את המערכת החיסונית, ההתפתחות ואפילו את אופן היצמדות הווירוסים. המחקר הזה בוחן שינוי עדין אך בעל עוצמה בסוכרים אלה — הוספת "כובעים" כימיים קטנים שנקראים קבוצות אצטיל לסוכר קצה בשם חומצה סיאלית — וחושף מכונה מולקולרית דו־חלקית מפתיעה ששולטת בתהליך זה בתוך גולג׳י התא. הבנת המערכת החבויה הזו מסייעת להסביר כמה הפרעות נוירולוגיות קשות ומספקת רמזים לאופן שבו תאים מכווננים בעדינות את המשטחים שלהם במצב בריאות ובמחלה. 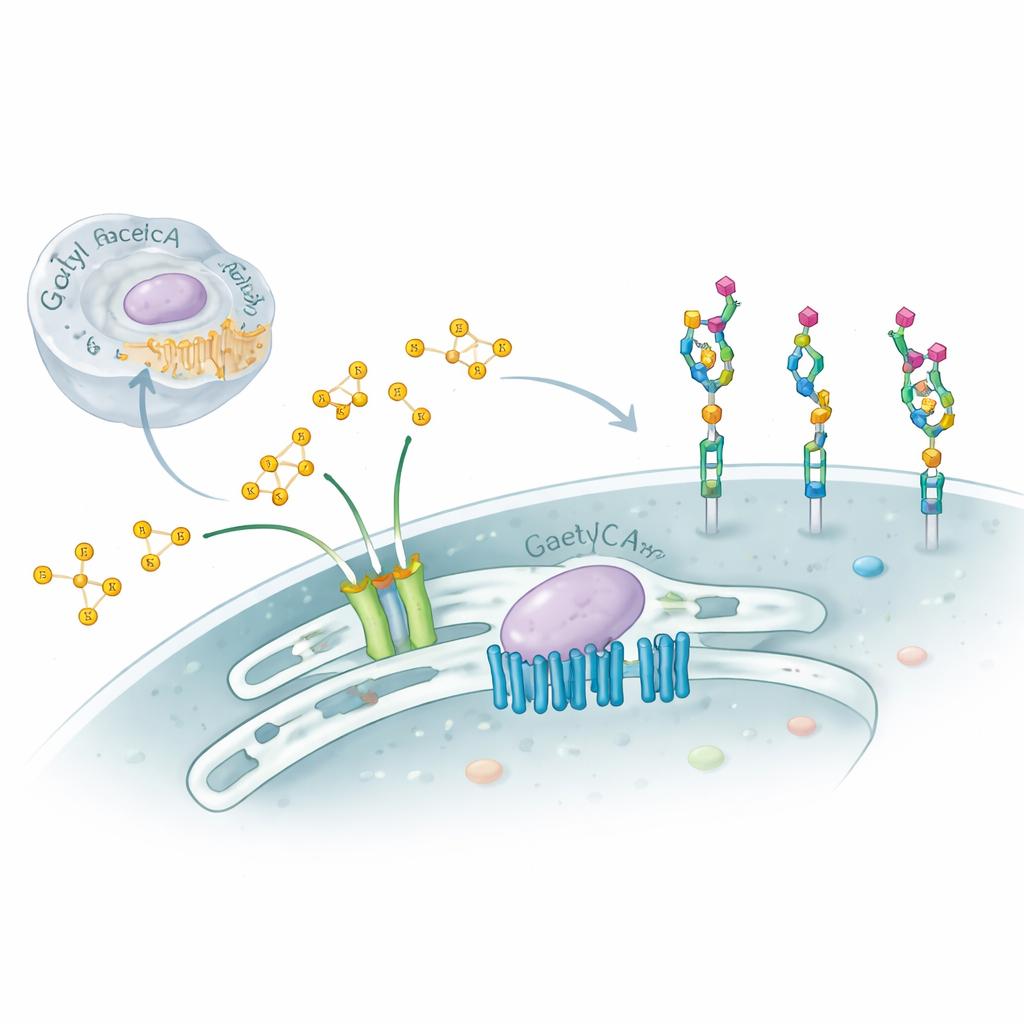
הסוכרים המיוחדים על פני התא
חומצות סיאליות יושבות בקצות החיצוניים של הרבה סוכרים על פני התא, על חלבונים וליפידים, ובמיוחד על מולקולות שנקראות גאנגליוזידים במוח. על ידי שינוי קל של חומצות סיאליות — כמו הוספת אחת או שתי קבוצות אצטיל בעמדות ספציפיות — תאים יכולים להסתיר אתרי זיהוי קיימים או ליצור אתרים חדשים. וירוסים כמו שפעת C וכמה קורונוויירוסים מחפשים במדויק את הסוכרים המומתנים הללו, וגאנגליוזידים אצטילטיים יכולים להשפיע על הישרדות או מוות של נוירונים וכן על התנהגות סרטן. למרות חשיבותם, המנגנונים הפנימיים של מכונת התא שמניחה את קבוצות האצטיל בגולג׳י נותרו לא מובנים היטב.
מוביל וחנקן-מעביר (אנזים) עובדים יד ביד
החוקרים התמקדו בשני חלבונים הנמצאים בתוך או סביב הגולג׳י: SLC33A1, נשא שמוביל אצטיל‑CoA (תורם האצטיל העיקרי של התא) דרך ממברנות, ו‑CASD1, אנזים הידוע כמעביר קבוצות אצטיל לחומצה סיאלית. באמצעות עריכת גנים בקווי תאים אנושיים וחמאריים הם הסירו את SLC33A1 וצפו במה שקרה לגאנגליוזידים ספציפיים. תאים ללא SLC33A1 יכלו עדיין לייצר את הגאנגליוזידים הבסיסיים GD3 ו‑GD2, אך איבדו לחלוטין את הצורות 9‑O‑אצטילטיות, שינוי סימני הכר שמקושר לסרטן ולתפקוד עצבי. החזרת SLC33A1 האנושי שיקמה את הגאנגליוזידים האצטילטיים, מה שמראה ש‑SLC33A1 הוא ספק קריטי של אצטיל‑CoA למסלול זה. 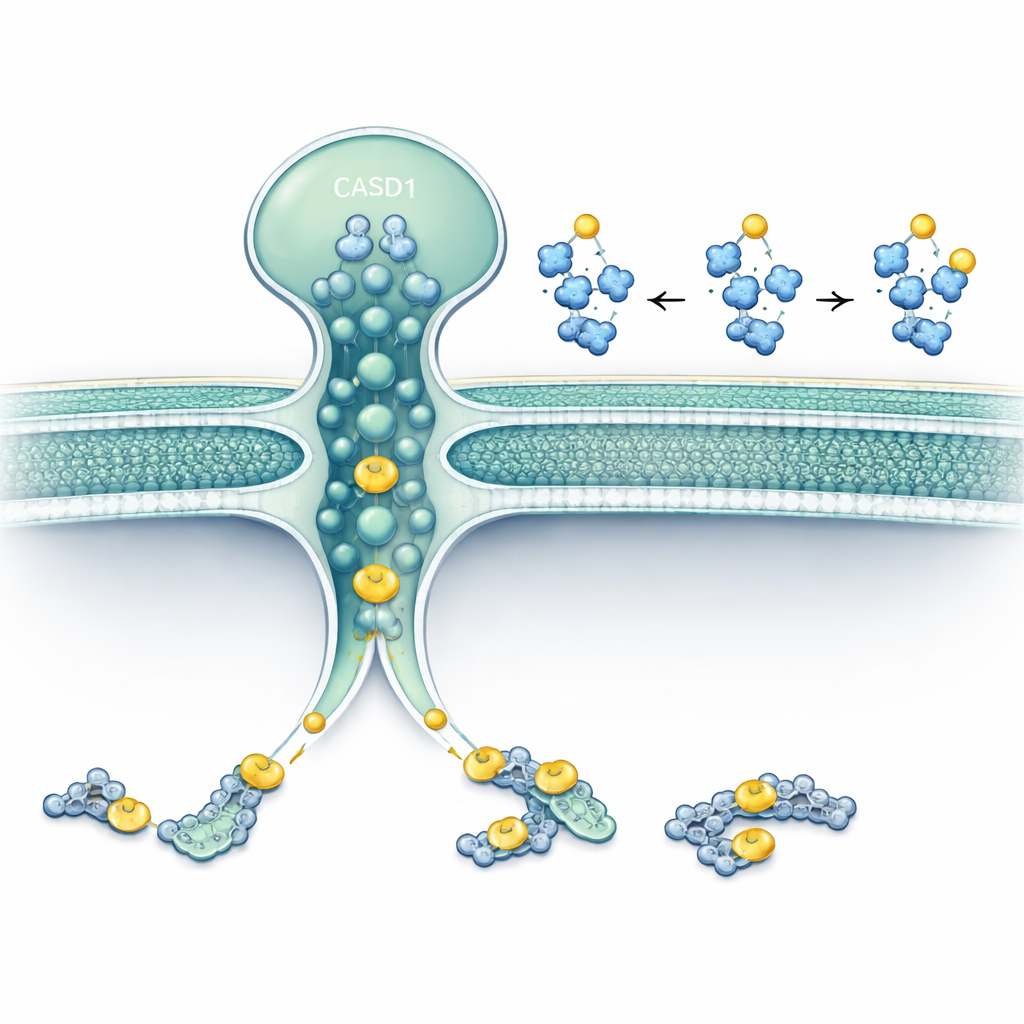
מוטציות של מטופלים מגלות רלוונטיות רפואית
SLC33A1 קשור בכמה מצבים נוירולוגיים נדירים, כולל הפרעה ילדותית חמורה (תסמונת הופקה–ברינדל), צורה של פרפלקסיה ספסטית תורשתית ואטקסיה צרברלית בעלת הופעה מאוחרת. הצוות שיחזר ארבע וריאנטים של SLC33A1 שמקורם במטופלים בתאים חסרי הנשא הנורמלי ובדק האם חלבונים משונים אלה יכלו להחזיר את אצטילציית הגאנגליוזידים. כל הארבעה הראו פונקציה מופחתת, וההפרעות הקשות בהופעה בילדות כמעט ולא שחזרו אצטילציה. בעזרת מבנה תלת־ממדי של SLC33A1 שפורסם לאחרונה, המחברים מיפו את המוטציות על פני החלבון והראו כיצד סביר שהן משבשות את הארכיטקטורה שלו או את יכולתו לקשור אצטיל‑CoA. זאת מציעה באופן חזק שאובדן אצטילציית גאנגליוזידים תורם לתסמינים הנוירולוגיים הנצפים במטופלים.
אתר פעיל שני חבוי ב‑CASD1
העבודה גם חשפה טוויסט בלתי צפוי: נראה כי CASD1 עצמו הוא אנזים דו‑תכליתי. הקטע המוכר שלו בלומן של הגולג׳י משתמש באצטיל‑CoA שנמסר על ידי SLC33A1. אך כאשר SLC33A1 הוסר, תאים עדיין הצליחו להניח קבוצת אצטיל אחת על חומצות סיאליות מסוימות בתנאים מסוימים, אם כי הם לא הצליחו להוסיף את קבוצת האצטיל השנייה הנחוצה לתבניות מורכבות יותר. באמצעות חיזוי מבני מתקדם וסימולציות מולקולריות הראו המחברים שחלק החודר ממברנה של CASD1 דומה במידה רבה לאצטילטרנספראז טרנסממברנלי ידוע מליזוזומים. הם זיהו חומצות אמינו מפתח באזור זה שקושרות אצטיל‑CoA בצד הציטוזולי ומעבירות את קבוצת האצטיל דרך הממברנה ישירות לחומצה סיאלית. כאשר שינו את שרשראות החומצות האלו, CASD1 איבד את הפעילות השנייה הן בניסויי מבחנה והן בתאים חיים.
שני מסלולים, קוד סוכרי מכוונן בעדינות
ביחד, הנתונים תומכים במודל של "שני אתרי קטליזה". מסלול אחד תלוי ב‑SLC33A1 שמכניס אצטיל‑CoA ללומן של הגולג׳י, שם הדומיין הלומינלי של CASD1 מוסיף קבוצת אצטיל לחומצה סיאלית, מה שמאפשר גם תבניות אצטילציה פשוטות וגם כפולות. המסלול השני משולב בליבת החודרת ממברנה של CASD1, שפונה ישירות אל אצטיל‑CoA הציטוזולי ויכול לבצע רמת אצטילציה בסיסית אפילו כשה‑SLC33A1 חסר. למבין הלא־מקצועי, משמעות הדבר היא שאנזים יחיד, המסופק משני מאגרים שונים של אצטיל, כותב "סימני פיסוק" עדינים על סוכרי פני התא. כאשר הנשא או כל חלק של האנזים תקולים, הסימנים הללו מונחים במקום הלא נכון או חסרים, דבר שעשוי לסייע להסביר מחלות נוירו־התפתחותיות ונוירודגנרטיביות מסוימות ומדגיש שכבת בקרה חדשה באופן שבו תאים מעצבים את זהותם החיצונית.
ציטוט: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
מילות מפתח: חומצה סיאלית, אצטילציה בגולג׳י, גאנגליוזידים, SLC33A1, CASD1