Clear Sky Science · he
הדינמיקה המבנית של מידנולין-פרוטאזום במהלך פירוק תת-מולקולות ללא יוביקוויטין
כך תאים משליכים את האשפה במהירות
בתוך כל תא, חלבונים מיוצרים ומתפוררים ללא הפסקה. רבים מסומנים במולקולות קטנות הנקראות יוביקוויטין לפני שהם נשלחים למכונת המיחזור המרכזית של התא — הפרוטאזום. אך חלק מהחלבונים הגרעיניים חייבים להיעלם במהירות כל כך גדולה שאין זמן לסימון. מחקר זה מגלה כיצד חלבון עזר מעט מוכר, מידנולין, מתחבר ישירות לפרוטאזום כדי לפנות את המטרות הדחופות האלה, ומספק רמזים לאופן שבו תאים שומרים על שליטה מהירה וקפדנית על פעילות הגנים.
קיצור דרך למטחנת התאים
הפרוטאזום 26S הוא קומפלקס בצורת חבית שמפרק חלבונים לחתיכות קטנות. באופן מסורתי הוא מזהה מטרות על ידי קריאת שרשראות יוביקוויטין המצורפות אליהן. עבודה עדכנית חשפה מסלול חלופי: נתיב "קיצור דרך" שבו מידנולין מלווה חלבונים גרעיניים מסוימים — ובעיקר תוצרי גנים מוקדמים מידיים שמדליקים וכבים גנים במהירות — ישר אל הפרוטאזום ללא תגי יוביקוויטין. חלבונים אלה, כגון גורמי שעתוק המעורבים בתגובות ללחץ ודלקת, חייבים להופיע ולהיעלם בתוך דקות. המאמר החדש משלב קריואלקטרון-מיקרוסקופיה ברזולוציה גבוהה עם ניסויים ביוכימיים כדי למפות, כמעט פריים אחר פריים, כיצד מידנולין נצמד לפרוטאזום וממקם את המטען שלו להריסה.
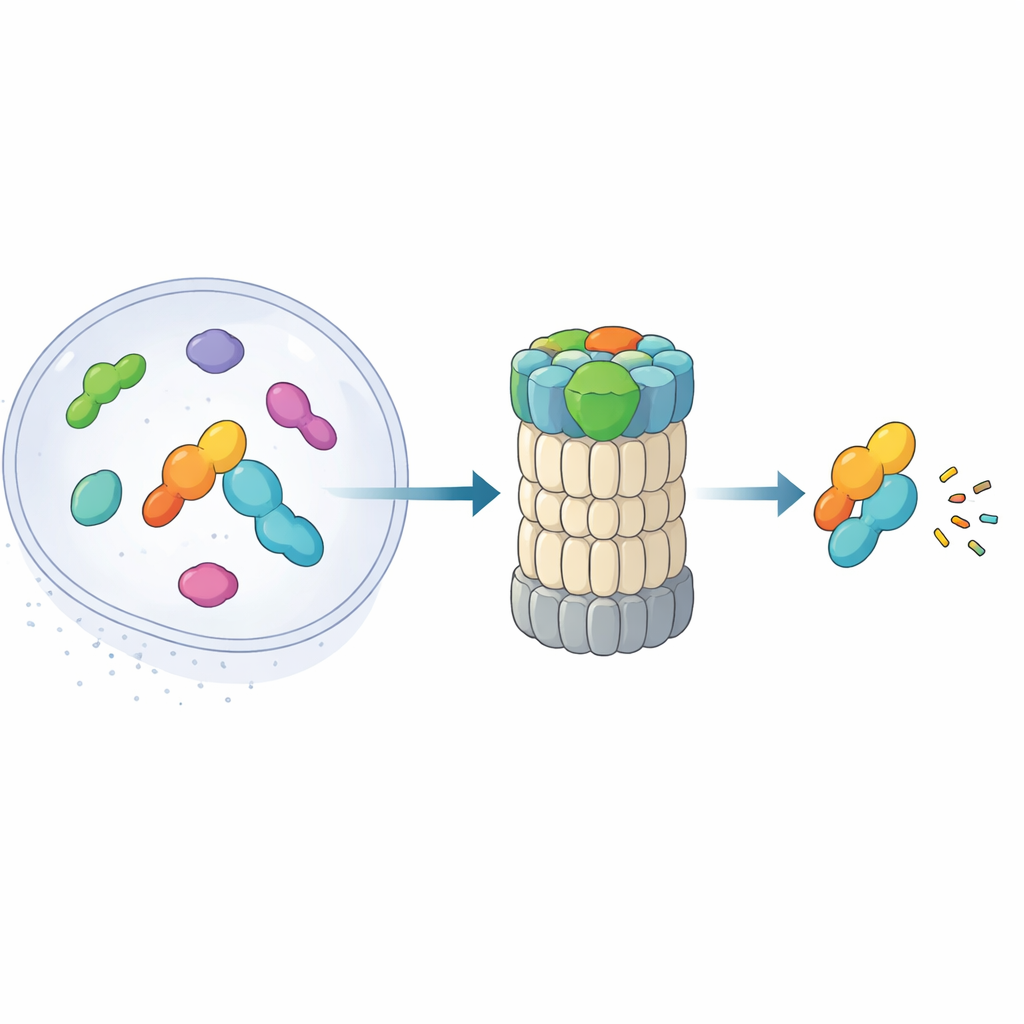
עזר בשלושה חלקים שמאחוז ומכוון מטרות
מידנולין פועל כמו כלי-רב תכליתי עם שלושה מודולים מרכזיים. קצה אחד, סליל C-טרמינלי, נכנס לאתר עגינה ברכיב הפרוטאזום שנקרא RPN1 ומעגן את מידנולין למכונת המיחזור. אזור אמצעי, ה"תפיסה" (Catch), מזהה ומאחז תכונה חוטית מסוימת (דגרון) בחלבוני המטרה. בקצה הנגדי נמצא תחום דמוי-יוביקוויטין. מפתיע שהתחום הזה אינו מיועד בעיקר לקישור לפרוטאזום, כפי שקורה בחלבוני נשיאה דומים. במקום זאת, המחברים מראים שהוא נח בחיבוק אל RPN11, אנזים שבמקרה רגיל מסיר יוביקוויטין ממטרות. כאן RPN11 מתפקד יותר כשלד: על-ידי אחיזת הקטע הדמוי-יוביקוויטין של מידנולין, הוא מסייע להחזיק את אזור ה-Catch ואת המטען שלו ישירות מעל נקב הכניסה הצר לפרוטאזום.
הכוונת החלבון אל הליבה הטוחנת
לאחר שמידנולין עוגן, המנוע הצורך אנרגיה של הפרוטאזום — טבעת AAA+ ATPase — נכנס לפעולה. טבעת זו יושבת ממש מתחת לפתח הכניסה ומשכה שרשראות חלבון לא מקופלות אל הליבה, צעד אחר צעד. הצילומי cryo-EM מגלים סדרת עמדות של "מדרגות ספירליות" שאימצו ששת תת-היחידות של המנוע כשהן מאחוזות ומעבירות את המצע דרך הערוץ המרכזי. המחברים לכדו ארבעה שלבים עוקבים של מחזור זה, כולם עם חומר קשור למידנולין המשורטט דרך הנקב, ואף ראו כיצד שחרור יון מגנזיום בתת-יחידה אחת מצטלב עם הזזה כלפי מטה של כל הטבעת. זה מעיד ששימוש מתואם ב-ATP ושחרור מגנזיום מסייעים ל"קרת" החלבון עמוק יותר לתוך התאים שבהם נמצאים אתרי החיתוך.
מדוע מיקום וביטוי משותף חשובים
הקבוצה בדקה כיצד כל מודול של מידנולין תורם ליעילות. סליל העגינה לבדו יכול לקשור RPN1 אך אינו מייעל באופן משמעותי את פעילות הפרוטאזום. הסרת אזור ה-Catch משאירה פרוטאזומים רבים תקועים במצב רדום, ללא מצע, אף על פי שמידנולין עדיין יכול להתחבר; החלפת ה-Catch במצע המחובר קבוע אף היא נכשלת בשחזור הפעילות המלאה. ממצאים אלה מצביעים ש-Catch עושה יותר מאשר אחיזה של המטרה — היא גם מייצבת את החלבון במדויק מול פתח הכניסה. נתונים ביוכימיים ונתוני רנ״א של גידולים מראים בנוסף שמידנולין נוטה להיות מיוצר יחד עם המצעים שלו. כאשר הם מבוטאים במשותף, מידנולין מתקפל טוב יותר ויוצר קומפלקסים יציבים, מה שיוצר חבילת "לפגוע בי" מוכנה שניתן למסור במהירות לפרוטאזום כאשר התא צריך לאפס את ביטוי הגנים.
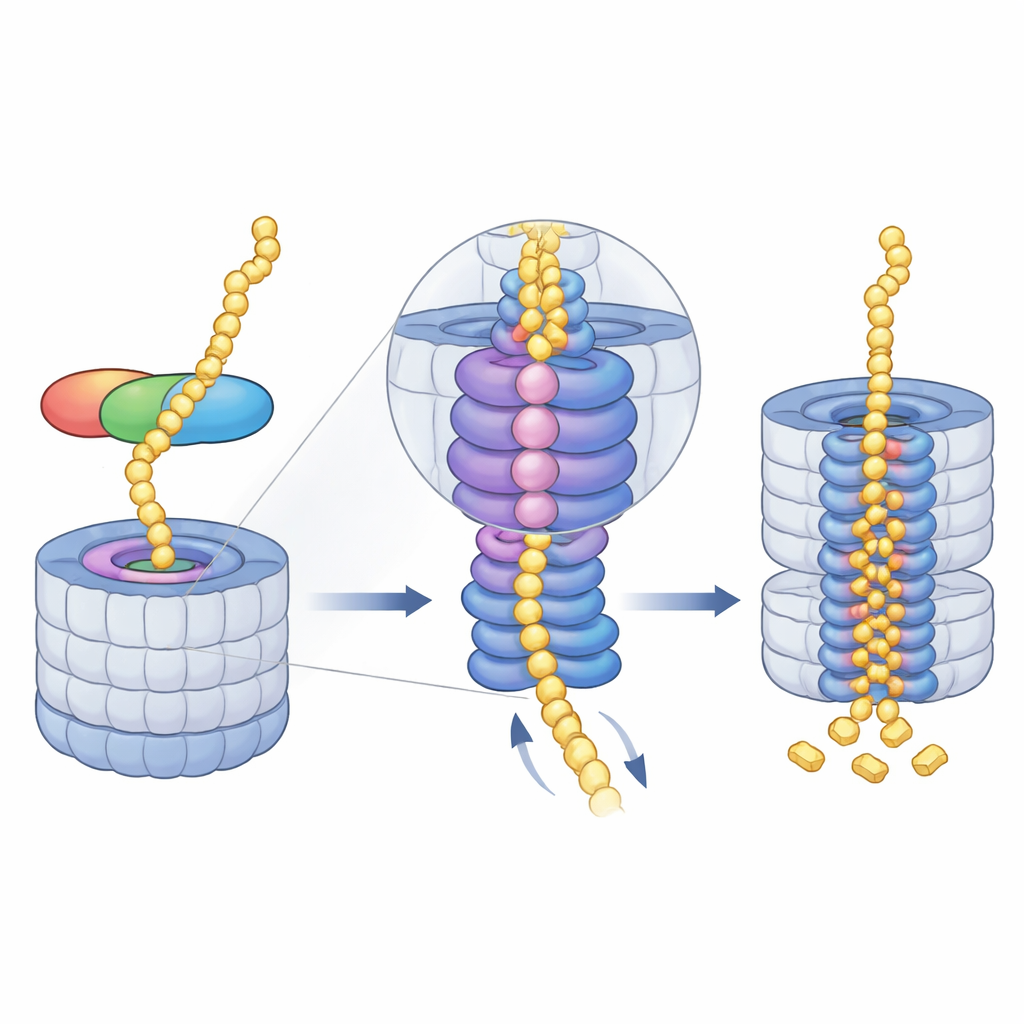
ניקוי עצמי ואפשרויות רפואיות עתידיות
לאחר שהחלבון המטרה נמשך ונחתך, מידנולין עצמו אינו מוחרג. האזורים הלא-מובנים שלו יכולים להישרטט לתוך המנוע ולהיזרק לאותה ליבת הרס, מה שמבטיח שהעזר לא ייערם ללא צורך. על ידי הבהרת הנתיב החופשי מיוביקוויטין אל הפרוטאזום, המחקר מרחיב את ההבנה שלנו כיצד תאים מנהלים את אורך החיים של חלבונים ביומדידות זמן קפדניות מאוד. הוא גם מרמז על אסטרטגיות תרפויטיות חדשות: בהנדסת מולקולות מבוססות מידנולין שיקשרו חלבונים גרעיניים גורמי מחלה ישירות אל הפרוטאזום, ייתכן שבעתיד ניתן יהיה לחסל מטרות "בלתי ניתנות לתרופות", כולל מכוונים סרטניים מסוימים, במהירות ובסלקטיביות רבה יותר.
ציטוט: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
מילות מפתח: פרוטאזום, מידנולין, פירוק חלבונים, נתיב בלתי תלוי ביוביקוויטין, גנים מוקדמים מידיים