Clear Sky Science · he
יכולת השעתוק מגדירה את הפוטנציאל הנוקלאציה של יחידות MSR מבודדות
מחליפים מוסתרים ב‑DNA שלנו
הגנומים שלנו דחוסים בתוך גרעין התא בשתי צורות עיקריות: אזורים פעילים שמכילים גנים, ומקטעים דחוסים מאוד שחשבו זמן רב כ"חומר חשוך" גנטי. המחקר שואל שאלה שנראית פשוטה אך מטעה: מה גורם לפיסת DNA להפוך לחומר דחוס זה — הידוע כהטרוכרומטין — מלכתחילה? באמצעות פירוק סוג מסוים של DNA חוזר בעכברים, המחברים מגלים שלא כל הרצפים החוזרים זהים: רק אלה המסוגלים לתמוך בסוג מיוחד של שעתוק יכולים להפוך את המתג שבונה ומתחזק את השכונות השקטות הללו של ה‑DNA.
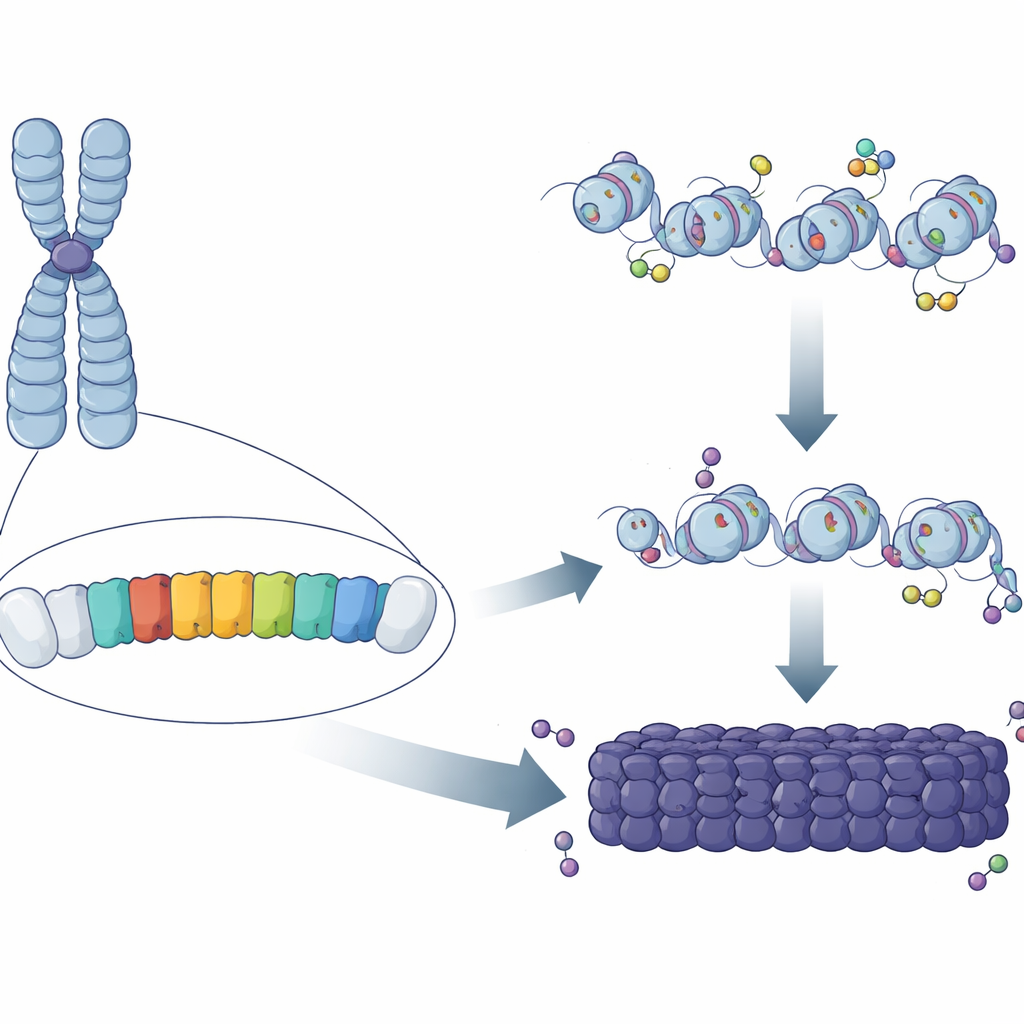
דפוסים חוזרים בגנום
כמעט חצי מה‑DNA של מאמלים מורכב מרצפים חוזרים, רבים מהם מרוכזים באזורי סביב מרכז הרבומוזום. בעכברים, מרכיב מרכזי של אזורים אלה הוא "חזרת הלוויין הראשית" (MSR), רצף קצר עשיר ב‑A/T המועתק מאות אלפי פעמים. עבודות קלאסיות הראו שאזורים אלה מצופים בסימנים כימיים וחלבונים שנועלים את ה‑DNA במצב דחוס ומגן. אך נותרה חידה מדוע עותקים מסוימים של MSR הפכו להטרוכרומטין מלאים בעוד אחרים, המפוזרים במקומות אחרים בגנום, לא עשו זאת. המחברים חשבו כי הבדלים קטנים ברצף או בהתנהגות של יחידות MSR בודדות עשויים לקבוע האם הן יכולות לשמש זרע, או "לנוקלאט", כתם של הטרוכרומטין.
בנייה של אתר מבחן בגנום
כדי לבדוק רעיון זה בצורה נקייה, הקבוצה הטביעה תאי גזע עובריים של עכבר להכיל מגרש נחיתה מלאכותי במקטע שקט של כרומוזום 2 — אזור ללא גנים או חזרות שכנות וללא פעילות ניתנת לזיהוי. לאתר הנייטרלי הזה הוכנסו קטעי DNA שונים: יחידות MSR שלמות, וריאנטים של MSR שבהם הרצף שונה באופן נרחב, ואלמנטים בקרה כגון מנגנוני קידוד ויראליים או מקטעים של אלמנטים ניידים. זה אפשר להם לשאול, יחידה אחרי יחידה, אילו רצפים מסוגלים למשוך את התכונות המאפיינות הטרוכרומטין: תווית כימית ספציפית על חלבוני ההיסטון (H3K9me3), קשירת חלבוני HP1, והטמעת ההיסטון מקשר H1 — שכולם יחד מעבים ומייצבים את הכרומטין המקומי.
רק חזרות "מוכנות לשעתוק" זורעות כרומטין שקט
הממצאים היו בררניים באופן מטלטל. יחידת MSR שלמה שהוכנסה לאתר הבדיקה לא הספיקה לשנות את הכרומטין. עם זאת, שלוש עותקים או יותר ברצף של רצף MSR שלם המירו את האזור הסובב לאי־הטרוכרומטין, עם רמות חזקות של H3K9me3, HP1 והיסטון H1. לעומת זאת, מקטעים זהים באורכם של רצפי MSR משובשים, או של סוג חזרה אחר (אזור לא מתורגם בקצה 5' של LINE-1), לא הצליחו לעשות זאת, אף על פי שיכלו להניע שעתוק חזק. ההבדל המרכזי היה שעותקי MSR מרובי־עותקים ותיקיים תמכו בשעתוק דו‑כיווני מתון שהפיק מולקולות RNA קצרות וא-אופן‑תקני שנשארו קשורות בצמוד לכרומטין. דפוס זה, ולא שעתוק גבוה בדומה לגנים, תאם את היכולת לנוקלאציה של הטרוכרומטין.
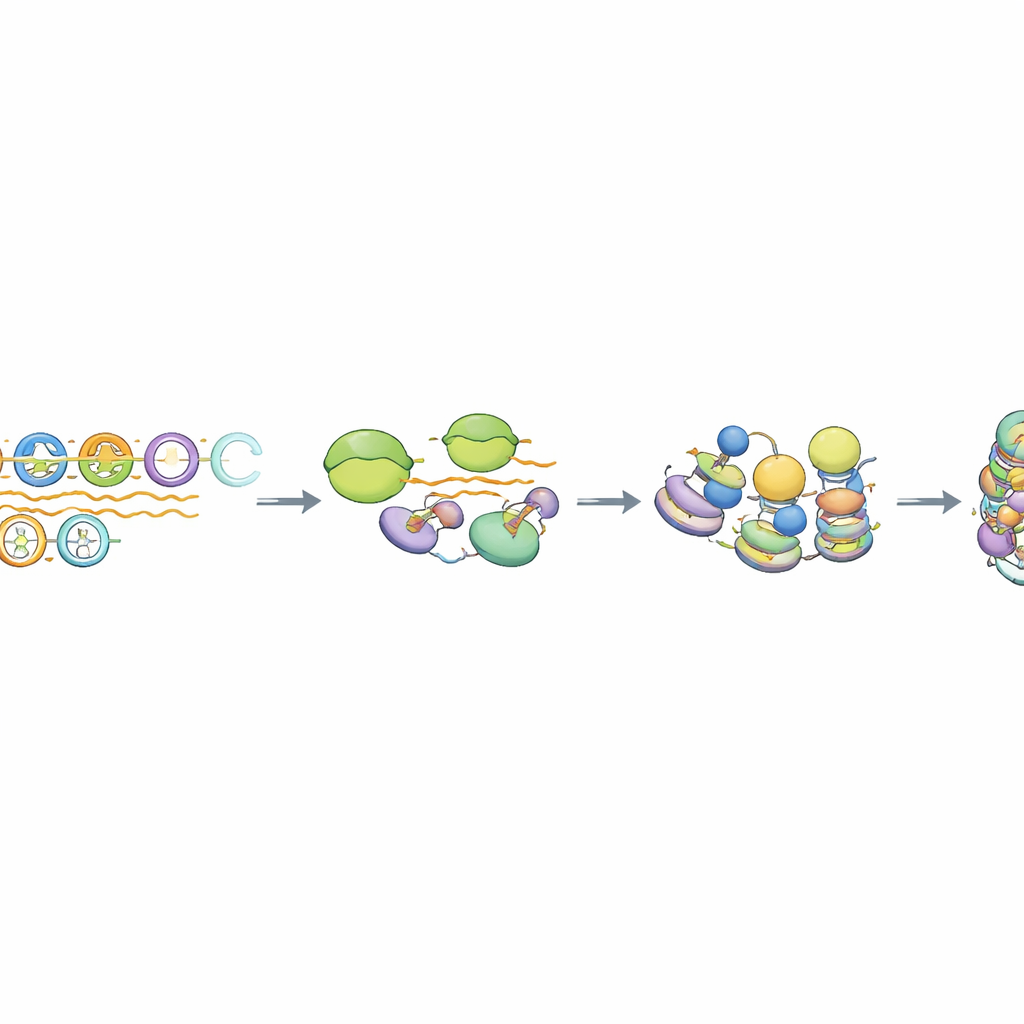
סוג מיוחד של שעתוק ועיבוד RNA
בבדיקה מעמיקה יותר, המחברים מצאו כי פולימראז RNA II, האנזים שמייצר בדרך כלל mRNA, נוטל חלק קצר בארסוני MSR אך אינו ממשיך ביעילות ליצירת תמלילים ארוכים. ה‑RNA המתקבלים חסרים סממנים טיפוסיים של mRNA כגון כובע 5' מגן וזנבות פוליאדניל ארוכים, והם נשארים קרובים ל‑DNA שמייצר אותם. מכונה חלבונית הנקראת קומפלקס Integrator, ידועה בתפקידיה בגזירה ובסיום של RNAים לא‑מקודדים, היה מועשר במיוחד ביחידות MSR שלמות. כאשר הפעילות החותכת של Integrator הופחתה, רמות ה‑RNA המקוריות מ‑MSR עלו באופן משמעותי, אך התווית הדכאנית על ההיסטון נשארה בעוד קשירת HP1 השתנתה בעדינות. ניתוח ברמת הגנום הראה שרק כ־10–15% מהעותקים השימוריים ביותר של MSR מתנהגים כך, מה שמבליט תת־קבוצה של חזרות "כשירות" המכוונות למסלול דיכוי המקושר לשעתוק זה.
DNA פרום כפילוח ממחזר פרומוטר
הצוות חקר גם כיצד DNA של MSR מעודד את השעתוק הבלתי שגרתי הזה. מערכי MSR מרובי־עותקים, אך לא עותק יחיד או זוגי, הראו סימנים ברורים של DNA פתוח מקומית והיברידים RNA:DNA, תצורות מבניות שנראות לעתים קרובות ליד פרומוטרים פעילים ובאתרי עצירה. תצורות אלה הורחבו כאשר עוכבו אנזימי טופואיזומראז, והן הצטלבו עם שעתוק מוגבר של MSR ותכונות הטרוכרומטין חזקה יותר. המחברים מציעים כי שלוש יחידות MSR או יותר ברצף יוצרות טופולוגיית DNA פיזיקלית המדמה פרומוטר, ומזמינה את הפולימראזות ופקטורי השעתוק להשתתף במידה מספקת ליצירת RNAים קצרים שביחד עם חלבונים ספציפיים מחזקים ארכיטקטורת כרומטין דחוסה.
מדוע זה חשוב לבריאות הגנום
לעין לא מומחית, עבודה זו מראה כי חלקים מה"DNA המיותר" שלנו פועלים כמחליפים מכוונים בקפידה, משתמשים בתערובת של צורת DNA, שעתוק ברמה נמוכה ועיבוד RNA כדי לבנות את המעטפת המגינה של הגנום. רק יחידות MSR היכולות לתמוך בשעתוק מבוקר זה, שאינו מייצר mRNA, יכולות להצית הטרוכרומטין חדש, בעוד רצפים משובשים או אלמנטים פעילים מדי אינם מסוגלים לכך. הלוגיקה המבוססת על DNA/RNA זו מסייעת להסביר כיצד תאים מבחינים בין אזורים שיש להחזיק בשקט לאלה שרשאים להכיל גנים, ולמה RNAים לווייניים שאינם מוסדרים כראוי קשורים לסרטן ולבעיות התפתחות. למעשה, המחקר מראה כי הרקע החוזר של הגנום אינו מילוי פסיבי אלא מהנדס פעיל של ארכיטקטורת הגרעין ויציבותו.
ציטוט: Lo, YH., Shukeir, N., Erikson, G. et al. Transcriptional competence defines the heterochromatin nucleating potential of isolated MSR units. Nat Commun 17, 2653 (2026). https://doi.org/10.1038/s41467-026-70991-2
מילות מפתח: הטרוכרומטין, DNA לווייני, RNA לא-מקודד, מבנה כרומטין, יציבות הגנום