Clear Sky Science · he
הטרוגניות מרחבית של MDSC שמתווכת על‑ידי איתות ANXA1‑FPRs מניעה דיכוי חיסוני בהתקדמות OSCC
מדוע המערכת החיסונית מתקשה מול סוגים מסוימים של סרטן הפה
סרטן אפיתליאלי של חלל הפה, צורה שכיחה של סרטן פה, לעתים קרובות מתנגד לטיפולים החיסוניים המבטיחים ביותר של היום — אלו שמשחררים את מנגנוני ההגנה של הגוף. המחקר הזה שואל שאלה בסיסית אך מכרעת: מדוע תאי חיסון רבי עוצמה, שאמורים לזהות ולהשמיד סרטן, נכשלו כל‑כך לעתים קרובות בגידולים אלה? על‑ידי מיפוי המיקום של תאים שונים בתוך הגידול ואופי התקשורת ביניהם, החוקרים חושפים משחק חתול‑ורקול משתנה בין תאי הסרטן, תאי מדכא ו‑T קטלניים שמסייע להסביר כישלון טיפולים — ומציע דרך לתקנו. 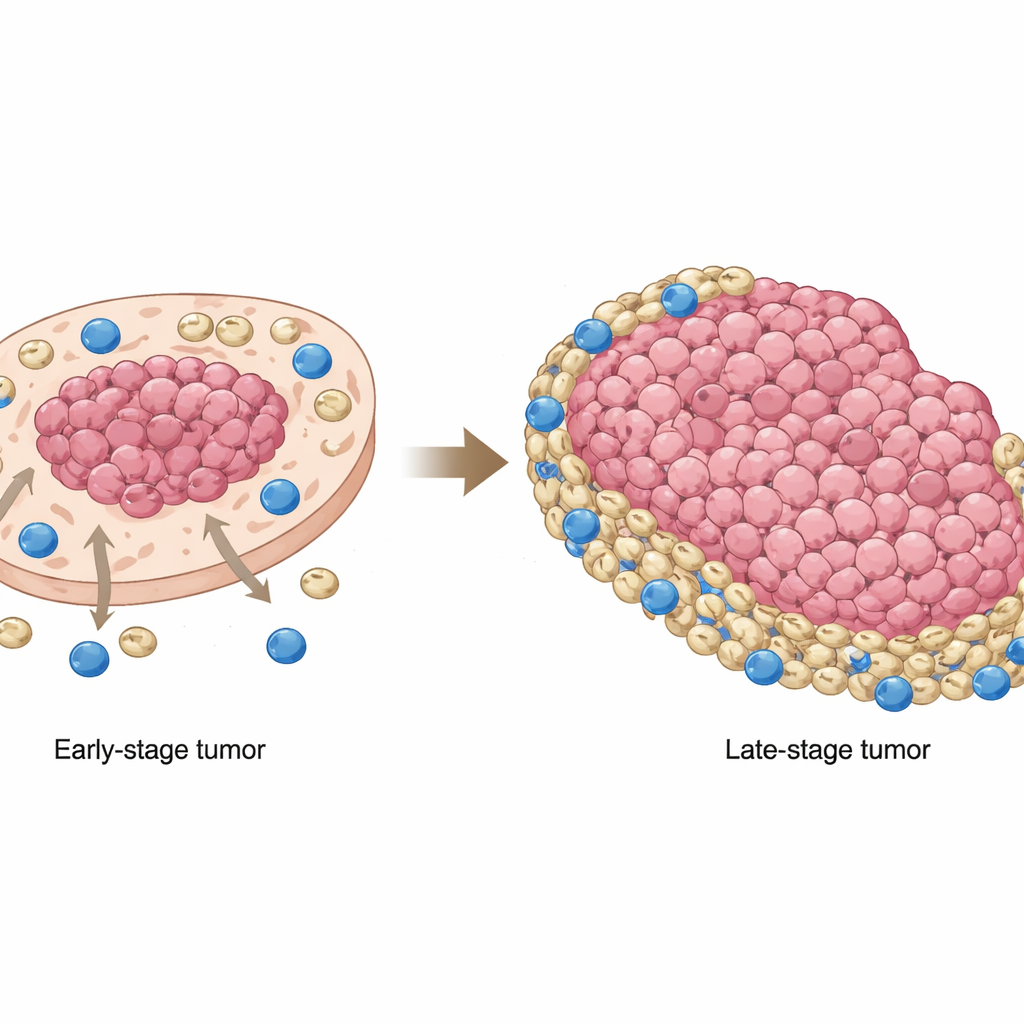
נוף נסתר בתוך הגידול
המחברים שילבו שתי גישות חדישות: ריצוף RNA של תא יחיד, שקורא את פעילותם של תאים בודדים, וטרנסקריפטומיקה מרחבית, המראה היכן התאים האלה ממוקמים בפרוסות רקמה של הגידול. בניתוח גידולים ממטופלים בשלבים מוקדמים ומתקדמים של סרטן הפה, הם זיהו את השחקנים העיקריים: תאי אפיתל סרטניים, תאי CD8 "קטלניים", תאי T ו‑B נוספים, פיברובלסטים שמספקים תמיכה מבנית, ותאים חיסוניים מיוחדים הנקראים תאי מדכאים נגזרים ממיויד (MDSCs). בעוד שבתהליכי המחלה המוקדמים נמצאו יותר תאי CD8 פעילים, בגידולים בשלב מאוחר אותרה איתות T חלש יותר ואותות מדכאים חזקים יותר מהמיוֹידיים, מה שמצביע על סביבה שהולכת והופכת עוינת יותר לחיסון נגד הסרטן.
תאי מדכא בתנועה
אחד הממצאים הבולטים היה כיצד מיקומם של MDSC השתנה ככל שהגידול התקדם. בגידולים בשלב מוקדם, תאים מדכאים אלה נטו להצטבר באזורים עשירים בתאי גידול, קרוב לגרעין הסרטני. בשלבים מאוחרים הם זזו החוצה, והצטברו באזורים דלים בגידול ובשוליים, היכן שתאי CD8 היו שכיחים יותר. משמעות הדבר היא שבגידולים מתקדמים תאי הקטלניים נדחקו ברובם לקצוות ואז נתקלו בחגורת MDSC שהחלישה את יכולתם לתקוף תאי סרטן. דגימות מחולים ומודלים בעכברים איששו שמעבר זה לא היה רק סקרנות מדעית: כאשר הימצאות ה‑MDSC חפפה פחות עם תאי הסרטן ובמקום זאת התמקמה באזורים שאינם‑גידוליים, להישרדות הכללית של החולים היה חיזוי גרוע יותר. 
מתג איתות בין תאי הסרטן לתאי המדכא
המחקר ביקר בתקשורת מולקולרית בין תאי הסרטן ל‑MDSC הכוללת חלבון בשם אנקסין A1 (ANXA1) על תאי הגידול ומשפחת קולטים הנקראת FPRs על תאים מיוידיים. במחלה המוקדמת, ANXA1 על תאי הסרטן קושר בעוצמה את FPR1 ו‑FPR3, במיוחד על MDSC ומקרופאגים קשורים לגידול, וסייע לגייס ולשמר תאים מדכאים אלו בגרעין הגידול. ככל שהסרטן התקדם, רמות ה‑ANXA1 בתאי הגידול ירדו, מה שהחליש את הקשרים המקוריים האלה. במקביל, יותר MDSC החלו לבטא את הקולטן FPR2, והאיתות ANXA1–FPR2 צמח כציר מפצה לשמירה על מעורבות ה‑MDSC. תת‑קבוצה ספציפית של תאי גידול עם רמות גבוהות של ANXA1, שהראתה גם מאפייני דמיון‑גזע, נראתה כ"פיתיון" שמושך אליה MDSC בשלב מוקדם; כש־ANXA1 ירד, MDSC כבר לא הורעפו בגרעין אלא זזו לאזורים עשירים בתאי CD8.
כיבוי המגן כדי לסייע לאימונותרפיה לפעול
כדי לבדוק האם שבירת תקשורת זו יכולה לשפר טיפול, החוקרים השתמשו במודל עכבר של סרטן פה וחסמו את FPR2 בעזרת מעכב מולקולרי קטן בשם WRW4. לבדו, עיכוב FPR2 הפחית את נוכחות ה‑MDSC והגביר את תאי CD8 בסביבת הגידול אך לא האט דיו את גדילת הגידול. באותה מידה, טיפול בנוגדן נגד PD‑1 לבדו הניב תועלות מתונות, כיוון ש‑MDSC עדיין יצרו מחסום מדכא. כששני התרופות שויכו יחד, עם זאת, גדילת הגידול הוגבלה בחוזקה והעכברים חיו יותר זמן. בבעלי החיים הללו, החדירה של MDSC צנחה באופן חד בעוד שתאי CD8 חדרו עמוק יותר לאזורים עשירים בתאי הגידול, מה שמרמז שחסימת FPR2 מסירה מגן מרכזי שמגן בדרך כלל על תאי הסרטן מפני התקפה חיסונית.
מה משמעות הדבר לטיפול בסרטן בעתיד
לסיכום, העבודה מראה שלא רק סוגי התאים אלא גם הסידור המרחבי שלהם ושותפויות האיתות קובעות אם אימונותרפיה תצליח בסרטן הפה. ככל שהגידול מתקדם, MDSC נודדים מהמרכז אל השוליים, שם הם חוסמים את תאי הקטלניים, ואיתות ANXA1–FPR2 תורם לשימור הסידור המדכא הזה. על‑ידי שיבוש מסלול זה — במיוחד בשילוב עם תרופות צ'ק‑פוינט קיימות — ייתכן שרופאים יוכלו לתכנת מחדש את סביבת הגידול כך שתאי החיסון של הגוף יוכלו שוב לזהות ולהשמיד את הסרטן. זה מציע אסטרטגיה קונקרטית: שילוב חוסמי FPR2 עם אימונותרפיה עשוי לשפר תוצאות עבור מטופלים שסרטני הפה שלהם עמידים כיום לטיפולים הטובים ביותר הקיימים.
ציטוט: Li, F., Han, Y., Ou, F. et al. Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression. Nat Commun 17, 2535 (2026). https://doi.org/10.1038/s41467-026-70861-x
מילות מפתח: סרטן אפיתליאלי של חלל הפה, מיקרו‑סביבת הגידול, תאי מדכאים נגזרים ממיויד, טרנסקריפטומיקה מרחבית, אימונותרפיה בסרטן