Clear Sky Science · he
קולטני מכניקה מלאכותיים מבוססי אפטמרים מאפשרים חישה כוחית ספציפית לתא ושליטה זמנית באמצעות מעגלי DNA
הקשבה לתאים באמצעות משיכות עדינות
גופנו מלא תאים שממשיכים לדחוף ולמשוך את סביבתם, משתמשים בכוחות זעירים כדי להכריע מתי לגדול, לזוז או להשתנות. המחקר הזה מתאר שיטה חדשה להאזנה לכוחות אלה באמצעות התקנים מבוססי DNA שניתן לכוונן לסוגי תאים ספציפיים ולהפעיל או לכבות אותם לאורך זמן. טכנולוגיה כזו עשויה באחת מהשיטות לסייע למהנדסים לכוון גדילת רקמות, להבין את התנהגות הגידולים או לעצב חומרים חכמים שמגיבים לתאים חיים בזמן אמת.
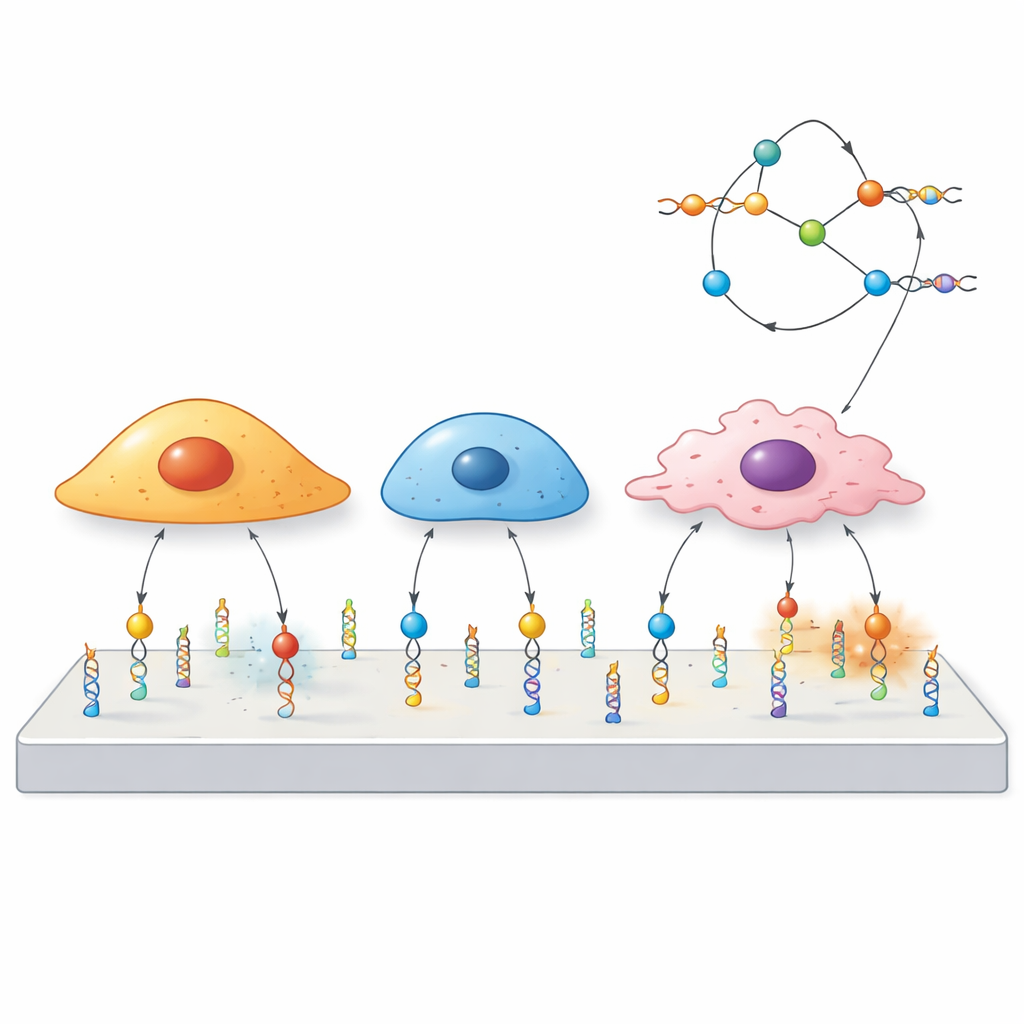
שימוש ב-DNA כמתג מכני זעיר
החוקרים בנו "מכנופרובים" מ-DNA, אותו מולקולה שנושאת מידע גנטי. כל פרוב מורכב משלושה חלקים: רצף DNA קצר הנקרא אפטמר שמדביק לחלבון נבחר על פני התא, מקטע DNA מזוגג שמשמש כקפיץ המכוון להיפרד בכוח מסוים, וצבע זוהר שמתנגן כשהקפיץ נפתח. כשאדם התא מושך בחוזקה על הקולטן שאליו נקשר האפטמר, הדופלקס של ה-DNA נפתח והאות נדלק. מאחר שאפטמרים שונים נקשרים לקולטנים שונים, הצוות יכול להחליט מראש אילו תאים או חלבונים יוכלו להפעיל את הפרוב.
גילוי מסלולי כוח חבויים על פני התא
מרבית חיישני הכוח הקיימים מתמקדים באינטגרינים, חלבונים מוכרים שמסייעים לתאים לאחוז בסביבתם אך נמצאים ברוב סוגי התאים, מה שמגביל סלקטיביות. כאן הצוות במקום זאת כיוון ל"קולטנים לא-קנוניים" שלא בהכרח נחשבים למכניים. הם הראו שאפטמר בשם AS1411, שקושר חלבון בשם נוקלאולין הנמצא בשפע בתאי סרטן, הפיק אות רק כאשר הוא זיהה במדויק את המטרה שלו. על ידי עיצוב פרובים שדרשו כוחות חלשים או חזקים יותר לפתיחה, הם גילו שנוקלאולין מעביר כוחות מתונים יחסית לאינטגרינים ואיננו כשלעצמו מסייע לפריסת התא על משטח. לעומת זאת, אפטמר אחר, Sgc8, שמזהה את הקולטן PTK7, הצליח לדווח על כוחות גם כאשר התאים כמעט ולא נדבקו, ויצר תבניות טבעתיות שהצביעו על מקור תנועה שונה.
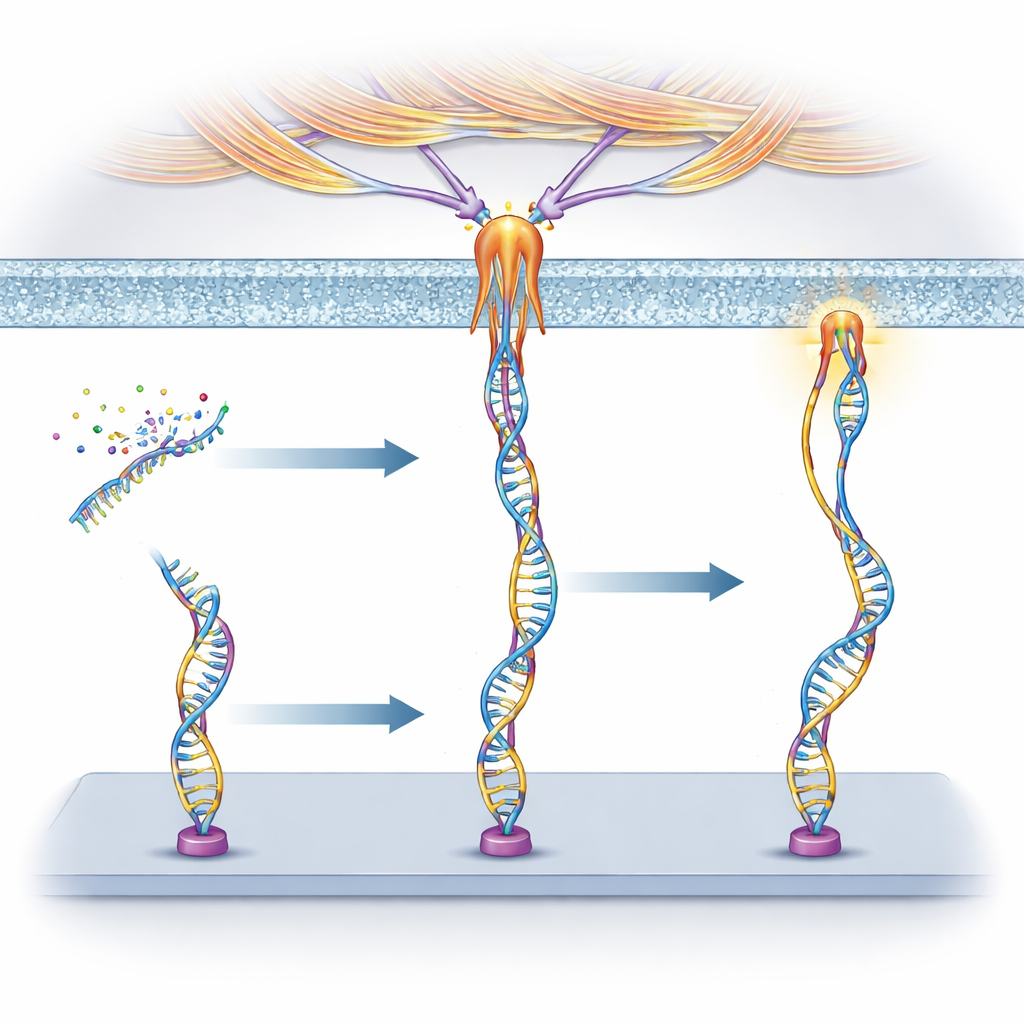
מעקב אחר מקור הכוחות
כדי להבין מה מושך את ההתקנים הללו, השתמשו החוקרים בתרופות שחוסמות באופן סלקטיבי תהליכים תאיים שונים. עבור נוקלאולין, הם מצאו שכוחותיו תלוים בחוזקה במיוזין, חלבון המנוע שמסייע להתכווצות שרירים, והופיעו באתרי אחיזה מוקדיים—נקודות מגע מיוחדות המשמשות לאחיזה ותחושת קשיחות. ממצא זה מרמז שנוקלאולין מקושר בעקיפין למכונת האקטין–מיוזין הפנימית של התא ויכול לשתף בכוחות החוזרים שלה. עבור PTK7, לעומת זאת, חסימת תהליך שנקרא מקרופינוציטוזה—אשר בתוכו התא ממרוט את ממברנתו ובלוע נוזל—הפחיתה משמעותית את האותות. הכוחות נבעו בעיקר מריפוד מוקדם של הממברנה המונע על ידי גדילת האקטין, ולא משלביו המאוחרים של איטום הוגולות, וכך נחשף מסלול מכני מובחן.
כוונון סלקטיביות התאים בדיוק מולקולרי
מפני שכל אפטמר מזהה קולטן משטח מסוים, אותו שלד DNA ניתן לתכנת מחדש בפשטות על ידי החלפת אפטמר אחד באחר. הצוות הדגים זאת עם פרובים לשלוש מטרות שונות—PTK7, mucin-1 ו-EpCAM—על פני לוח של שורות תאים סרטניות עם רמות גבוהות או נמוכות של כל חלבון. תאים עשירים בקולטן מסוים הפיקו אותות חזקים, בעוד אלה בעלי מעט קולטן כמעט ולא הגיבו, גם כשהם מעורבבים יחד באותו מעטפת. באופן בולט, תאים ששיתפו את אותו קולטן יכלו עדיין להציג דפוסי כוח מרחביים שונים, מה שמדגיש שזרימת הכוח דרך קולטן תלויה לא רק בנוכחותו אלא גם בחיווט הפנימי של כל סוג תא.
תכנות מתי מותר לתאים למשוך
בהתבסס על העובדה שאפטמרים הם מולקולות DNA, קשרו החוקרים את הפרובים שלהם לרשתות תגובה של DNA שולטות האם האפטמר יכול להתחבר כלל. גדילים משלימים "חוסמים" יכולים להסתיר זמנית את האפטמר, וגדילי "מפעיל" יכולים אחר כך להסיר את החוסמים באמצעות תגובת החלפת גדיל, ולהחזיר את הרגישות לכוח. הם גם תכננו חוסם מבוסס RNA שניתן לחתוך על ידי האנזים RNase H, ועיכבו חיתוך זה בעזרת מולקולות דמוי-פיתיון שמתחרות על האנזים. בכך הפכו את חיישנות המכאניקה לתוכנית מתוזמנת: תאים יכלו להפיק אותות רק אחרי עיכוב מובנה או בתוך חלונות זמן נבחרים.
מדוע הדבר משנה עבור חומרים חיים עתידיים
במונחים יומיומיים, עבודה זו הופכת את ה-DNA למנעול מכני חכם שנפתח רק עבור תאים מסוימים, רק תחת כוחות מסוימים ובזמנים נבחרים. על ידי גילוי כי קולטנים פחות בולטים כמו נוקלאולין ו-PTK7 יכולים לשאת מידע מכני דרך נתיבים שונים בתוך התא, היא מרחיבה את תמונתנו כיצד תאים "מרגישים" את סביבתם. מאחר שהמערכת כולה בנויה מחומצות גרעין, היא יכולה להתחבר ישירות לאפשרויות המתפתחות במהירות של מעגלי DNA וננו-מכשירים. זה יוצר בסיס לחומרים ורקמות מהונדסים שלא רק חשים מתי תאים דוחפים או מושכים, אלא גם מגיבים בפעולות ביוכימיות מתוזמנות בקפידה, ובפוטנציאל יכול לכוון ריפוי, גדילה או טיפול בסרטן בצורה ניתנת לתכנות גבוהה.
ציטוט: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
מילות מפתח: מכנוטרנסדוקציה, אפטמרי DNA, מכניקת תאים, ביולוגיה סינתטית, רשתות תגובה של DNA