Clear Sky Science · he
הידרופוביות וקשיחות פני השטח קובעות את הכתר החלבוני על ננו-חלקיקים שניתנים דרך הפה לטיפול בקוליטיס
להפוך כדורים לטיפולים חכמים יותר
אנשים החולים במחלות מעי דלקתיות כמו קוליטיס לעתים נוטלים תרופות אנטי-דלקתיות עוצמתיות, אך חלק גדול מהמינון מבוזבז או גורם לתופעות לוואי באיברים אחרים. המחקר בוחן גישה חדשה שמאפשרת לתרופות הניתנות דרך הפה לפעול בדומה לטילים מנועים: על ידי עיצוב חלקיקים נשאים זעירים שימשכו חלבונים מהמעי עצמו כדי לשמש כמערכת מיקוד טבעית, וכך לסייע לתרופות למצוא את תאי החיסון המובילים את הדלקת במעי.
איך המעי מלביש ננו-חלקיקים
כאשר כל ננו-חלקיק נכנס לגוף, הוא מצופה במהירות בשכבת חלבונים דקה, מה שמכונה מדענים "כתר חלבוני". במעי החולה הכתר הזה שונה מאוד מזה שנוצר ברקמה בריאה, משום שתמהיל החלבונים המקומי משתנה. המחברים מצאו קודם לכן שקוליטיס יוצר כתר ייחודי במעי שמטה במידה חלקיקים כלפי תאים חיסוניים הנקראים מאקרופאג׳ים, שמזינים ומווסתים דלקת. כאן הם שואפים לעצב במכוון את הכתר על ידי התאמת שתי תכונות בסיסיות של נשאי התרופה — דחיית המים (הידרופוביות) והקשיחות (נוקשות) — כדי להפוך אפקט חלש שנוצר על ידי המחלה לאסטרטגיית מיקוד חזקה.
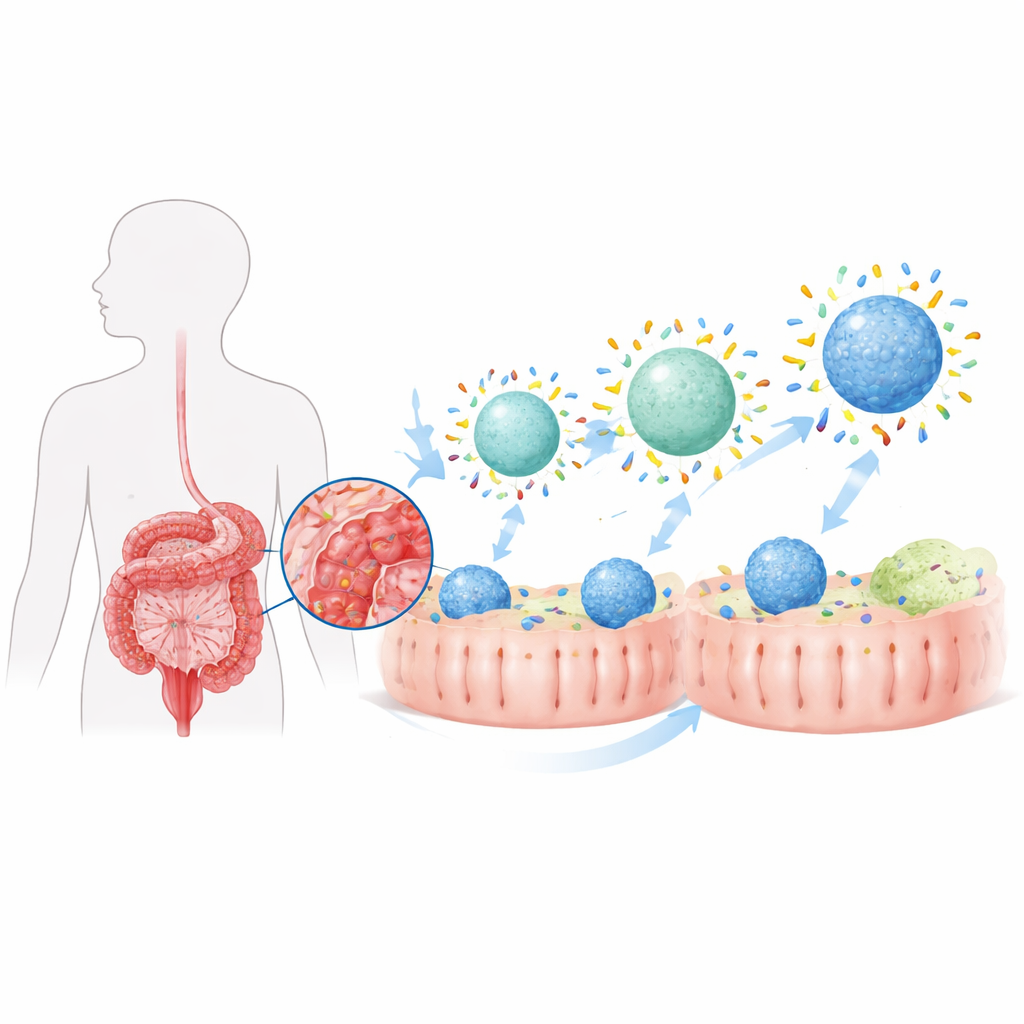
להפוך חלקיקים למושכים יותר לחלבונים
הקבוצה בנתה ננו-חלקיקים מבוססי ליפידים הדומים לבועות שומן זעירות וכיוונה עד כמה משטחיהם אוהבי-מים או שונאי-מים על ידי הוספת כמויות משתנות של ציפוי פולימרי שכיח. חלקיקים עם משטחים יותר הידרופוביים קישרו הרבה יותר חלבונים מעיים כאשר הוצפו בנוזלי קוליטיס, הן בבעלי חיים והן בצינורות מבחנה. כאשר חלקיקים "פוביים" אלה הוטענו בסטרואיד בודזוניד וניתנו דרך הפה לעכברים עם קוליטיס, הם מסרו הרבה יותר תרופה למאקרופאג׳ים במעי הגס לעומת גרסאות יותר הידרופיליות. כתוצאה מכך, בעלי החיים המטופלים החזירו יותר משקל גוף, ונוצר פחות קיצור ושל נזק של המעי הגס, בנוסף לרמות נמוכות יותר של מולקולות דלקת במעי. עם זאת, למרות שיפור בדלקת, המצב לא שב במלואו למצב בריא, מה שמרמז שהגדלת כמות חלבון הכתר לבדה לא הספיקה.
הקשחת החלקיקים לבחירת שותפים טובים יותר
כדי לדחוף את הרעיון עוד יותר, החוקרים שמרו על משטחים הידרופוביים אך שינו את המבנה הפנימי כדי להפוך חלקיקים לרכים, בינוניים או קשיחים על ידי מילוי הליבות שלהם בכדורי פלסטיק בגדלים שונים. כל השלוש עדיין צברו כמויות כוללות דומות של חלבון מעי, אך תמהיל החלבונים השתנה. החלקיקים הקשיחים ביותר יצרו כתרים עשירים במיוחד בחלבונים שיכולים להיקשר לקולטנים על מאקרופאג׳ים או לשאת מזון קטן שתאים אלה סופגים. חלבון כזה, S100A8, שפע במעיים מדוללים ויכול להפעיל קולטנים מסוימים של מאקרופאג׳ים. חסימת S100A8 על הכתר הפחיתה באופן חד את קליטת החלקיקים הקשיחים על ידי מאקרופאג׳ים, מה שחשף אותו כמרכיב מיקוד מפתח שנבחר על-ידי קשיחות החלקיק.
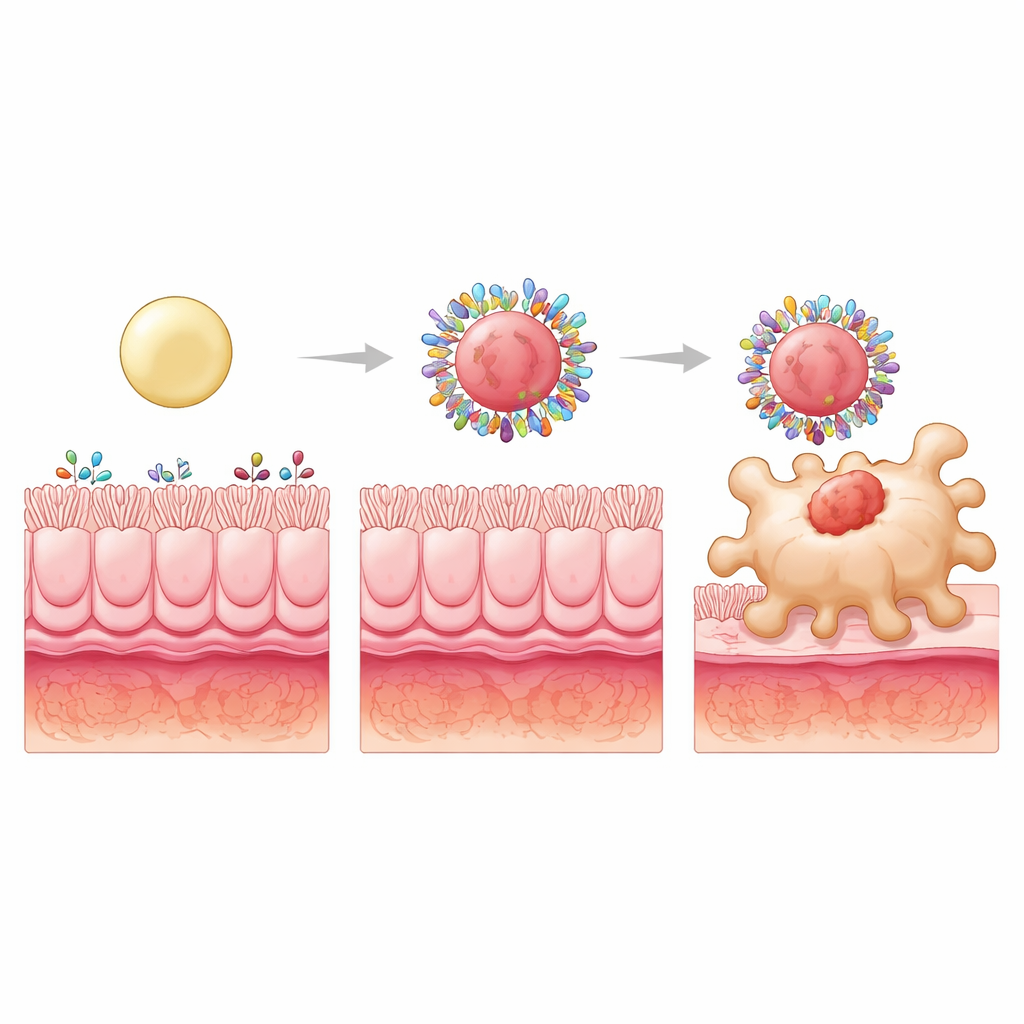
ממיקוד טוב יותר לריפוי טוב יותר
כאשר בודזוניד נארז בתוך חלקיקים בעלי הידרופוביות וקשיחות גבוהות וניתן דרך הפה לעכברים עם קוליטיס, התועלות היו מרשימות. הנוסחה הקשיחה לא רק צמצמה נזק חוטי ומתח חמצוני במעי, אלא גם נירמלה מספר אותות דלקתיים לרמות הנצפות בחיות בריאות. היא השיבה איזון בריא יותר בין סוגי מאקרופאג׳ "תוקפים" ו"מרגיעים" והגבירה תאים T רגולטוריים, המסייעים לשלוט בתגובות החיסוניות. חשוב לציין שהשיפורים הללו התבססו על סביבת החלבונים המשתנה במחלה בקוליטיס; אותו עיצוב לא הראה מיקוד מיוחד בעכברים בריאים, מה שמדגיש שהכתר הוא בעלות דינמי ותלוי במחלה.
מדוע זה חשוב לתרופות עתידיות
העבודה מראה שאפשר לכוון את חלבוני הגוף לפעול כמ"תויות" חכמות המתחדשות על נשאי תרופות דרך הפה פשוט על-ידי כוונון תכונות המשטח והמכניות של הנשאים. על ידי הגברת לכידת החלבון באמצעות משטחים הידרופוביים ואז שימוש בקשיחות להעדפת חלבונים המוליכים למאקרופאג׳ים כמו S100A8, החוקרים יצרו ננו-חלקיקים שמחפשים באופן טבעי את תאי החיסון שמניעים את הקוליטיס ומספקים תרפיה היכן שהיא דרושה ביותר. אותה לוגיקת עיצוב — מניפולציה של התחושה וההתנהגות של חלקיקים על פני שטח המעי — ניתנת להתאמה לצורות רבות של ננו-רפואה ומחלות, ומציעה נתיב עדין חדש למיקוד טיפולי ללא הוספת מולקולות מיקוד מלאכותיות.
ציטוט: Wu, J., Ni, M., Xing, L. et al. Surface hydrophobicity and rigidity determines protein corona on orally delivered nanoparticles treating colitis. Nat Commun 17, 2497 (2026). https://doi.org/10.1038/s41467-026-70453-9
מילות מפתח: העברת תרופות בננו-חלקיקים, דלקתיות של מעי, כתר חלבוני, ננו-רפואה דרך הפה, מיקוד בתאי מאקרופאג׳