Clear Sky Science · he
אטלס אינטראקציות ברמת הגנוס על פני אורטופלביווירוסים מזהה תפקיד משומר ל-UFMylation בשכפול אורתופלביווירוס
מדוע המחקר הזה על וירוסים חשוב
וירוסים כמו דנגי, זיקה ווסט ניל מתפשטים לאזורים חדשים ויכולים לגרום לכל דבר מחום ועד זיהומים מוחיים ומומים מולדים. עם זאת, עדיין חסרים טיפולים רחבי־היקף ואמינים. מחקר זה בוחן כיצד שותפות חבויה בין וירוסים אלה לבין מערכת תגיות תאית מעט ידועה בשם UFMylation מסייעת לפתוגנים להתחלק. על ידי מיפוי הקשר הזה על פני מספר וירוסים קרובים, החוקרים חושפים נקודת תורפה משותפת שעשויה להיות מנוצלת לפיתוח תרופות אנטי־ויראליות עתידיות.
בעקבות פנימי ויראלי מפתח
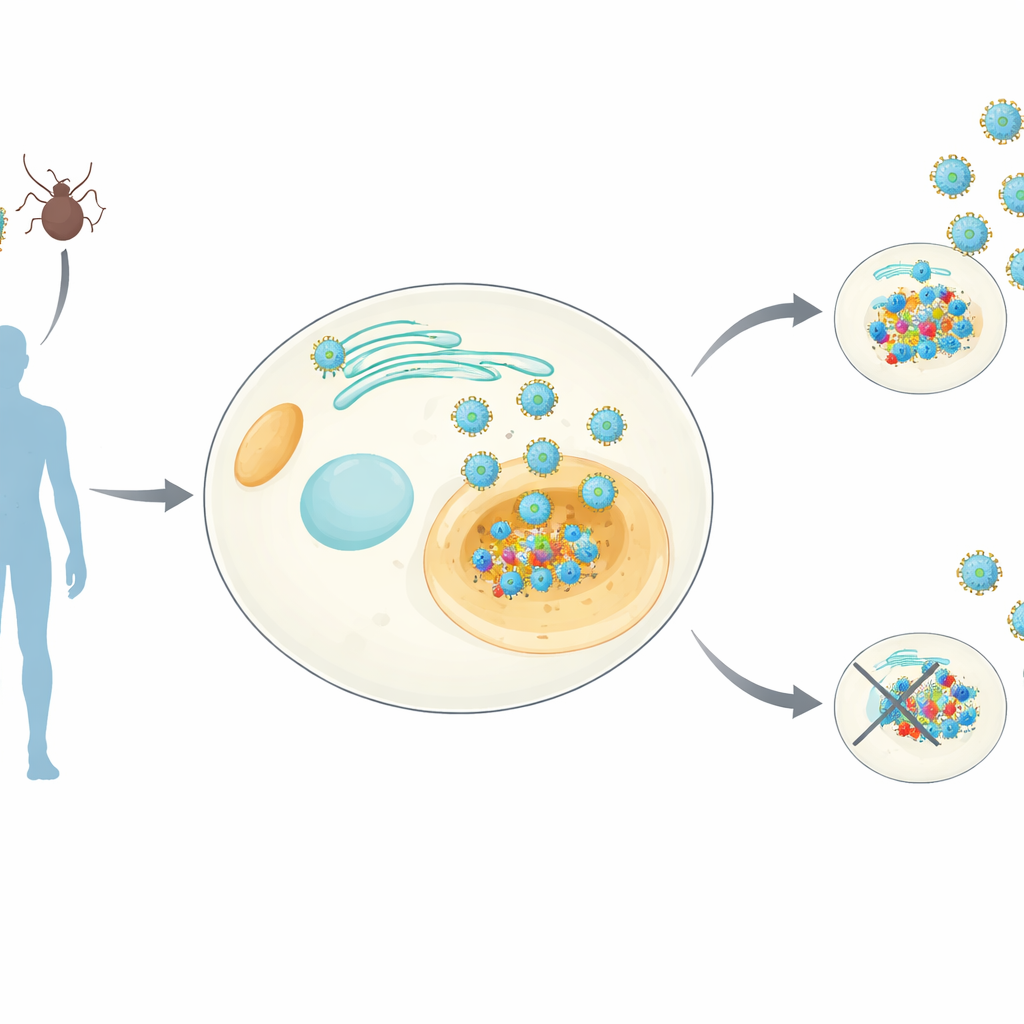
אורתופלביווירוסים – הקבוצה שכוללת את דנגי, זיקה, קדחת צהובה ואחרים – נושאים חלבון זעיר בשם NS4B שנצמד לממברנות בתוך התאים שלנו. ידוע כי NS4B חיוני לשכפול הוירוס, אך תפקידיו המדויקים נותרו טמירים. החוקרים יצרו קווי תאים אנושיים שמייצרים באופן יציב את NS4B משמונה אורטופלביווירוסים שונים. הם השתמשו בטכניקות ספקטרומטריה מסה רגישות כדי למשוך מטה את NS4B יחד עם חלבוני אדם שבא לידי הדבקות בו, ובמקביל מדדו כיצד הבעתו של NS4B משנה את התמהיל הכולל של חלבונים בתא. כך נוצר "אטלס אינטראקציות" ברמת הגנוס – אותם הם קוראים NS4Bome – שמציג גם מטרות מארח משותפות וגם כאלה הספציפיות לוירוס.
טריקים משותפים ופתרונות מותאמים
האטלס חשף 538 חלבוני אדם שמתקשרים עם NS4B ולמעלה מ־500 שחלות בהם שינויים בשפע כשה־NS4B נוכח. רבים מהם מרוכזים במסלולים המנהלים ייצור אנרגיה במיטוכונדריה, עיצוב ממברנות פנימיות ותנועה של חלבונים ושומנים חדשים. חלק מהאינטראקציות היו משותפות לרוב הוירוסים, מרמזות על טריקים משומרים אבולוציונית שכל האורתופלביווירוסים משתמשים בהם. אחרות הופיעו רק במינים או בזנים מסוימים, ועשויות להסביר מדוע חלק מהוירוסים מעדיפים יתושים על פני קרציות, או גורמים למחלות מוח במקום קדחת מדממת. התמונה הסיסטמטית הזו מאחדת סדרת מחקרים מפוזרת לקראת מפת קוהרנטית של האופן שבו הוירוסים האלה משנים את פעולת התא.
בעל ברית מפתיע: מערכת ה‑UFMylation
בין שותפי הרבים ש־NS4B התחבר אליהם, אחד בלט: UBA5, האנזים הפותח של מסלול ה‑UFMylation. UFMylation היא מערכת תאית שמחברת תג חלבוני קטן, UFM1, למטרות נבחרות, ומשפיעה על תהליכים כמו בקרת איכות חלבון ותגובת מתח. באמצעות התערבות RNA ונוקאאוטים מבוססי CRISPR, הצוות הראה שתאים החסרים UBA5 או שאינם יכולים לבצע UFMylation חוו ירידה משמעותית בשכפול זיקה ומספר וירוסים קשורים. החזרת UBA5 נורמלי שיקמה את גדילת הוירוס, בעוד שצורות מוטנטיות שלא יכולות להניע UFMylation לא עשו כן, והוכיחו כי פעילות התגית עצמה חיונית לזיהום.
כיצד התיוג תומך במפעלים ויראליים
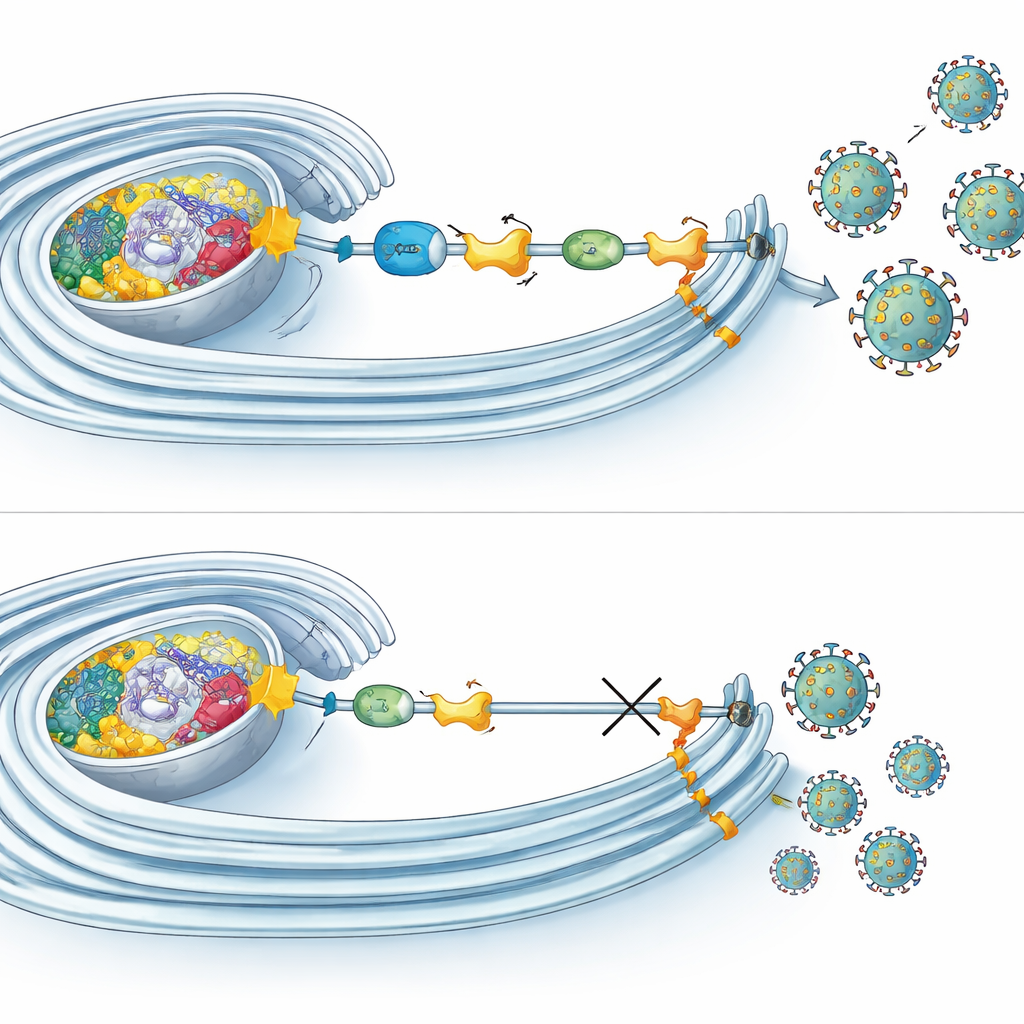
מיקרוסקופיה וניסויים ביוכימיים הראו כי מרכיבים רבים של מערכת ה‑UFMylation מתרכזים בדיוק באתרים שבהם עותק ה‑RNA הוירלי נוצר בתוך ממברנות שעוצבו מחדש. שם הם מקושרים לא רק עם NS4B אלא גם עם חלבונים ויראליים אחרים שבונים את מכונת השכפול. מעניין לציין שחסימת UFMylation לא עצרה כניסת הוירוס, ייצור RNA או סינתזת חלבון. במקום זאת היא פגמה בעיקר בשלבים המאוחרים של המחזור, כגון הרכבה או שחרור של חלקיקים מידבקים. במקביל, התברר ש‑UFMylation משפיעה על אופן נשימת המיטוכונדריה: כאשר המסלול הושבת, התאים הראו צריכת חמצן מופחתת וצורות מיטוכונדריאליות משונות. לעומת זאת, בשלבים המוקדמים של זיהום בזיקה, נשימת המיטוכונדריה עלתה, מה שמרמז כי הוירוסים עשויים לנצל את ה‑UFMylation להגברת תפוקת האנרגיה של התא בדיוק כשהם זקוקים לה ביותר.
בדיקת תרופה בתאים ובדגיגים זעירים
המחברים פנו אז לתרכובת מולקולרית קטנה, DKM 2‑93, החוסמת את אתר הפעולה של UBA5. בתאים אנושיים בתרבית, המעכב צמצם את ייצור נגיף הזיקה בכ־עשר פעמים במינונים שמשאירים את התאים ברובם בריאים, והראה פעילות במספר סוגי תאים. כדי לבדוק האם אסטרטגיה זו יכולה לפעול באורגניזם חי, השתמשו במודל דג זברה לזיהום בזיקה, המדמה מאפיינים מרכזיים של המחלה במוח המתפתח. טיפול בעוברים מודבקים ב‑DKM 2‑93 במהלך התפתחות מוחית מוקדמת הפחית משמעותית את רמות ה‑RNA הוירלי והקטין את אחוז הדגים שהראו מומים קשים, דבר שמעיד על תועלת אנטי־ויראלית ממשית במסלול חי.
מה משמעות זה עבור טיפולים עתידיים
על ידי בניית מפת אינטראקציות מקיפה של NS4B ממספר אורתופלביווירוסים וכיצד הוא מתקשר עם חלבוני אדם, המחקר מדגיש את ה‑UFMylation כנתיב מסייע משומר שהוירוסים האלה תלויים בו ליצירת חלקיקים מידבקים. מכיוון שמערכת המארח אותה נראית תומכת בדנגי, זיקה, ווסט ניל ואחרים, תרופות שממעטות בבחירה את פעולת ה‑UFMylation עשויות לשמש כנוגדי וירוס רחבי־טווח, במקום למקד כל פעם וירוס אחד. בעוד שעדיין דרושות עבודות נוספות כדי להבין בדיוק אילו חלבונים מתוייגים ולהבטיח בטיחות, הממצאים מזהים יעד מבוסס מארח מבטיח שעשוי יום אחד לסייע בריסון התפרצויות של מחלות הנישאות על ידי יתושים וקרציות בגישה טיפולית אחת.
ציטוט: Rajasekharan, S., Barragan Torres, V.A., Pinheiro Gomes, Y.C. et al. A genus-wide interaction atlas across NS4B orthologues identifies a conserved role for UFMylation in orthoflavivirus replication. Nat Commun 17, 2489 (2026). https://doi.org/10.1038/s41467-026-70437-9
מילות מפתח: נגיף זיקה, דנגי, אינטראקציות מארח–וירוס, UFMylation, נוגדי וירוס רחבי-טווח