Clear Sky Science · he
אפיון מנגנוני מבוסס מסיסות של טיפול משולב בתרופות
מדוע השילוב של תרופות חשוב
הטיפול המודרני בסרטן מסתמך לעתים קרובות על שילובי תרופות, אך קביעת אילו תרופות פועלות טוב יחד נשארת במידה רבה ניסוי וטעייה. המחקר הזה מתמקד בלויקמיה מיאלואידית חריפה, סרטן דם תוקפני החוזר לעתים קרובות אחרי טיפול. החוקרים מציעים דרך חדשה לצפות, בכמות גדולה, כיצד חלבוני התאים מגיבים כאשר ניתנות שתי תרופות יחד. הגישה שלהם מסבירה מדוע שילובים מסוימים יעילים יותר ופחות רעילים, ומספקת מפת דרכים לעיצוב טיפולים משולבים חכמים ומדויקים יותר למקרים קשים.
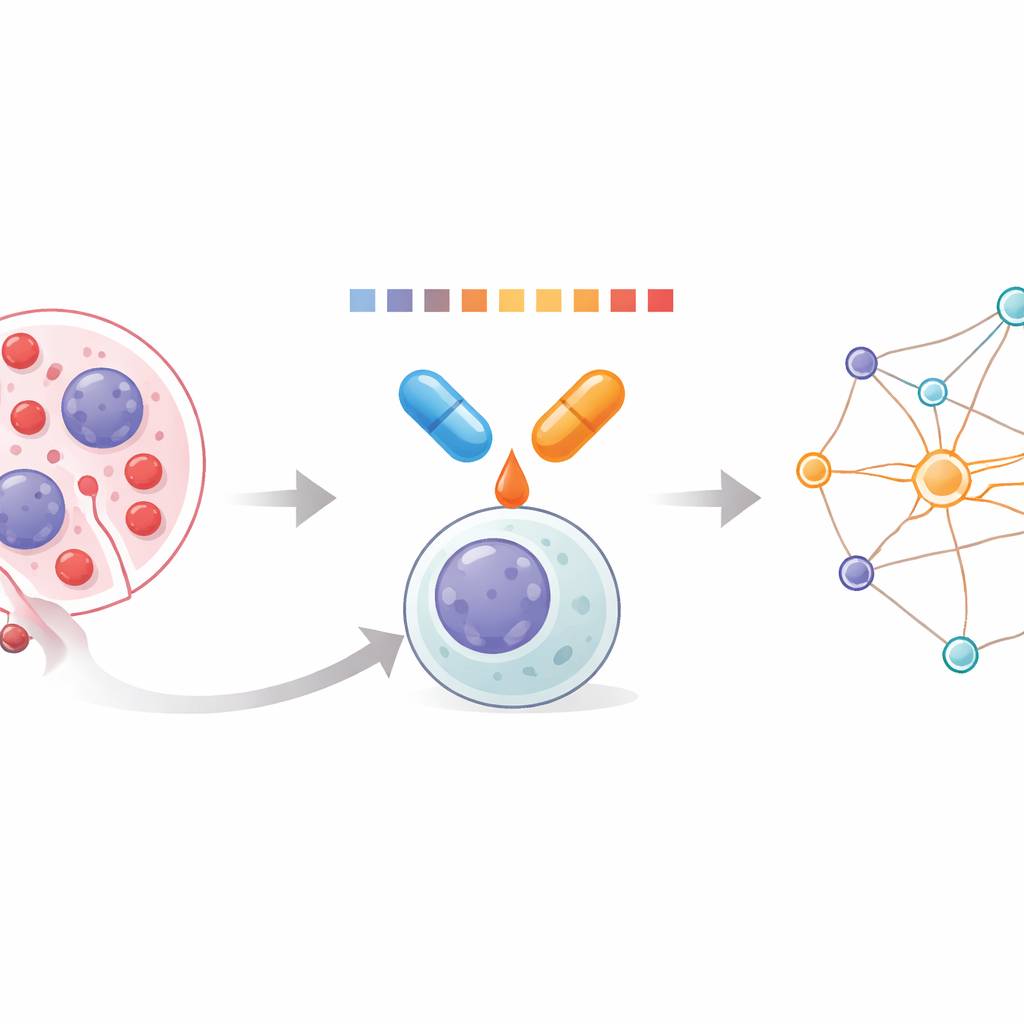
מבט פנימי לתאי הלוקמיה
לויקמיה מיאלואידית חריפה (AML) נוצרת כאשר תאי דם לבנים בלתי בשלים במח העצם גדלים ללא שליטה ומדחקים את יצירת הדם התקינה. מכיוון ש-AML מונעת על ידי שינויים גנטיים רבים ושונים, תרופות בודדות נדירות פועלות לאורך זמן. שילובים יכולים להיות יעילים יותר, אך לרופאים היו כלי מוגבלים לראות כיצד זוגות תרופות פועלים יחד ברמת אלפי חלבונים בתוך התא. הצוות מאחורי העבודה הזו שאף למדוד את השפעות השילוב ישירות, באמצעות שיטה שקוראת עד כמה חלבונים נמסים או מתקבצים כאשר מחממים אותם. שינויים במסיסות חושפים אילו חלבונים מתייצבים או מתפרקים בעקבות הטיפול, ומהווים חלון להשפעה האמיתית של התרופות.
דרך חדשה לפרופיל זוגות תרופות
החוקרים פיתחו זרימת עבודה שהם קוראים לה ניתוח שינויי מסיסות/יציבות אינטגרלית של הפרוטאום המשולב (Combinatorial Proteome Integral Solubility/Stability Alteration), או CoPISA. תאים, או תמציות החלבון שלהם, נחשפים לתרופה A, לתרופה B, לשילוב של A ו-B, או ללא תרופה. כל דגימה מחוממת בקצרה בסדרה של טמפרטורות, והחלבונים שנשארים מסיסים נתפסים ומוכריםזים בכמות בעזרת ספקטרומטריית מסה. במקום להתאים עקומות מורכבות חלבון חלבון, השיטה משתמשת בשטח הכולל תחת פרופיל ההתכה של כל חלבון כמדד דחוס של התנהגותו. השוואת שטחים אלה בין הטיפולים מראה אילו חלבונים הופכים למסיסים יותר או פחות בכל תנאי, וחושפת דפוסים הנבדלים בין תרופות בודדות לשילובים.
מציאת מטרות שמופיעות רק בנוכחות שתי התרופות
CoPISA יושמה על שני זוגות תרופות ל-AML שנבחרו בקפידה: LY3009120 עם סאפאניסטיב (שנקרא LS), ורוקסוליטיניב עם אוליקסרטיניב (RU). זוגות אלה הראו כבר פעילות חזקה ורעילות יחסית נמוכה במדגמים של חולים, בקווי תאים ובמודלים של דגי זברה. CoPISA חשפה לא רק חלבונים שהושפעו מכל תרופה לחוד, אלא גם סט מובחן של חלבונים שמסיסותם השתנתה רק כאשר שתי התרופות היו נוכחות. המחברים מתארים זאת כ"מטרתיות משולבת" (conjunctional targeting), בדומה לשער לוגי AND: החלבון מגיב רק אם שני הקלטים (התרופות) דלוקים. עבור LS, השפעות ייחודיות לשילוב התמקדו בתהליכים כמו אריזת ה-DNA, תגיות חלבוניות קטנות בשם SUMO ששולטות ביציבות הגנום, ואופן הידבקות תאי הלוקמיה לרקמתם. עבור RU, המטרות הייחודיות הצביעו על החלשות נקודות ביקורת של נזק ל-DNA, פגיעה בייצור אנרגיה במיטוכונדריה והפרעה בעיבוד RNA.
מיפוי הנקודות החלשות של הסרטן
על ידי הצמדת נתוני המסיסות שלהם למפות גדולות של גנים ומסלולים הקשורים ל-AML, החוקרים יכלו לראות כיצד כל טיפול שינה את הרשת הפנימית של הסרטן. גנים מוכרים רבים ב-AML — כגון DNMT3A, NPM1 ו-TP53 — הושפעו באופן שנראה רק בטיפול משולב, מה שמחזק את הרעיון ששילוב תרופות יכול לחשוף פגיעויות שאינן נראות לסוכנים בודדים. הצוות בחן גם קישוטים כימיים על חלבונים, כגון אצטילציה, מתילציה ופוספורילציה, הפועלים כמפסקים מולקולריים. הם מצאו שצורות מסוימות שעברו שינוי של חלבונים מרכזיים, כולל NPM1 ופקטור תיקון ה-DNA BLM, הוכו ספציפית על ידי השילובים, מה שמעיד על כך שהשינוי במיקום החלבון ובאותות תורם להשפעה המחוזקת.
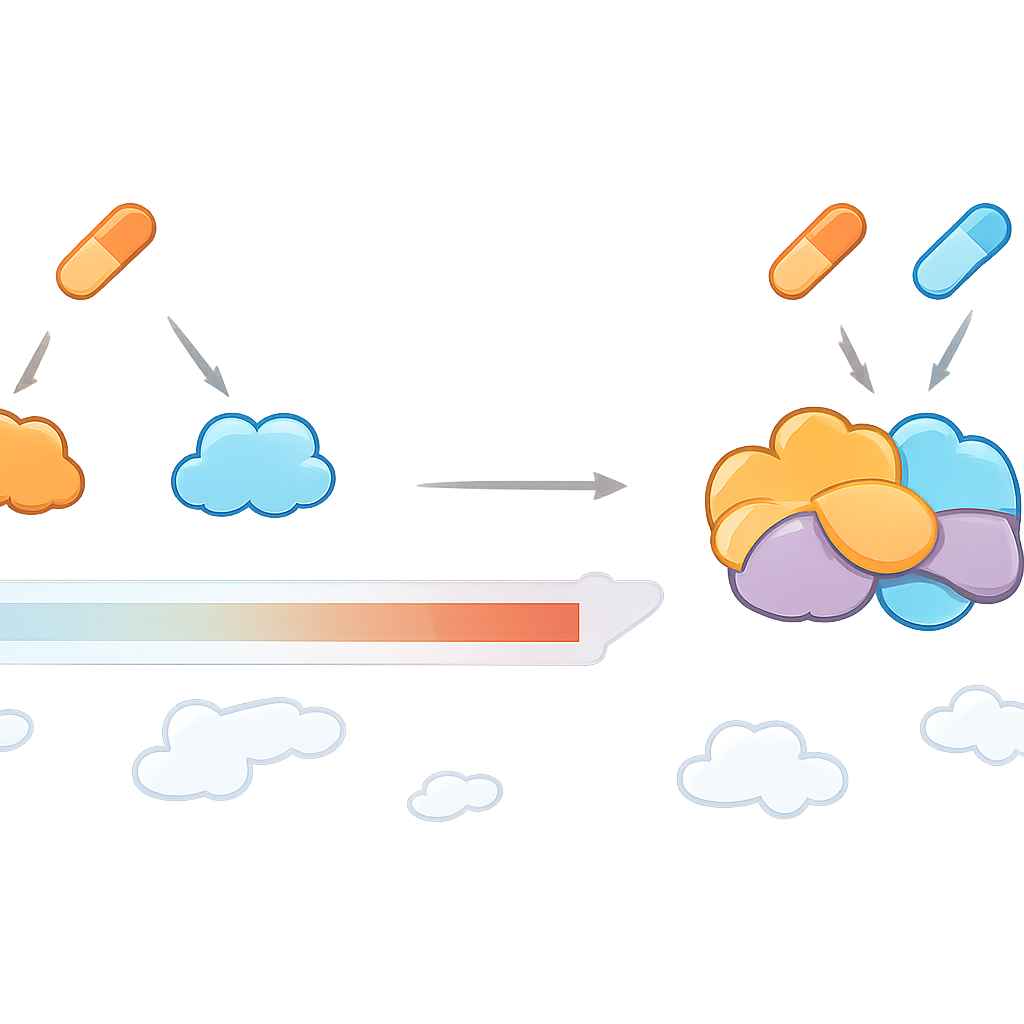
מה משמעות הדבר לטיפולים עתידיים
בסך הכל, המחקר מראה ששילובי תרופות יכולים ליצור נוף ייחודי של מטרות חלבוניות, ולא פשוט לחבר יחד את השפעות כל תרופה בנפרד. CoPISA מספקת דרך פרקטית למפות נוף זה, ומדגישה חלבונים ומסלולים שהופכים לפגיעים רק כאשר שתי תרופות פועלות במקביל. עבור מטופלים, הדבר עשוי להתבטא בבחירת טיפולים משולבים לא רק כי הם מצמצמים גידולים במבחנה, אלא כי הם נוגעים בנקודות החלשות העמוקות של הסרטן תוך הגבלת רעילות מיותרת. אף שהודגם כאן ב-AML, הגישה רחבה ויכולה לסייע בעיצוב רציונלי של טיפולים משולבים במגוון מחלות מורכבות.
ציטוט: Gholizadeh, E., Zangene, E., Vadadokhau, U. et al. Solubility based mechanistic profiling of combinatorial drug therapy. Nat Commun 17, 2744 (2026). https://doi.org/10.1038/s41467-026-70394-3
מילות מפתח: לויקמיה מיאלואידית חריפה, שילובי תרופות, פרוטאומיקה, מסיסות חלבונים, טיפול ממוקד