Clear Sky Science · he
בקרת תפקוד הליזוזום על ידי חלבון מאיץ הידרוליזת GTP TBC1D9B ובן‑זוגו הקושר TMEM55B
איך מרכזי המיחזור בתא שומרים על שיווי המשקל
בתוך כל תא שלנו נמצאים שקיקים זעירים הנקראים ליזוזומים, שמשמשים כמרכזי מיחזור וכנקודות בקרה לצמיחה. כשהם פועלים היטב, חלקים שחוקים מפורקים והרכיבים שלהם מנוצלים מחדש; כשהם נכשלו, פסולת מצטברת ועלולות להופיע מחלות, כולל ניורודגנרציה וסרטן. המחקר הזה מגלה כיצד שני חלבונים מעט מוכרים מסייעים להעביר את הליזוזומים בין מצב נייד ותומך־צמיחה לבין מצב מצטבר המיועד לפינוי פסולת, ומאיר את הדרך שבה תאים מסתגלים לשפע ולרעב.
הזזת מרכזי המיחזור בתא
ליזוזומים אינם קבועים במקומם. הם נעים לאורך מסלולים פנימיים, נגרפים החוצה על‑ידי קבוצת מוטורים מולקולריים ונמשכים פנימה על‑ידי אחרים. המיקום שלהם בתא חשוב: כאשר המזון בשפע, הליזוזומים מתפזרים לעבר אזורים חיצוניים של התא ותורמים לאיתותי צמיחה; כאשר המזון נדיר, הם נסוגים למרכז, החומציות שלהם עולה, והם מגבירים את פירוק החומר התאי. חלבון קטן בסגנון מפתח־מנוף בשם ARL8 ידוע בכך שהוא דוחף את הליזוזומים החוצה, אבל עד כה לא זוהה מנגנון־בלימה ייעודי שיפעיל עליו מעצור. המחברים חשדו שמעצור כזה יהיה קריטי כדי לאפשר לתאים לעבור במהירות למצב חיסכון בזמן רעב.
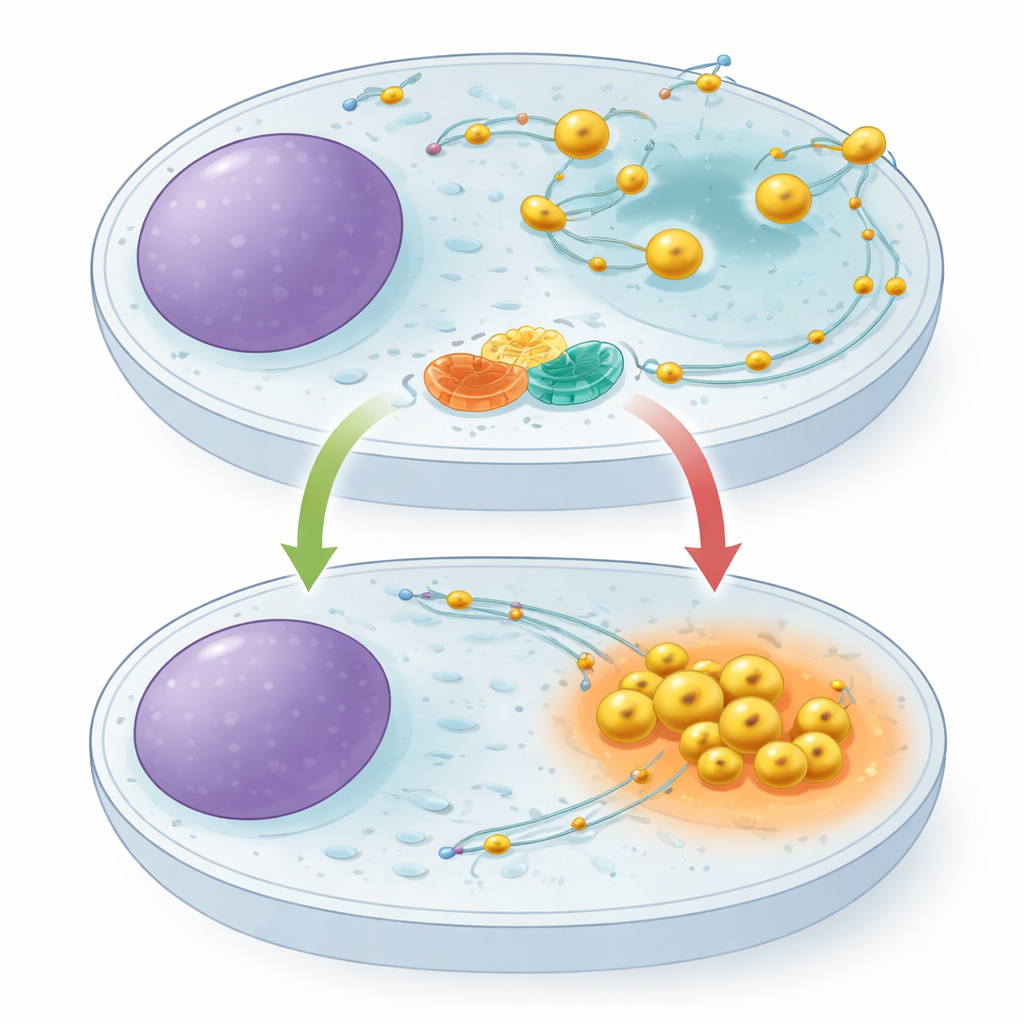
שותפות מולקולרית על פני מעטפת הליזוזום
באמצעות שיטות „דיג חלבונים" וספקטרומטריית מסה, החוקרים גילו שחלבון בשם TBC1D9B מתחבר לחלבון ממברנלי ליזוזומלי שנקרא TMEM55B. TMEM55B משתרע על פני מעטפת הליזוזום, בעוד ש‑TBC1D9B ברובו מסיס ויכול לעגין על הממברנה. הצוות הראה ששניים אלה יוצרים קומפלקס ישיר: TBC1D9B מטוהר נדבק לחלק החשוף של TMEM55B בצינורות מבחנה, וגרסאות מתוייגות של החלבונים מושכות זו את זו מתוך תמציות תאים. מיפוי קפדני של מקטעי החלבון חשף שמספר אזורים ב‑TBC1D9B נוגעים ב‑TMEM55B, וממקמים את TBC1D9B על פני הליזוזום מבלי לחסום את החלק האחראי לפעילות הקטליטית שלו.
כשהמעצור נכשל, הליזוזומים יוצאים משליטה
כדי לגלות מה עושה השותפות הזו, המחברים השתמשו בעריכת CRISPR כדי להסיר או את TMEM55B או את TBC1D9B מתאים אנושיים. בשני המקרים, הליזוזומים הפסיקו להצטבר בסמוך לגרעין ובמקום זאת התפזרו לעבר קצה התא ונעו מהר יותר לאורך המסלולים שלהם, מה שהדמה מצב של תא תמיד מאוכל. החזרת TBC1D9B תקין השיבה את המיקום הנכון, אך גרסה חסרת פעילות קטליטית לא עשתה זאת, מה שמעיד שפעילות האנזימטית שלה חיונית. כאשר התאים הועברו לצום, תאים בקרה משכו את הליזוזומים פנימה והגבירו את כוח העיכול שלהם, כפי שנמדד על‑ידי עלייה בפעילות אנזימים מרכזיים ובהגברה של פירוק מטען ניסיוני. תאים חסרי TMEM55B או TBC1D9B נכשלו בכך: ליזוזומיהם נשארו פריפריאליים ותגובת הפירוק שלהם לרעב הייתה מוחלשת. גם האוטופגיה — התהליך שבו תאים ‘‘אוכלים עצמם’’ על מנת לעבד רכיבים פגומים — נפגעה, עם עיבוד פחות יעיל של מדד האוטופגיה והצטברות של חלבון הסיגנון p62.
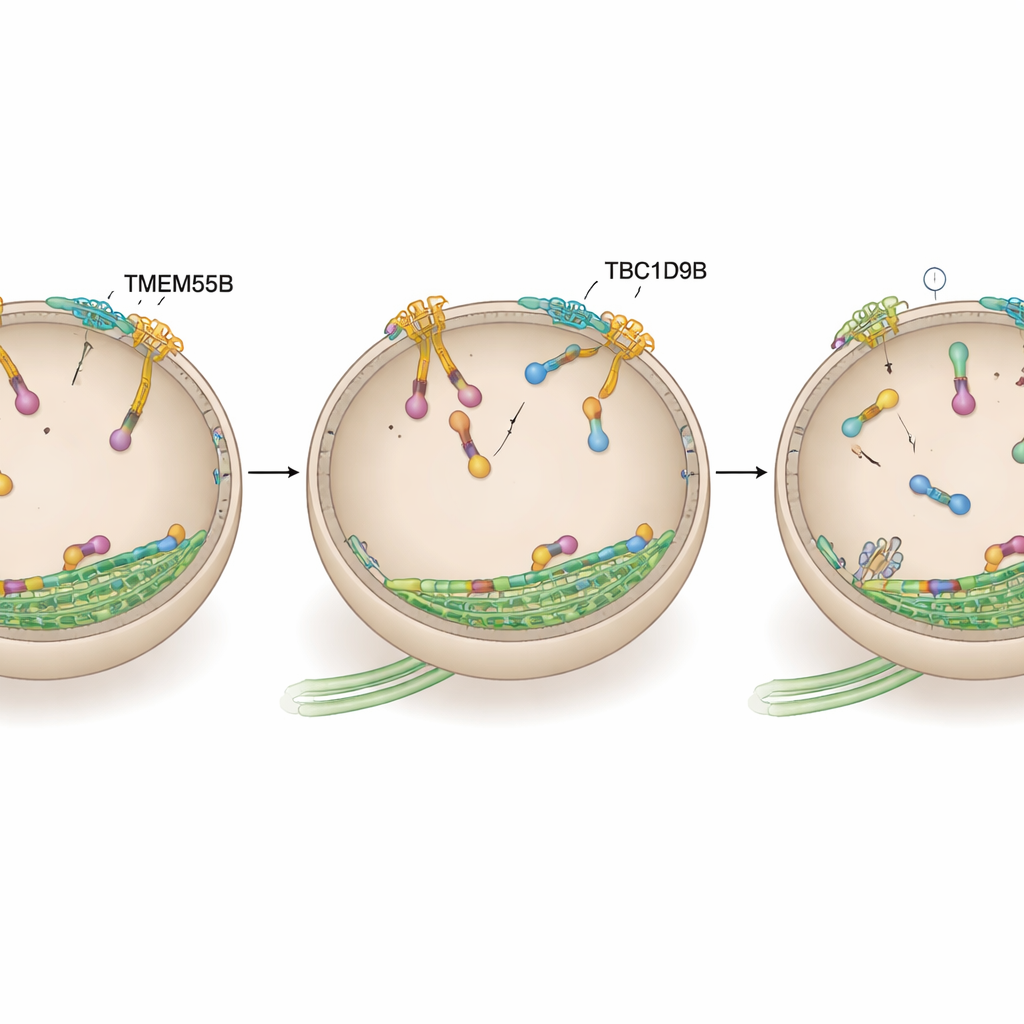
כיבוי המנוע של הליזוזום
הצוות שאל האם TBC1D9B משפיע ישירות על ARL8, המתג שמוביל החוצה. באמצעות תיוג קרבה בעצבי אדם וניסויי קישור בקווי תאים ובחלבונים מטוהרים, הם הראו ש‑TBC1D9B נקשר באופן סלקטיבי לצורתו הפעילה, טעונת GTP, של המשטה ARL8B, אך לא לצורתו הלא פעילה ולא ל־ARL8A הקרוב לו. דוגמנות מבנית ניבאה כי שאריות מרכזיות ב‑TBC1D9B נוגעות לכיס ה‑GTP של ARL8B. בניסויי ביוכימיה, TBC1D9B האיץ את הידרוליזת ה‑GTP הקשור ל‑ARL8B, והפך את החלבון ממצב "דלק" למצב "כבה"; גרסה מוטנטית של TBC1D9B שחסרה שאריות אלה לא יכלה לעשות זאת. בהתאמה, תאים חסרי TMEM55B או TBC1D9B הראו עליה ב‑ARL8B על הליזוזומים, בעוד שהבעה מופרזת של TBC1D9B משכה את הליזוזומים חזרה למרכז, בדומה להורדת פעילות ARL8B.
כפתור בקרה חדש למשמורת התאית
לבסוף, המחברים בדקו האם מעצור ARL8B הזה מסביר את השינויים התאיתיים שנצפו בהיעדר TBC1D9B. כאשר ARL8B הוסר, הליזוזומים נשארו מצטברים סביב הגרעין ללא תלות בנוכחות TMEM55B או TBC1D9B, והפגמים באוטופגיה שנגרמו מאובדן TBC1D9B בוטלו ברובם. יחד, הנתונים תומכים במודל שבו TMEM55B מגייס את TBC1D9B לליזוזומים, שם זה ממטע את ARL8B ומאפשר לליזוזומים לעבור ממצב מפוזר התומך בצמיחה למצב מרוכז המתמקד בעיכול. עבור קהל לא‑מומחה, משמעות הדבר היא שהמחקר חשף אגודל בקרה חשוב שהתאים משתמשים בו כדי להחליט מתי למחזר באופן אינטנסיבי יותר — תהליך שיש לו השלכות להפרעות של הצטברות פסולת במוח, למטבוליזם ולסרטן.
ציטוט: Duhay, V., Tian, M., Kosieradzka, K. et al. Control of lysosome function by the GTPase-activating protein TBC1D9B and its binding partner TMEM55B. Nat Commun 17, 2487 (2026). https://doi.org/10.1038/s41467-026-70345-y
מילות מפתח: ליזוזומים, אוטופגיה, אותות תאיים, הובלת אברונים, ניורודגנרציה