Clear Sky Science · he
שיקום דיסרגולציה סינפטית מוקדמת לאחר הלידה מצילדגנון נוירונים מוטוריים בעכבר עם דגם של אטרופיה שרירית שדרתי-בלורית
מדוע שינויים זעירים מוקדמים יכולים להשפיע על חולשת השרירים אחר כך
אטרופיה שרירית שדרתי-בלורית (SBMA) היא מצב תורשתי נדיר שבו מבוגרים, לרוב גברים, מאבדים בהדרגה כוח בגפיים, בגזע ובגרון. התסמינים מופיעים באמצע החיים, אבל בעיות עדינות מתחילות הרבה קודם. המחקר הזה שואל שאלה מפתיעה: האם אירועים קצרים בימים הראשונים לאחר הלידה עלולים לשים במתינות את הבסיס לאובדן תאי העצב שנים או עשורים אחר כך — והאם תיקון התקלים המוקדמים האלה יכול להגן על התנועה?
מחלה שמושרשת במתג הרגיש להורמונים
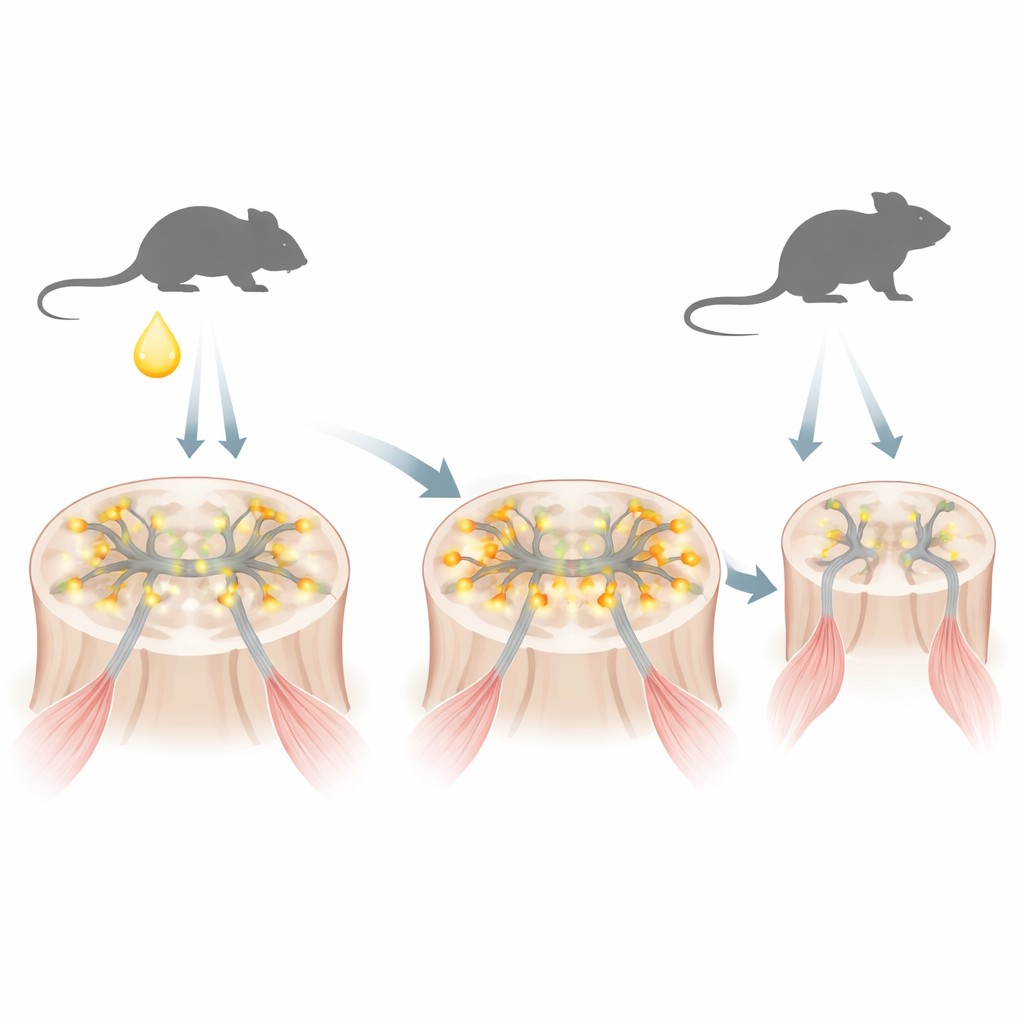
SBMA נגרמת מגרסה משנה של קולטן האנדרוגן, חלבון החוש את ההורמונים המיניים הזכרים כגון טסטוסטרון. הקולטן המוטנטי נושא רצף ארוך מדי של חומצת האמינו גלוטמין. בדגם עכבר המדמה את המחלה האנושית, המחברים מצאו שמיד לאחר הלידה, כשיש עלייה זמנית בטסטוסטרון אצל זכרים צעירים, הקולטן המוטנטי מצטבר במהירות בתוך גרעיני תאי העצב המוטוריים — תאים שמוּפַקדים על שליטת השרירים. בשלב מוקדם זה החלבון עדיין לא התמזג לצברים גדולים הקשורים בדרך כלל לנוירודגנרציה, אך הוא כבר משנה אילו גנים נדלקים וכבים.
עודף פעילות סינפטית מוקדמת ותאי עצב מוטוריים חסרי מנוחה
באמצעות רצף RNA ברמת הגנום של חוט השדרה של עכברים ניו־נולדים, הצוות גילה שרבים מהגנים המעורבים בסינפסות מעוררות — נקודות המגע שבהן תאים עצביים משדרים זה לזה — היו פעילים באופן חריג. רבים מהגנים האלה מקודדים לקולטי גלוטמט, שעושים את הנוירונים נוטים יותר לירות. הקבוצה עקבה אחרי התבנית הזו ונמצאה שהיא נובעת מהפרעה בפעילות REST, חלבון «בלם» ראשי שמקפיד בדרך כלל על שליטה הדוקה בגנים סינפטיים במהלך ההתפתחות. בעכברי SBMA ובנוירונים מוטוריים שגודלו מתאי גזע פרי־השרייה של מטופלים, פעילות REST הוחלשה וצורת קיצוץ קצרת אורך הנקראת REST4 הועדפה, מה שהרים את הבלם והגביר את ביטוי גני הסינפסות הגלוטמרגיות. בהתאם לכך, תאי עצב מוטוריים של ניו־נולדים עם SBMA הראו רמות גבוהות יותר של c-Fos, סמן של ירי אחרון, ותאי עצב מוטוריים שמקורם במטופלים אנושיים הציגו התפרצויות סידן חזקות ותכופות יותר — סימנים של היפראקסיטציה.
טיפול קצר מוקדם שמשנה מהלך חיים
החוקרים שאלו האם הפחתת הקולטן המוטנטי או שחזור בלם REST רק בחלון הנו neonatal יכול לשנות את מהלך המחלה בטווח הארוך. הם הזריקו אוליגונוקלאוטידים אנטיסנס — מקטעים קצרים של חומר גנטי מותאם — לנוזל סביב המוח וחוט השדרה של עכברי SBMA בני יום אחד. סוג אחד של אוליגונוקליאוטיד הוריד באופן זמני גם את הקולטן המוטנטי וגם את הקולטן הרגיל במערכת העצבים המרכזית. סוג שני השפיע על עיבוד ה־RNA של REST כך שהספlicing הוסט הרחק מ־REST4 וחזרה לצורת REST המלאה, ובכך שיקם את הבקרה על גני הסינפסה. באופן מיידי מופלא, אף על פי שהטיפולים ניתנו רק פעם אחת והשפעותיהם המולקולריות הישירות דהו בתוך מספר שבועות, העכברים חיו זמן רב יותר, הלכו טוב יותר על מוט מסתובב והחזיקו חזק יותר מאוחר בחיים. תאי העצב המוטוריים וסיבי השריר שלהם היו פחות מצטמקים, וסימני מוקדמות של יתר־פעילות נוירונלית ושל פרץ מאוחר של נוירופפטידים הקשורים ללחץ הומרו.
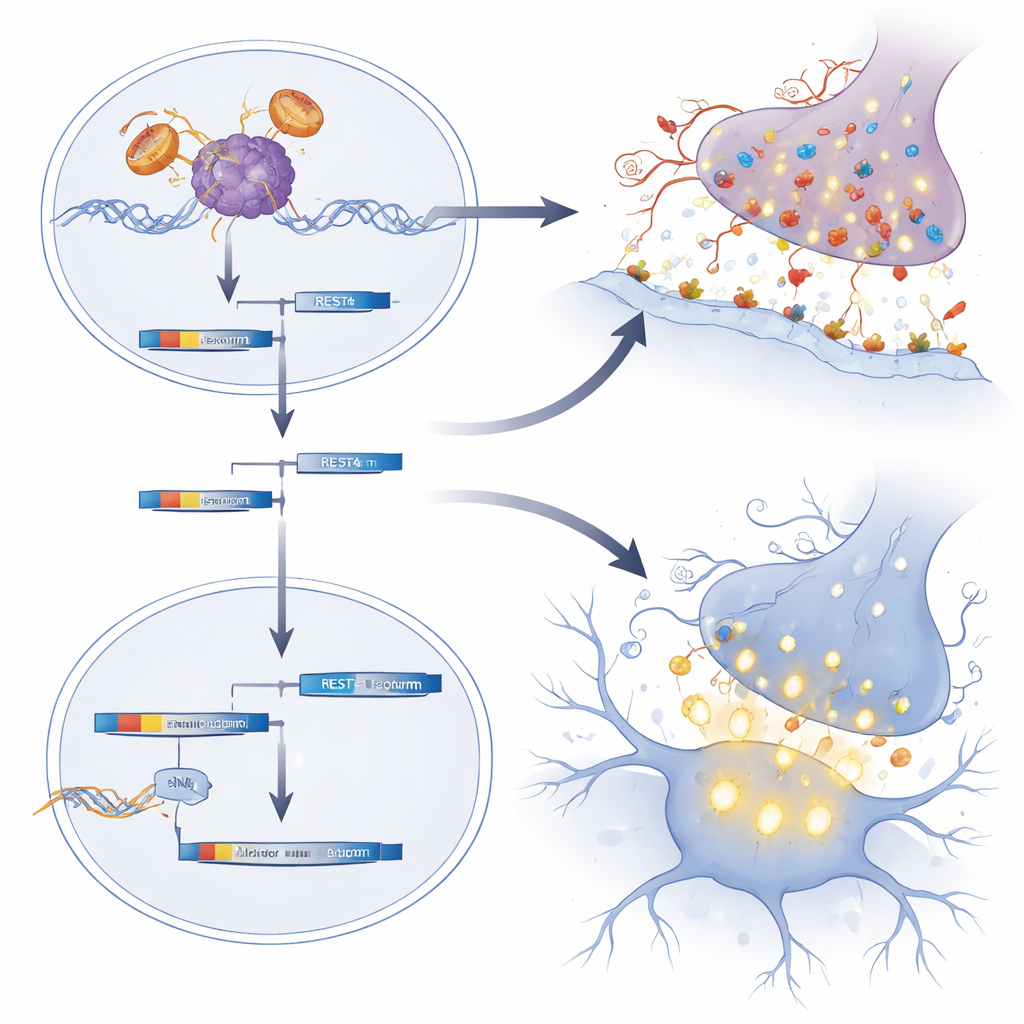
כיצד הורמונים מוקדמים וכיוונון גנים מעצבים פגיעות
העבודה גם מדגישה את הפגיעות המיוחדת של תאי העצב המוטוריים לפרץ הקצר של טסטוסטרון המתרחש זמן קצר לאחר הלידה. כאשר עכרי SBMA ניו־נולדים קיבלו תוספת טסטוסטרון, החולשה והירידה במשקל בהמשך הוחמרו, ותכניות גנטיות הקשורות לבשלות בריאה של תאי העצב המוטוריים הופרעו עוד יותר. בעכברים רגילים לא נצפה נזק כזה, מה שמדגיש שהשילוב של הקולטן המוטנטי עם הפרץ ההורמונלי הוא זה שמזיק. יחד, הממצאים מרמזים שבעת SBMA, עודף סינפסות מעוררות ותאי עצב מוטוריים יתר־רגישים בתחילת החיים דוחפים לאט לאט את המערכת לכשל, אף על פי שהתסמינים הברורים אינם נראים עד אמצע החיים.
מה משמעות הדבר לאנשים החיים עם SBMA
בעיני מי שאינו מומחה, המסר המרכזי הוא ש־SBMA עשויה להיות, בחלקה, מחלה של סינפסות שנקבעו בזמן ובמבנה בצורה שגויה בימים הראשונים לאחר הלידה. חיישן הורמונלי פגום דוחף תאי עצב מוטוריים מתפתחים למצב של יתר־עוררות, ולחץ מוקדם זה תורם בסופו של דבר להתנוונותם שנים לאחר מכן. החדשות המעודדות הן שתרופות גנטיות מתוכננות בקפידה, שניתנות בחלונות קריטיים אלה, יכולות לאפס את מאזן האותות בתאי העצב המוטוריים, להרגיע את יתר־הפעילות שלהם ולעכב או לצמצם משמעותית את אובדן התאים בהמשך בבעלי חיים. בעוד שהעברה של התערבויות כאלה לאנשים תדרוש זהירות רבה ולימוד נוסף, התוצאות האלה מצביעות על אסטרטגיות חדשות המתמקדות בשורשי SBMA הרבה לפני שהחולשה מופיעה.
ציטוט: Hirunagi, T., Sahashi, K., Iida, M. et al. Restoring early postnatal synaptic dysregulation rescues motor neuron degeneration in a mouse model of Spinal and Bulbar Muscular Atrophy. Nat Commun 17, 2412 (2026). https://doi.org/10.1038/s41467-026-70244-2
מילות מפתח: אטרופיה שרירית שדרתי-בלורית, יתר־גירוי של תאי עצב מוטוריים, קולטן אנדרוגן, רגולציית סינפסה על ידי REST, תרפיית אוליגונוקלאוטידים אנטיסנס