Clear Sky Science · he
DiNovo מאפשר רצפי פפטידים de novo עם כיסוי גבוה וביטחון גבוה בעזרת פרוטאזות מראה ולמידת עומק
להביט בחלבונים בפרטים חדשים
חלבונים הם המכונות המיקרוסקופיות שמחזיקות את התאים שלנו בחיים, אך קריאת המבנים שלהם במלואם עדיין קשה באופן מפתיע. מאמר זה מציג את DiNovo, מערכת תוכנה חדשה המסייעת למדענים "לקרוא" מקטעי חלבון בצורה הרבה יותר מלאה ואמינה מאשר בעבר. על ידי שילוב של תחבולה ביוכימית חכמה עם בינה מלאכותית מודרנית, היא מבטיחה לחשוף חלבונים נסתרים, סמני מחלה ואפילו מטרות חיסוניות ששיטות מסורתיות לעתים קרובות מפספסות.
למה קריאת מקטעי חלבון כה מאתגרת
הרוב הגדול של ניתוח חלבונים כיום מסתמך על חיתוך החלבונים לחתיכות קטנות יותר, הנקראות פפטידים, ואז שקילת שבריהם בספקטרומטר מסה. מתוך משקלים אלה, מחשבים מנסים לשחזר את רצף הפפטיד המקורי, כמו לפתור תשבץ מתוך רמזים חלקיים. שיטות קיימות בדרך כלל מניחות שהפפטידים נובעים ממסדי נתונים של חלבונים ידועים, מה שעובד היטב עבור חלבונים מוכרים אך מתקשה עם חלבונים חדשים או בלתי צפויים. ריצוף מסוג de novo נמנע מהמגבלה הזו על ידי ניסיון לקרוא פפטידים ישירות מהנתונים, אבל לעתים קרובות נכשל כיוון שיש חסרים בחלק מהשברים וכיוון שחלק מהפפטידים מעולם לא נחתכים בצורה נקייה מלכתחילה.
שימוש באנזימים מראה למילוי הרווחים
הרעיון המרכזי מאחורי DiNovo הוא שימוש בזוגות של "פרוטאזות מראה" – זוגות של אנזימי חיתוך החותכים את החלבון בצידן הנגדי של אותו סוג חומצת אמינו. לדוגמה, אנזים אחד חותך ממש לפני ליזין בעוד שבן הזוג שלו חותך ממש אחרי אותה ליזין. זה מייצר שני פפטידים קשורים שחולקים את הקטע הפנימי אך שונים בקצוות. כאשר מנתחים את הפפטידים ה"מראיים" האלה, ספקטרות המסה שלהם מכילות דפוסי שבירה משלימים: מה שחסר בספקטרום אחד לעתים קרובות מופיע בשני. הכותבים מראים ששילוב זוגות מראה כאלה יכול לדחוף את כיסוי השברים כמעט למצב שלמות, עם כ~98% מחיתוכים אפשריים הנתמכים על ידי אותות ניסויים אמיתיים, הרבה יותר מאשר כשמשתמשים באנזים יחיד בלבד.
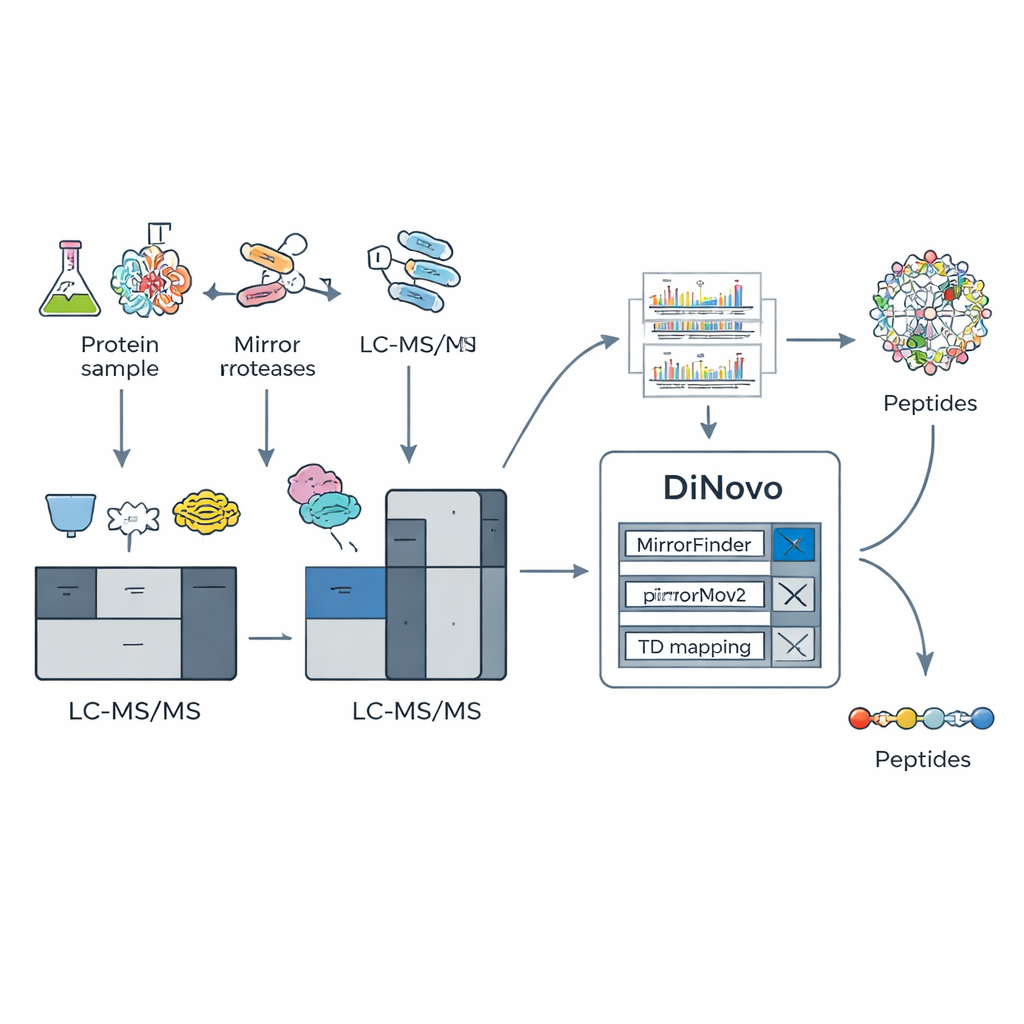
צנרת תוכנה חכמה שנבנתה עבור נתוני מראה
כדי לנצל את התחבולה הביוכימית הזו, הצוות בנה את DiNovo כזרימת עבודה מקצה לקצה. תחילה, חלבונים מבקטריה ושמרים מעוכלים עם שני זוגות מראה של אנזימים, והפפטידים המתקבלים מנותחים באמצעות ספקטרומטר מסה ברזולוציה גבוהה. DiNovo משתמשת אז במודול שנקרא MirrorFinder כדי לזהות אוטומטית אילו זוגות ספקטרות נובעים מפפטידים מזוג מראה, ועושה זאת ישירות מתוך דפוסי האות במקום להסתמך על ניחושים רצפיים מוקדמים. לאחר מכן, מנוע ה-de novo הראשי שלה, MirrorNovo, משתמש בלמידת עומק כדי לפרש את הספקטרות המזוגות, בעוד שמנוע גיבוי מבוסס גרף, pNovoM2, מציע אופציה מהירה יותר הפועלת רק על CPU. יחד, הכלים האלה מתרגמים פסגות לרצפי חומצות אמינו ובודקים גם את הספקטרות האישיות שלא יצרו זוגות ברורים, וממיצים כמה שיותר מידע.
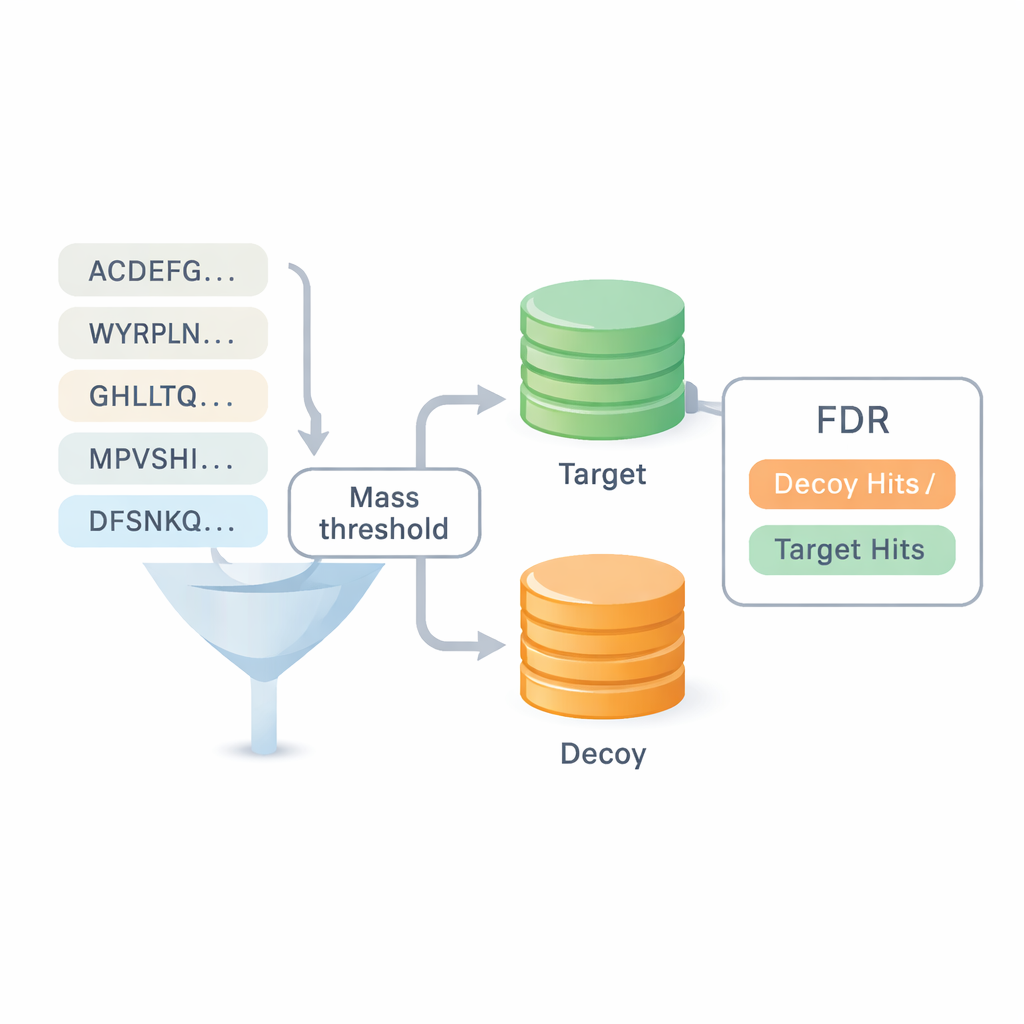
מדידת אמינות בלי להישען על מסדי נתונים ישנים
אחת השאלות הגדולות בריצוף de novo היא כמה כדאי לסמוך על התוצאות. רוב המדדים הקיימים משתמשים בתשובות ממחיפוש במסד נתונים, מה שמטשטש את הגבול בין שתי השיטות ועלול להסתיר שגיאות. DiNovo מציגה שיטת בדיקת איכות שונה שנקראת מיפוי יעד-דצוי (target-decoy mapping). כאן, הפפטידים שנקראו לאחרונה ממופים לאוסף משולב של רצפים אמיתיים (יעד) ורצפים מלאכותיים, ממוינים (דצויים). על ידי השוואת כמה פעמים פפטידים נופלים בקבוצת האמיתיים לעומת הקבוצה הממוינת, התוכנה יכולה להעריך שיעור שגיאות, או שיעור גילוי שגוי, בלי להישען על זיהויים קודמים. זה מאפשר להשוות את DiNovo ישירות לתוכניות חיפוש מסדי נתונים סטנדרטיות תחת אותן בקרות שגיאה.
מה DiNovo מספק בפועל
במבחנים על דגימות מבקטריה, שמרים ונוגדנים, DiNovo קראה בעקביות הרבה יותר פפטידים וחומצות אמינו מאשר כלים ידועים de novo המשתמשים באנזים יחיד. בשימוש בשני זוגות מראה, היא הניבה 2–3 פעמים יותר חומצות אמינו באמינות גבוהה מאשר תצורת טריפסין בלבד וזיהתה יותר חלבונים ברמות שגיאה דומות. כאשר השוו אותה ישירות לשלושה מנועי חיפוש מסדי נתונים מובילים, DiNovo מצאה מספרים דומים של חומצות אמינו וחלבונים, ורוב הרצפים שלה תאמו לאלה שמצאו מנועי החיפוש על אותן ספקטרות. המחברים טוענים שרמת כיסוי וההסכמה הזו משמעותית כי ריצוף de novo, שפעם נחשב לשיטת גיבוי, יכול כעת לעמוד לצד חיפוש במסדי נתונים כאופציה רצינית, ובמקרים מסוימים עדיפה.
מבט כולל: לקראת קריאה מלאה וללא הטיה של חלבונים
ללא מומחיות מיוחדת, המסקנה היא ש-DiNovo מקל משמעותית את קריאת מקטעי החלבון בצורה מדויקת מבלי להיות מוגבל למה שכבר קיים במסדי נתונים רפרנסיים. על ידי הכפלה או שלשול כמות המידע הרצפי הנתמך היטב וסיפוק בדיקות שגיאה משולבות, הגישה הזו פותחת את הדלת לגילוי חלבונים לא מוכרים, מעקב אחר וריאציות עדינות וחקירת תערובות מורכבות שבהן מרכיבים רבים עדיין לא ידועים. בקיצור, על ידי צימוד אנזימי מראה עם למידת עומק וסטטיסטיקה קפדנית, DiNovo מסייעת להפוך עקבות ספקטרליים רועשים לתמונה בהירה ואמינה יותר של החלבונים שמאחורי הבריאות והמחלה.
ציטוט: Cao, Z., Peng, X., Zhang, D. et al. DiNovo enables high-coverage and high-confidence de novo peptide sequencing via mirror proteases and deep learning. Nat Commun 17, 2203 (2026). https://doi.org/10.1038/s41467-026-70224-6
מילות מפתח: פרוטאומיקה, ריצוף פפטידים de novo, ספקטרומטריית מסה, למידת עומק, פרוטאזות מראה