Clear Sky Science · he
מולטי-אומיקס בתא בודד חושף ציר אנדותליאלי רגיש-מכנית PIEZO1-IL-33 המניע פיברוזיס ריאתי
מדוע ריאות קשות חשובות
פיברוזיס ריאתי הוא מצב הרסני שבו שקיות האוויר שהיו גמישות הופכות בהדרגה לרקמת צלקת נוקשה, מה שהופך כל נשימה למאמץ. כיום הרופאים יכולים רק להאט את ההתקדמות של המחלה, אך לא לעצור או להפוך אותה. המחקר הזה שואל שאלה שנראית פשוטה אך בעלת משמעות רחבה: כיצד התאים המצפים את כלי הדם בריאה חשים שהרקמה שסביבם הפכה לקשה באופן חריג, וכיצד תחושה זו מומרת ליותר הצטלקות? באמצעות מעקב אחר שרשרת האירועים עד לרמה של תאים בודדים והגנים היחידים, החוקרים חושפים "מתג" מכני בכלי הדם שעשוי להיות ניתן ליעד תרופתי.
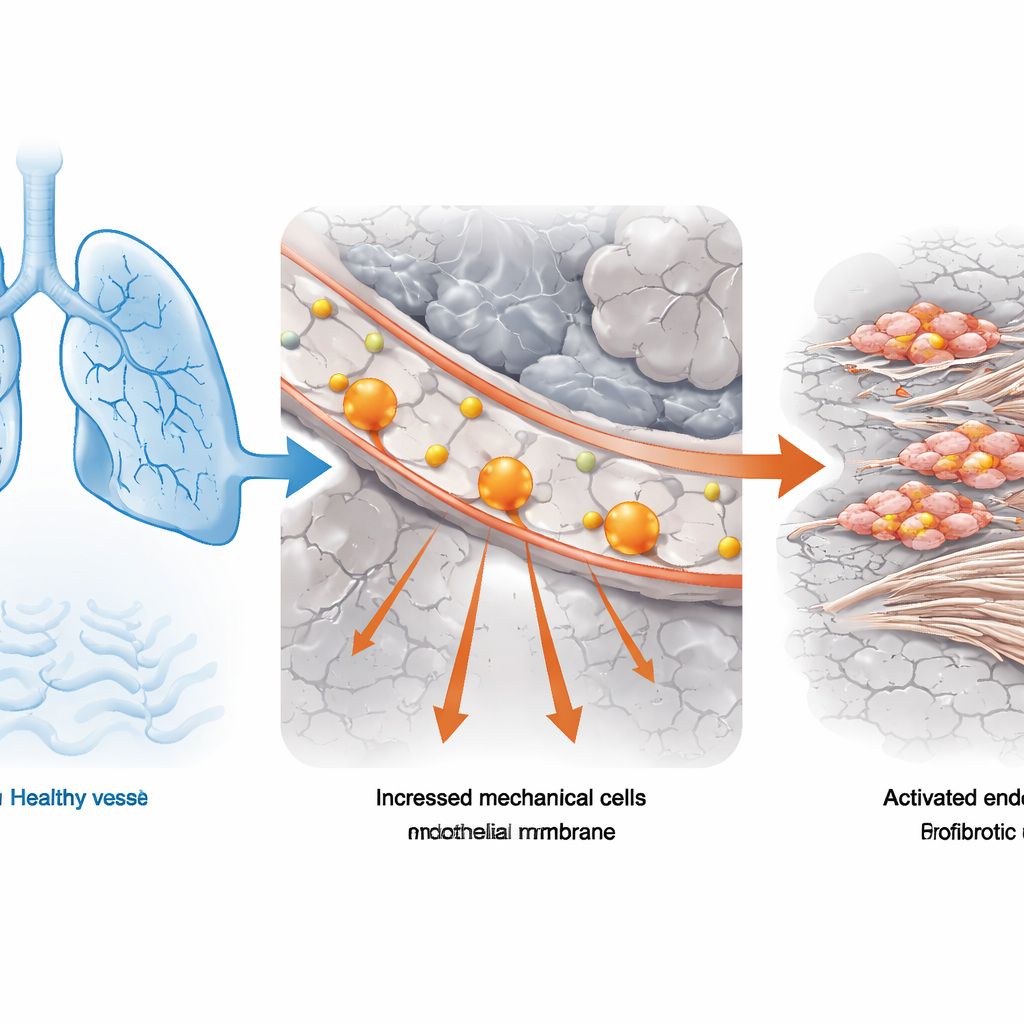
מבדיקות תפקוד ריאה לתאים בודדים
הצוות התחיל מרקמות ריאה של אנשים עם פיברוזיס ריאתי אידיופתי, הצורה השכיחה ביותר של המחלה, ומתורמים עם ריאות תקינות. הם שילבו מדידות סטנדרטיות של תפקוד ריאה (כמה אוויר אדם יכול לנשוף בכוח) עם ריצוף RNA בתא בודד עוצמתי, שמגלה אילו גנים פועלים באלפי תאים פרטניים. באמצעות כלי חישובי שמקשר נתונים קליניים ברמת האוכלוסייה עם פרופילי תא בודד, הם זיהו אילו סוגי תאים היו קשורים יותר לירידה החמורה בתפקוד הריאה. תאי האנדותל הווסקולאריים — התאים היוצרים את הציפוי הפנימי של כלי הדם — בלטו כהועשרו במיוחד אצל מטופלים שקיבולת הריאה שלהם הייתה פחות מחצי הנורמה. בתאים אלו, תוכניות גנטיות הקשורות ל"לחץ מכני" היו באופן עקבי מוקטבות, מה שמרמז שכוחות פיזיקליים חריגים היו חלק מהבעיה.
לחץ מכני כגורם נסתר
כדי לבדוק האם הקשר בין חישה של לחץ ומחלה הוא כללי, החוקרים פנו לשני מודלים עכבריים של הצטלקות ריאה: אחד הושרה על-ידי סם הכימותרפיה בליאומיצין, והשני על-ידי חשיפה ממושכת לאבק סיליקה, סיכון תעסוקתי מוכר. באמצעות שיטות תא־בודד על ריאות ניסיוניות אלו, הם שוב מצאו שתאי האנדותל נשאו חתימות ברורות של לחץ מכני מוגבר. בשני המודלים, כאשר רקמת הריאה שסביבה התעבה והתקשתה, הציפוי של כלי הדם נראה כשיורד למצב בלתי מסתגל. ההתכנסות הזו בין מדגמי אנוש למודלים בעלי חיים חיזקה את הרעיון שכוחות פיזיקליים מעוותים בריאה—ולא רק דלקת או פעילות חיסונית—מהווים גורם מרכזי בהתפתחות והתקדמות הפיברוזיס.
חושן לחץ בעל תפקיד קריטי
בהעמקה, הצוות חיפש "חושני מכניקה" ספציפיים — חלבונים שממירים מתיחה פיזית לאותות ביוכימיים — שהיו מובהקים בתאי אנדותל לוחצים. חלבון תעלת יונים אחד, הקרוי PIEZO1, הופיע שוב ושוב כחשוד המרכזי. הן בעכברים והן בבני אדם עם פיברוזיס, רמות PIEZO1 היו גבוהות באופן ניכר בתאי האנדותל הווסקולאריים לעומת בריאים. כאשר החוקרים הנדסו עכברים שבהם PIEZO1 הוסר רק באנדותל, בעלי החיים הראו עמידות רבה יותר להצטלקות ריאה המושרה על-ידי בליאומיצין: היה פחות הצטברות קולגן, פחות תאים פעילים היוצרים צלקת ורמות נמוכות יותר של סימן כימי לפיברוזיס. חסימה פרמקולוגית של PIEZO1 באמצעות מעכב פפטידי גם הקלה על ההצטלקות, בעוד שהפעלתו החריפה את הפיברוזיס—אלא אם הקולטן נעדר מתאי האנדותל. יחד, הניסויים הללו הראו כי PIEZO1 בתאי ציפוי כלי הדם אינו רק צופה מהצד אלא מניע הכרחי של המחלה.
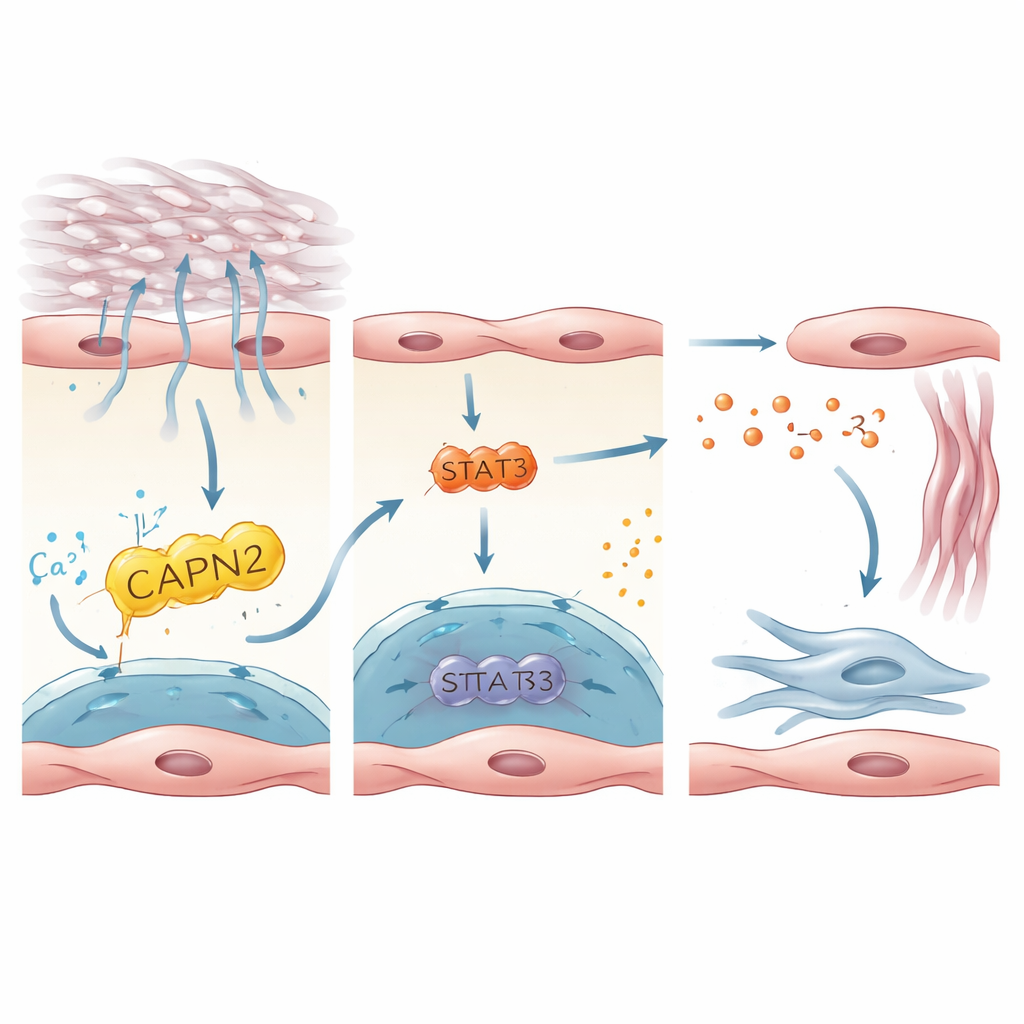
שרשרת איתות שמעירה תאי יוצרי צלקת
המחקר אז עקב כיצד הפעלת PIEZO1 בתוך תאי האנדותל מתורגמת לאותות שמעירים פיברובלסטים, התאים שמפרישים רקמת צלקת. באמצעות שילוב של מערכי נתונים אנושיים ועכבריים, המחברים התמקמו באינטרלוקין‑33 (IL‑33), חלבון קטן שמשתחרר על-ידי תאים תחת לחץ או ניזוקים, כשליח מרכזי. IL‑33 הובע בחוזקה בתאי אנדותל חיוביים ל‑PIEZO1 והיה מוגבר בריאות ממטופלים ולעכברים עם פיברוזיס. בתאי אנדותל אנושיים תרביים שגודלו על מצעים קשיחים או נמתחו כדי לדמות נשימה כנגד ריאה נוקשה, הפעלת PIEZO1 הגברה את ייצור IL‑33. זה תלוי באנזים מטה־זרם, CAPN2, ובגורם שעתוק, STAT3, שהכוונו ביחד את פעילות גן IL‑33. בעכברים, מחיקה של IL‑33 באופן ספציפי בתאי אנדותל הגנה מפני פיברוזיס, בעוד שכפיית ייצור גבוה של IL‑33 בתאי האנדותל מחקה את האפקט המגן של חסר PIEZO1. תוצאות אלה מתארות ציר ליניארי: לחץ מכני → PIEZO1 → CAPN2/STAT3 → IL‑33 → הפעלת פיברובלסטים והצטלקות.
מה המשמעות לטיפולים עתידיים
ללא‑מומחים, המסר הוא שפיברוזיס ריאתי לא מונע רק על-ידי תאי חיסון סוררים; זו גם מחלה של "מגע" לקוי בכלי הדם. תאי האנדותל חשים שסביבתם התקשתה, מפעלים את מתג ה‑PIEZO1 ובתגובה משחררים IL‑33, אות סכנה שמעודד פיברובלסטים סמוכים להמשיך להניח צלקת. באמצעות פירוק שרשרת זו מהכוח המכני לביטוי הגנים, העבודה מדגישה כמה יעדים מבטיחים—PIEZO1 עצמו, מצע CAPN2‑STAT3, ו‑IL‑33—לטיפולים שמטרתם לשבור את המעגל המעצים של נוקשות והצטלקות. בעוד שנדרשים עוד מחקרים כדי למתן בבטחה מסלולים אלו בבני אדם, הציר האנדותליאלי הרגיש‑מכני הזה מציע זווית חדשה, מבוססת פיזיקה, להתמודדות עם מחלה שהתנגדה זמן רב לטיפולים יעילים.
ציטוט: Zhang, L., Gui, X., Hou, R. et al. Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis. Nat Commun 17, 2655 (2026). https://doi.org/10.1038/s41467-026-70193-w
מילות מפתח: פיברוזיס ריאתי, תאי אנדותל, מכנוטרנסדוקציה, PIEZO1, IL-33