Clear Sky Science · he
ההרכבה הקוולנטית של חרב בת־הפעולה בביוסינתזה של פוסטריצין כוללת מלונילציה-לקטוניזציה על ידי תיאואסטרז דו-תפקודי ודמַלונילציה אנזימטית
כיצד הטבע בונה "חרב" כימית זעירה
תרופות נגד סרטן ואנטיביוטיקות לעתים קרובות תלויות בכמה אטומים המסודרים בדיוק כך — "חרב" זעירה שננעלת על חלבון ומכבה אותו. החומר הטבעי פוסטריצין הוא מולקולה כזו, בעלת פעילות חזקה נגד אנזימים המעורבים בצמיחת תאים. אך המבנה המורכב שלה מקשה על ייצור או שינוי במעבדה. המחקר הזה חושף, שלב אחר שלב, כיצד חיידקים מרכיבים את החרב הקריטית של הפוסטריצין, וחושף תכסיסים אנזימטיים שכימאים יכולים להעתיק לעיצוב תרופות חדשות.
החסם המיוחד בתרופות טבעיות עוצמתיות
רבות מהתרופות המבטיחות שמקורן בחיידקי הקרקע שייכות למשפחה הקרויה פוליקטידים. בתוך משפחה זו קבוצה אחת נושאת טבעת פעילה וריאקטיבית, שמכונה על ידי כימאים δ-לקטון α,β-בלתי רוויה, הפועלת כמו וו מולקולרי. היא יכולה ליצור קשר קוולנטי קבוע עם חומצות אמינו מסוימות בחלבונים, ולכבות מתגים ביולוגיים מרכזיים. בפוסטריצין ובמולקולות קרובות לכך, הוו משולב עם קבוצת פוספט המסייעת למולקולה לכוון לאנזימים ספציפיים השולטים בחלוקת התא. תכונות אלה הופכות אותן למועמדות מבטיחות נגד סרטן, אך אותו ריאקטיביות ומורכבות מבנית מקשות על הסינתזה ועל היציבות באחסון.
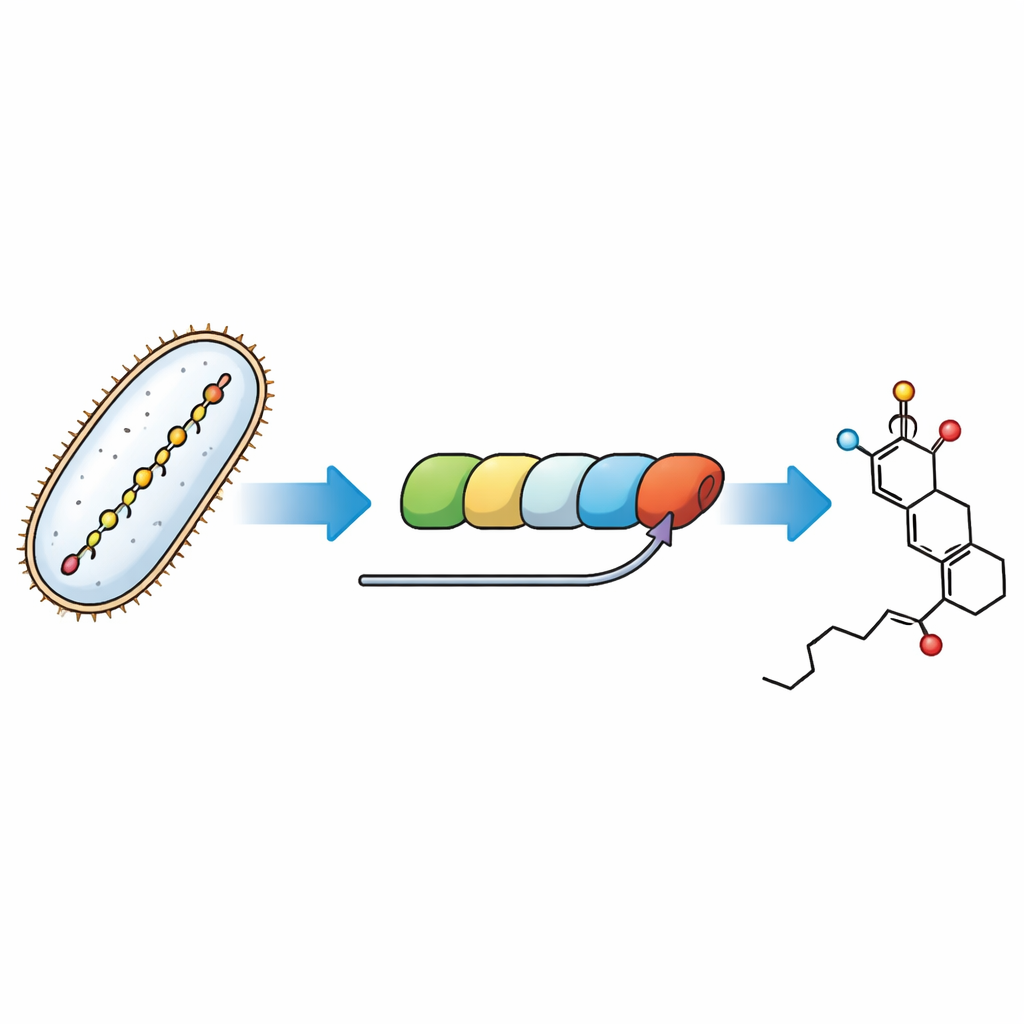
מעקב אחר השלבים הסופיים של פס ייצור מולקולרי
חיידקים בונים את הפוסטריצין באמצעות מכונה חלבונית מודולרית עצומה הנקראת פוליקטיד סינתאז — פס ייצור שבו כל תחנה מאריכה ומעצבת שרשרת פחמן גדלה. הפאזל שבדקנו כאן הוא כיצד המודול האחרון במכונה זו יוצר את טבעת ה"חרב" ומתקין "יד" זמנית בשם קבוצת מלוניל שצריך אחר כך להסיר. על ידי שיחזור מסלול זה בבקבוקים עם אנזימים מזוקקים וחיקויים מולקולריים קטנים שמדמים את הביניים הטבעיים, החוקרים יכלו לצפות בשלבים בודדים ולהקצות אותם לחלקים ספציפיים של פס הייצור.
אנזים מרובה-מטלות עם כישרון לא צפוי
הצוות גילה שהתחנה האחרונה בפס הייצור, דומיין בשם FosTE, מתנהגת בצורה שלא נצפתה קודם. גרסאות טיפוסיות של הדומיין הזה פשוט מקצצות מוצרים גמורים מהפס. FosTE, לעומת זאת, תופס תחילה שבר מלוניל מבלוק בניין תאי שכיח ומעבירה אותו לאתר חמצן מדויק בשרשרת המתפתחת, ואז מסייע לשרשרת להתקפל ולהיסגר לטבעת ה"חרב". שינוי חומצת אמינו סרין תגובתית אחת ב-FosTE משבית את שתי הפעילויות. מודל מבני מצביע על שני שארגינינים טעונים חיובית באתר הפעיל שמחבקים את שבר המלוניל וממקמים אותו להעברה — פונקציות שבדרך כלל מטפל סוג אחר של אנזים. החלפת שארגינינים אלה בחומצות נייטרליות ממחיקה את שלב העברת המלוניל תוך השארת יצירת הטבעת על פי רוב שלמה, מה שמעיד על תפקידם החיוני.
עיגון ה"חרב" ומניעת בזבוז
לאחר שהטבעת נוצרה ונושאת את קבוצת המלוניל הזמנית, אנזים נוסף, FosM, חייב להסיר קבוצה זו כדי לחשוף את ה"חרב" החמושה במלואה. המחקר מראה ש-FosM פועל ביעילות רק לאחר אנזים נוסף, קינאז רחב-ספציפיות בשם FosH, מוסיף פוספט למיקום סמוך על המולקולה. כשהחוקרים סיפקו את הטבעת המלונילית ל-FosM לבדו, התרחשה המרה מתונה בלבד. הוספת FosH תחילה הובילה להסרה כמעט מלאה של קבוצת המלוניל וליצירת היחידה התגובתית הסופית. חשוב לציין ש-FosH יכול גם לפוספוריל מטבולים "שונים" שנוצרים מתגובות צדדיות, ולייצבם כך כדי שיוכלו להיות מעובדים כראוי במקום ללכת לאיבוד כמוצרי סיום חסרי תועלת.
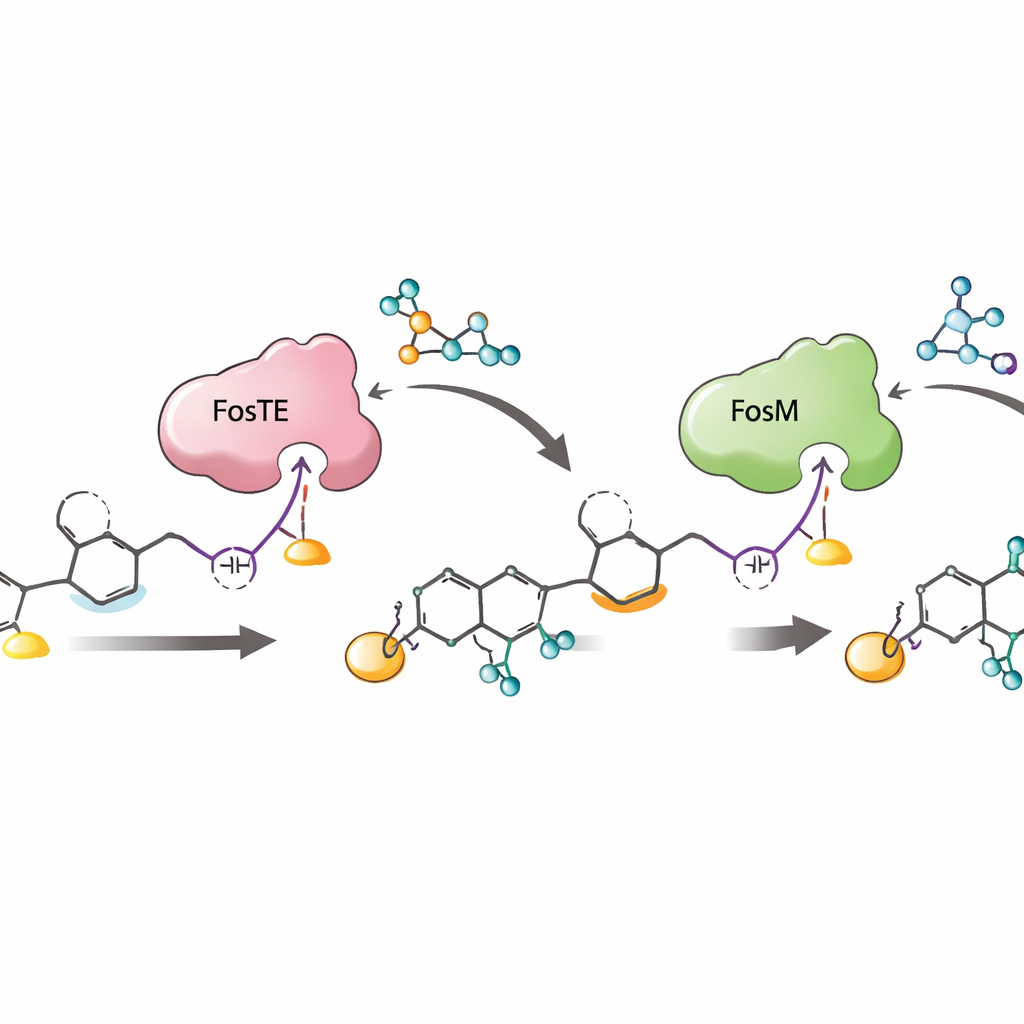
מדוע הכוריאוגרפיה האנזימטית הזו חשובה
ביחד, העבודה חושפת רצף מתוזמר בקפידה: הארכת השרשרת על פס הייצור, הוספת מלוניל וסגירת טבעת מונעות על ידי FosTE, פוספורילציה על ידי FosH, ולבסוף הסרת המלוניל מונעת על ידי FosM. הסדר הזה לא רק בונה את ה"חרב" העדינה ביעילות, אלא גם מגן על הביניים הבלתי יציבים מפירוק וממקסם את הייצור של הצורה המפוספטת הרצויה שהיא הפעילה ביותר כמוביל תרופתי. על ידי חשיפת האופן שבו דומיין אנזימטי יחיד יכול גם לקשט וגם לשחרר מולקולה גדלה — וכיצד אנזימים שותפים מכווננים ומצילים ביניים ריאקטיביים — המחקר מציע שרטוט למהנדסים ליצירת פוליקטידים נושאי-חרב חדשים ולבניית מסלולי סינתזה קצרים ויעילים יותר לסוכנים אנטי-סרטניים מורכבים כמו פוסטריצין.
ציטוט: Nguyen, L.N.K.T., Schlotte, L., Hoffmann, J. et al. Covalent warhead assembly in fostriecin biosynthesis involves malonylation-lactonisation by a bifunctional thioesterase and enzymatic demalonylation. Nat Commun 17, 2365 (2026). https://doi.org/10.1038/s41467-026-70144-5
מילות מפתח: פוסטריצין, ביוסינתזה של פוליקטידים, הנדסת אנזימים, חרבות מוצרים טבעיים, סינתזה כימואנזימטית