Clear Sky Science · he
ויסות תרגום על ידי דסולפורציה חמצונית של מודיפיקציות tRNA
איך תאים מכוונים את ייצור החלבונים תחת לחץ
כל תא חייב להחליט אילו חלבונים לייצר, בקצב כמה ומהו הזמן שבו להאט. המחקר הזה מגלה מתג כימי עדין על מולקולות ה-transfer RNA (tRNA) שעוזר לתאים להוריד את קצב ייצור החלבון כאשר סביבת התא נעשית יותר מחמצנת, למשל בזמן דלקת או לחץ מטבולי. על ידי מעקב אחרי התנהגות המתג בתאים יונקים ובמערכות מבחנה, החוקרים חושפים מנגנון חדש שבו שינויים דמויי-נזק ב-RNA יכולים לשמש כאות רגולטורי.
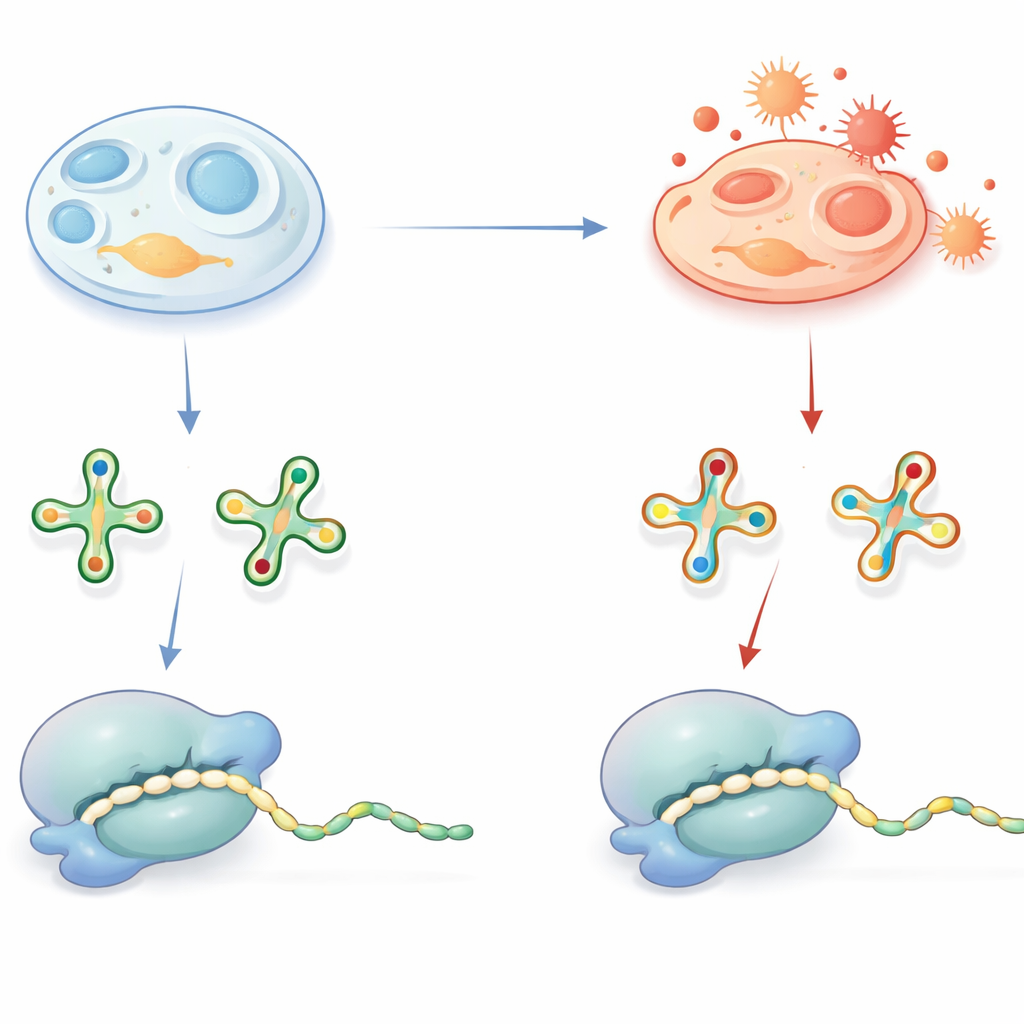
סימנים קטנים על tRNA עם השלכות גדולות
tRNA פועלים כאדפטורים שקוראים “מילים” בת שלוש אותיות ב-mRNA ומספקים את חומצות האמינו המתאימות במהלך סינתזת החלבון. כדי למלא את תפקיד זה בדיוק וביעילות, רבים מה-tRNA נושאים קישוטים כימיים מיוחדים, במיוחד בעמדה מפתח שמקושרת לאות השלישית של כל קודון. קישוט נפוץ אחד הוא קבוצה המכילה גופרית על בסיס יורידין, לעתים מסומנת כנגזרת 2-thiouridine. בתנאים בריאים הקבוצה הזו מסייעת ל-tRNA לזהות קודונים שמסתיימים ב-A או ב-G ותומכת בתרגום מהיר וללא שגיאות. פגמים בקישוטים אלה ידועים כבר שגורמים למחלות אנושיות, מה שמדגיש את חשיבותם.
כאשר לחץ חמצוני מחדש כותב את ה-tRNA
לקבוצת הגופרית שמגבירה את הדקודינג יש גם חסרון: היא פגיעה כימית לחמצון. הצוות שאל האם בתוך תאים הקבוצה הזו באמת מוסרת בתנאים מחמצנים, ומה יהיו ההשלכות על סינתזת החלבון. באמצעות ספקטרומטרית מסה רגישה הם זיהו גרסאות מחומצנות וחסרות גופרית של בסיסי ה-tRNA — שנקראות נגזרות h2U — ברקמות עכבר, במיטוכונדריה של חזיר, בחיידקים, בשמרים ובשורות תאים אנושיות שונות. ניסוי חכם של spike-in עם מעקב אחרי tRNA חיידקי הראה שהסימנים h2U אינם ארטיפקטים שנוצרו במהלך הכנת הדגימה אלא נוצרים בתוך תאים חיים. אף שהגרסאות המחומצנות היו רק בחלק מן ה-tRNA, השכיחות שלהן השתנתה בין רקמות וסוגי תאים, מה שמרמז כי מצב הרדווקס התאי ויכולת הנוגדי חמצון משפיעים על תדירות ההמרה הזו.
איך tRNA מחומצנים מאיטים את פס הייצור
החוקרים בחנו לאחר מכן כיצד tRNA השונים מתפקדים במהלך סינתזת החלבון. הם המירו כימית את הצורה המכילה גופרית לצורת h2U מחומצנת ב-tRNA כולל והשתמשו במערכת תרגום אנושית מאופסת במבחנה. חלבון מדווח שהייצור שלו תלוי במידה רבה ב-tRNA הממועדים למודיפיקציות האלה הראה ירידה חדה ביצירה כשה-tRNA עברו דסולפורציה, בעוד חלבון בקרה שמימנע שימוש בקודונים מושפעים תורגם כרגיל. בדיקות ביוכימיות חשפו את הסיבה: tRNA מחומצנים ל-ליזין, גלוטמין וגלוטמט טענו בחומצות האמינו שלהם הרבה פחות ביעילות, בעוד tRNA המתאימים לארגינין נשארו במידה רבה בלתי מושפעים. באופן חשוב, tRNA הנושאים h2U עדיין הופיעו בפרקי ריבוזומים קשורים (פוליסומים) מתוך תאים, מה שמעיד שהם משתתפים בתרגום אך עושים זאת ביעילות נמוכה.
מבט מבני על דקודינג מוחלש
כדי לראות בדיוק כיצד החמצון משנה את הדקודינג, הצוות השתמש במיקרוסקופ אלקטרונים קפוא-טמפרטורה ברזולוציה גבוהה כדי להדמות ריבוזומים חיידקיים המתוכנתים עם tRNA ליזין אנושי וקודונים ספציפיים. במצב הנורמלי, המכיל גופרית, הבסיס הממוטל בעמדת ה“וובּל” של ה-tRNA קשר או זוג בסיסים סטנדרטי עם קודון שמסתיים ב-A או זוג וובּל מיוחד עם קודון שמסתיים ב-G, שניהם מושקעים היטב במרכז הדקודינג של הריבוזום. לאחר דסולפורציה, אותו בסיס יכול להקים רק מגע יחיד וחלש עם הקודון שמסתיים ב-A והגה זוג וובּל פחות יציב עם הקודון שמסתיים ב-G. ניסויי קשירה תאמו את המבנים האלה: tRNA ליזין מחומצן כמעט איבד את היכולת לזהות את הקודון AAA וזיהה את הקודון AAG ביעילות מופחתת. יחדיו, הממצאים האלה מראים ששינוי כימי קטן לכאורה יכול לתרגם להאטות תרגום תלויות-קודון.
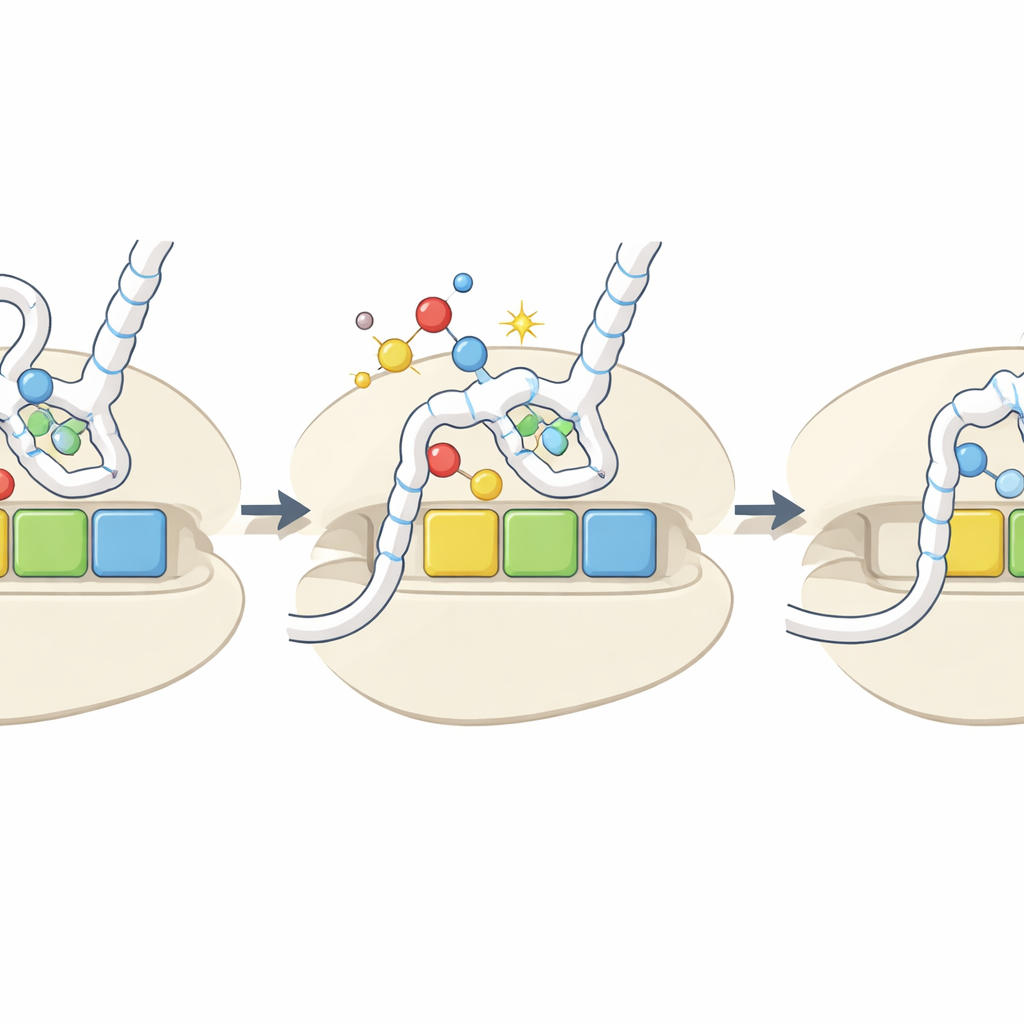
אות נזק שהופך לכפתור רגולציה
בסך הכל, המחקר מציע שהסרת גופרית חמצונית מבסיסי tRNA מרכזיים פועלת כחיישן מובנה למצב הרדווקס התאי. תחת לחץ חמצוני, יותר tRNA מומרות לצורת h2U, אשר טעונות בצורה לקויה וקושרות חלש קודונים מסוימים. זה מאט בצורה סלקטיבית את התרגום באותם קודונים, ובפוטנציאל משנה את יציבות ה-mRNA המושפעים, משנה את קיפול החלבונים ומפעיל מסלולי תגובת-לחץ כאשר ריבוזומים נעצרים. אף על פי שהסימנים המחומצנים יחסית נדירים ורמותיהם לא תמיד עולות בניסויי לחץ, ההשפעות הספציפיות לפי קודון וחומצת אמינו פירושן שגם שינויים צנועים יכולים לעצב אילו חלבונים נוצרים ובאיזה קצב בתנאים מאתגרים.
ציטוט: Mo, Y., Ishiguro, K., Miyauchi, K. et al. Translational regulation by oxidative desulfuration of tRNA modifications. Nat Commun 17, 2125 (2026). https://doi.org/10.1038/s41467-026-70126-7
מילות מפתח: מודיפיקציית tRNA, לחץ חמצוני, סינתזת חלבון, וויסות תרגום, נזק ל-RNA