Clear Sky Science · he
מיקוד בשימוש תלוי-tRNA בטירוזין חושף נקודת תורפה מטבולית בסרטן הכבד ההפטוצלולרית
להרעיב תאים סרטניים ממרכיב בנייה שכיח
תאי סרטן הכבד, כמו כל התאים המתחלקים במהירות, זקוקים לאספקה קבועה של חומצות אמינו — אבני הבניין הקטנות של חלבונים. המחקר הזה מגלה כי קרצינומת תאי הכבד, הצורה הנפוצה ביותר של סרטן הכבד, חשופה לחולשה לא צפויה: היא תלויה במידה רבה בחומצת האמינו טירוזין הן לייצור אנרגיה והן להישרדות. על ידי הגבלה סלקטיבית של אופן השימוש של תאים סרטניים בטירוזין, החוקרים הצליחו להאט את גדילת הגידול, לפגוע בתחנות הכוח של התא ולהפעיל צורת מוות תאי שניתן לנצל לטיפולים חדשים.
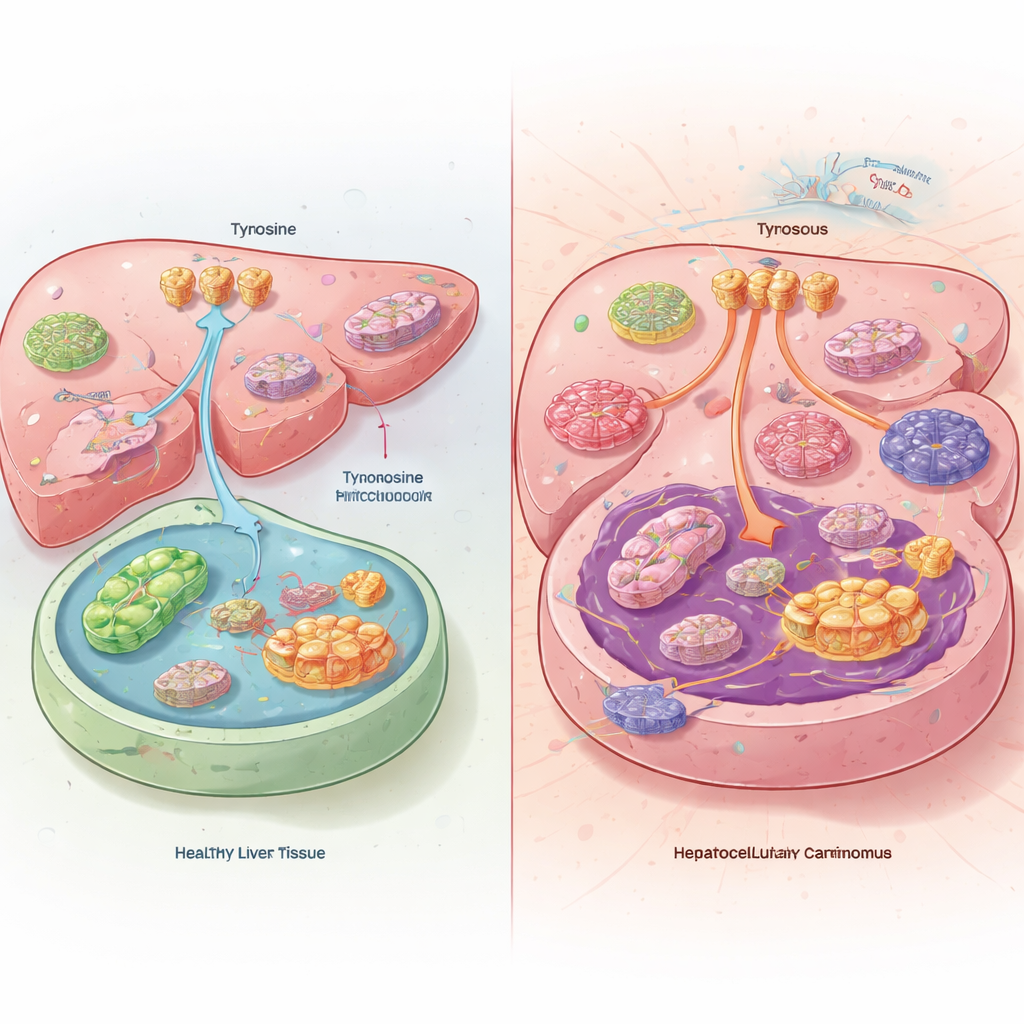
חוסר איזון חבוי בגידולי כבד
כאשר הצוות השווה בין גידולי כבד לרקמת כבד בריאה ממטופלים ועכברים, הוא מצא תופעה תמוהה. בתוך התאים הסרטניים, רמות הטירוזין היו למעשה נמוכות, אף על פי שהגידולים משכו כמות גדולה יותר של טירוזין מהדם ופירקו פחות ממנו. במקום לשרוף טירוזין כדלק, גידולי הכבד הפנו אותו לייצור חלבונים. הסרטנים השיגו זאת על ידי הגברת פעילות הטרנספורטרים של טירוזין בממברנת התא והורדת הפעילות של האנזימים שמפרקים בדרך כלל טירוזין בכבד. עכברים שהוזנו בדיאטה ללא טירוזין פיתחו גידולים קטנים יותר וחיו זמן ארוך יותר, בעוד שטירוזין עודף בתזונה האיץ את גדילתם של הגידולים.
איך הסרטן מחדש את תהליך ייצור החלבון
החוקרים עקבו אחרי רעב הטירוזין הזה עד גן מייצר־סרטן רב־עוצמה בשם MYC. בגידולי כבד, MYC מדליק חלבון שנקרא YARS1, שמצמיד טירוזין ל-tRNA מסוים (tRNA-TyrGUA). ה-tRNA הטעון הזה הוא מה שהריבוזומים צריכים כדי לבנות חלבונים עשירים בטירוזין. המחקר הראה כי סרטן הכבד מגביר הן את YARS1 והן את ה-tRNA התואם לו, ומבטיח צינור מועדף של טירוזין לתרגום חלבונים. שיבוש הצינור הזה — בין אם על ידי הורדת רמות הטירוזין, דיכוי YARS1 או tRNA-TyrGUA, או חסימת העמסת הטירוזין — הפך את תאי סרטן הכבד לפחות עמידים בתרביות ובעכברים, וחשף נקודת תורפה מטבולית שקשורה קשר הדוק לצורכי הייצור החלבוני הגבוהים שלהם.
פגיעה בתחנות הכוח ושיווי משקל השומנים
על ידי שילוב מדידות ברמת הגנום של RNA, ייצור חלבון ומטבוליטים, הצוות זיהה שני מטרות רגישות במיוחד להגבלת טירוזין. האחת, NDUFB8, היא רכיב של קומפלקס I במיטוכונדריה, חלק ליבה במכונת ייצור האנרגיה של התא. השנייה, SCD1, מסייעת להמיר שומנים רוויים לשומנים חד־בלתי רוויים שנוחים יותר לאחסון בממברנות ובטיפות שומניות. כאשר הטירוזין לתרגום הוגבל, הייצור של NDUFB8 ו־SCD1 ירד, בעוד שרמות ה‑RNA שלהם נותרו כמעט ללא שינוי — ראיה ברורה שהמכה נחתה על התרגום, לא על ביטוי הגן. זה הוביל להרכבה לקויה של קומפלקס I, נשימה תאית מופחתת, עודף של ריאקטיביות חמצונית ושינוי בשומנים מצד שומנים חד־בלתי רוויים לכיוון צורות פוליאנסטרטיות עדינות יותר שנוטות לחמצון.
והכריחה את התאים הסרטניים למוות מונע־ברזל
נזק המיטוכונדריה המצטבר ושומנים בלתי יציבים דחקו את תאי סרטן הכבד לעבר פרופרוטוזיס (ferroptosis), צורת מוות תאי התלויה בברזל ומונעת על־ידי פירוק שומנים. הגידולים ניסו להתנגד על ידי הגברה של חוסמי פרופרוטוזיס טבעיים כגון GPX4 ומולקולות קשורות, אך מסך CRISPR רחב היקף הראה כי השבתת מגן אלה הפכה את הגבלת הטירוזין לאלימה עוד יותר. במודלים תאיים ובעכברים, שילוב של אסטרטגיות להגבלת טירוזין עם תרופות המעכבות GPX4 או BCL2 — או עם תרופות קיימות לסרטן הכבד כמו סוראפניב ווניטוקלקס — הניב שליטה חזקה יותר על הגידול, עומס גידולי קטן יותר וחיים ארוכים יותר.
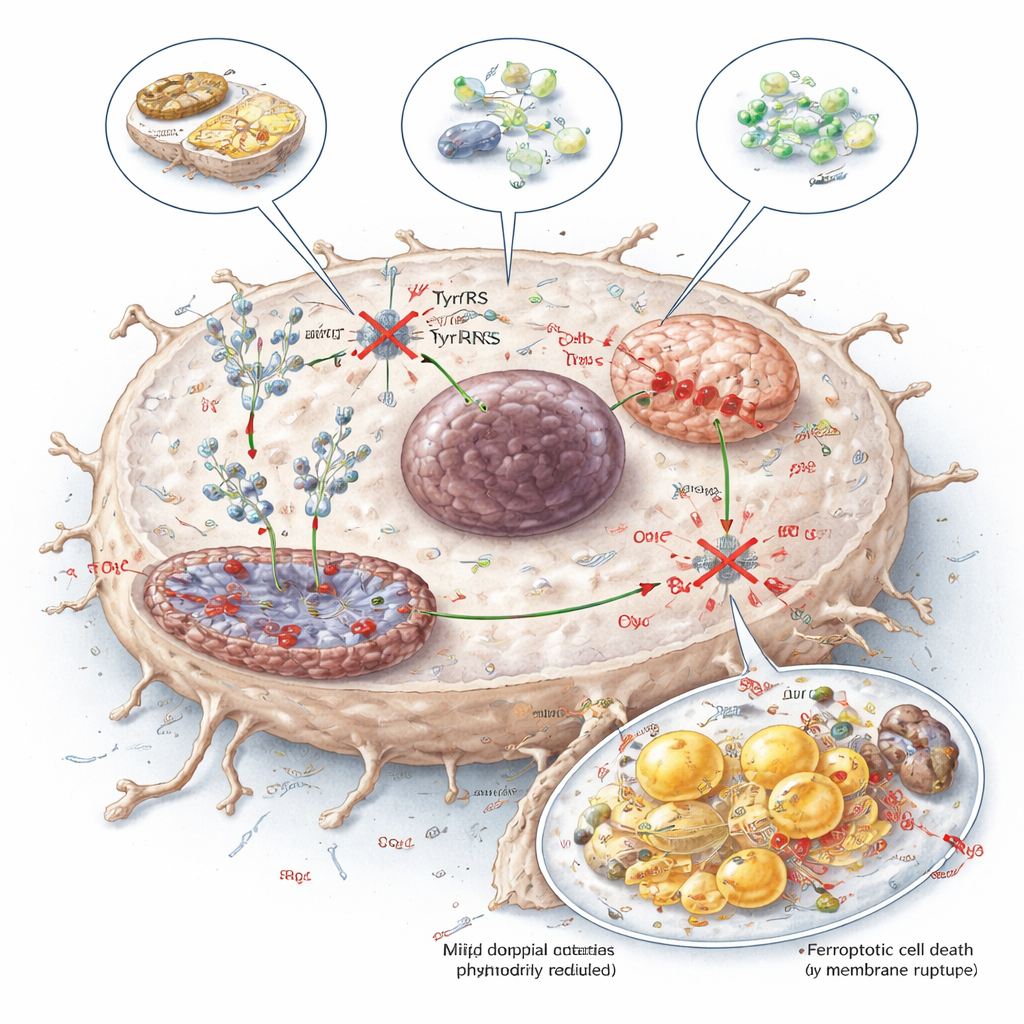
להפוך חולשה מטבולית לטיפול
כדי לבחון דרכים מעשיות לניצול החולשה הזו, החוקרים בדקו שלוש גישות: דיאטה המגבילה טירוזין, אנזים (TAL) שמפרק טירוזין באופן אנזימטי, ומולקולה קטנה בשם טירוזינול המתחרה עם טירוזין על קשירה ל‑YARS1. שלוש הגישות הפחיתו את זמינות הטירוזין לתרגום חלבונים, הורידו את רמות NDUFB8 ו‑SCD1, פגעו בתפקוד המיטוכונדריה והגבירו פרופרוטוזיס בגידולי הכבד, תוך התצוגת השפעות ניתנות לניהול על רקמות נורמליות בעכברים. להדיוט, המסר הוא שסרטני הכבד נדבקים לטירוזין לא רק כמזון, אלא כדלק מדויק למכונת יצירת החלבון שלהם. מיקוד בתלות זו — באמצעות דיאטה, אנזימים או תרופות — מציע דרך מבטיחה להחליש גידולים ולהגביר את השפעת הטיפולים הקיימים.
ציטוט: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
מילות מפתח: סרטן הכבד, מטבוליזם חומצות אמינו, טירוזין, מיטוכונדריה, פרוטאופתוזה/פרופרוטוזה (פרופרוטוזיס)