Clear Sky Science · he
דינמיקה של מולקולה יחידה חושפת שהיקשרות ATP לבדה מזרזת העברת מסלולים על ידי טרנספורטר ABC
למה משאבות קטנטנות בתאים חשובות
כל תא בגופך תלוי במכונות זעירות שמזיזות מולקולות דרך ממברנות, ויוצרות את היסוד לתהליכים כמו קליטת מזון והגנה חיסונית. מחלקה מרכזית של מכונות אלו, שנקראת טרנספורטרים ABC, משתמשת בדלק הכימי של התא — ATP — כדי לדחוף משא אל עבר המדרון, נגד גרדיאנטים טבעיים. ובמשך עשורים מדענים התווכחו על שאלה בסיסית: האם המהלך הפשוט של היקשרות ATP מספק את האנרגיה לצעד ההעברה, או שהאנרגיה משתחררת רק כאשר ATP נשבר? המחקר הזה מתמקד בטרנספורטר יחיד, מולקולה אחר מולקולה, כדי להכריע במחלוקת.
צפייה בטרנספורטר אחד בכל פעם
במקום למדוד את ההתנהגות המשולבת של מיליוני מולקולות, החוקרים בנו מערכת שמאפשרת לעקוב אחרי אירועי העברה בודדים בזמן אמת. הם התמקדו ב-TmrAB, קרוב חיידקי לטרנספורטר האנושי TAP שמעמיס פפטידים חיסוניים לתצוגה בפני תאי T קטלניים. TmrAB יושב בממברנה ומעביר חלקיקונים קצרים של חלבון (פפטידים) מצידה האחד של הממברנה לשני בעזרת ATP. כדי לראות כל צעד העברה, הצוות לכד מולקולת TmrAB בודדת בתוך בועה ממברנלית מלאכותית (ליפוזום) והכניס לתוכה חלבון "חיישן" מהונדס שמחליף את עוצמת הזוהר שלו כשהוא נתפס על פפטיד. באמצעות מיקרוסקופ רגיש מאוד הם יכלו לראות, כקפיצות קצרות באות האור, את הרגעים המדויקים שבהם פפטיד אחרי פפטיד הגיעו לתוך הבועה.
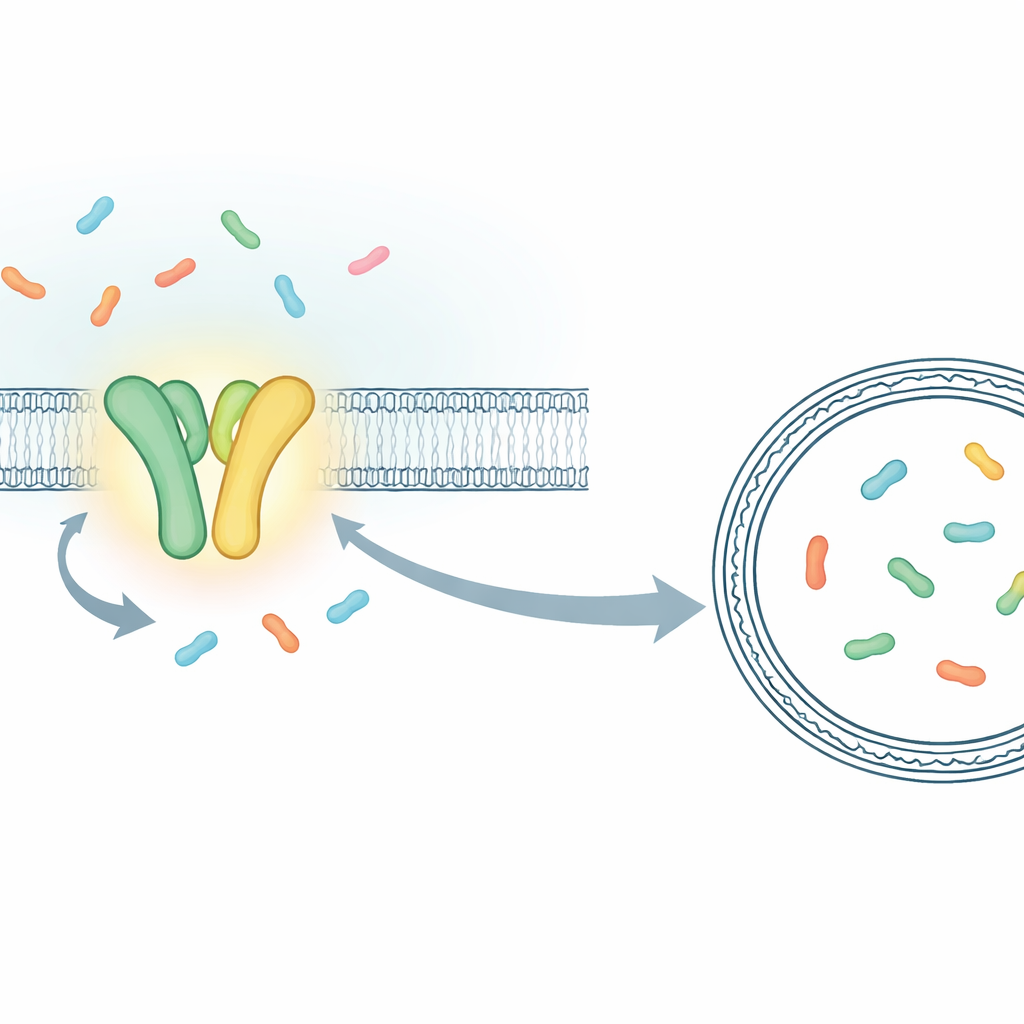
הוכחה שהיקשרות של ATP מזיזה פפטיד אחד
עם המבחן של מולקולה יחידה בידם, החוקרים השוו בין TmrAB רגיל לגרסה מוּדֶּרֶת בעלת קצב מחזור איטי שמותח את המחזורים בזמן. הווריאנט האיטי איפשר להבחין באירועים בודדים שאחרת היו מטושטשים. הם הראו שכאשר ATP ופפטידים היו נוכחים יחד, החיישן בתוך הליפוזום עבר ממצב "ריק" למצב "טעון" בצעדים ישרים, שכל אחד מהם תאם פפטיד יחיד שהועבר. על ידי ניתוח מהירות הסגירה של החיישן סביב הפפטידים והערכת הנפח המיקרוסקופי בתוך כל ליפוזום, הם אפילו יכלו לתרגם את השינויים באור לריכוזים מקורבים של פפטידים. המספרים התאימו למה שציפית אם אחד ואז שני פפטידים יצרמו בבועות בקוטר של כ-100 ננומטר, ואישוש לכך שהם סופרים עכשיו אירועי העברה אחד-אחד.
היקשרות ATP לבדה הופכת את המתג המולקולרי
המחלוקת המרכזית נוגעת ליוני המגנזיום (Mg2+), שלרוב מופיעים יחד עם ATP בתוך תאים וידועים כדרושים לפירוק יעיל של ATP. כמה מודלים הציעו ש-Mg2+ עשוי גם להיות נחוץ להיקשרות ATP או לסגירת הטרנספורטר. כדי להפריד בין התפקידים האלה, החוקרים הסירו Mg2+ באמצעות סוכן כילוי אך עדיין סיפקו ATP. בתנאים אלה, גם הטרנספורטר הרגיל וגם האיטי יכלו לבצע בדיוק צעד העברה אחד של פפטיד לכל מולקולה, ואז נעצרו. התנהגות זו מצביעה על כך ש-ATP עדיין יכול להיקשר ולכפות על הטרנספורטר לעבור ממצב הפונה פנימה למצב הפונה החוצה ולהזיז פפטיד — גם בלי Mg2+. עם זאת, ללא Mg2+ הטרנספורטר אינו יכול לפרק ATP ביעילות, ולכן אינו יכול לאפס את עצמו לסיבוב נוסף.
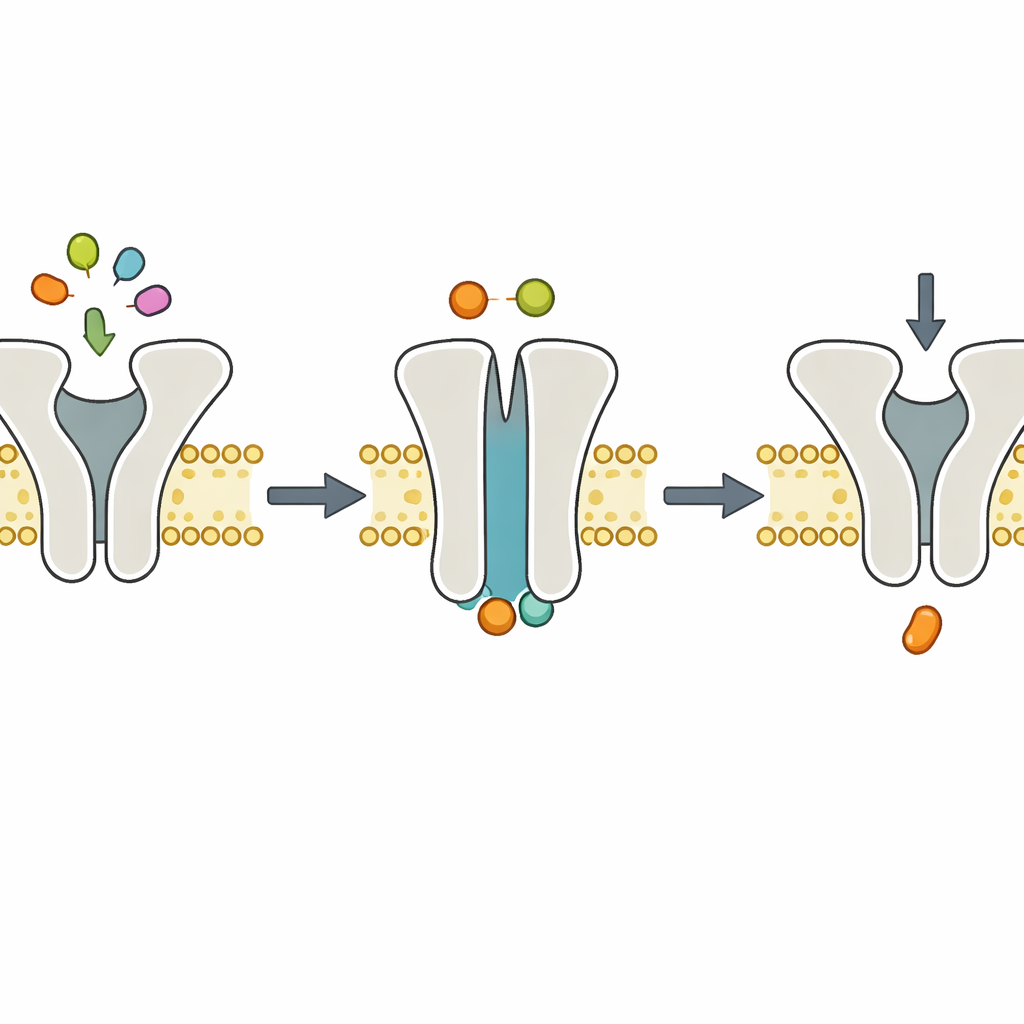
תמונות מבניות תומכות בדינמיקה
כדי לראות כיצד המכונה נראית במהלך הצעד החסר ב-Mg2+, הצוות פנה למיקרוסקופיית אלקטרונים קרים (cryo-EM), שמדמה מולקולות מהקפאה מהירה ברזולוציה קרובה לאטומית. הם השיבו את TmrAB בדיסקים שומניים (nanodiscs), הוסיפו ATP בלי Mg2+ והקפיאו את המורכבים. המבנים שהתקבלו הראו את TmrAB במצב הפונה החוצה, "סגור" (occluded), עם ATP תקוע בשני אתרי ההיקשרות הפנימיים שלו, אך ללא Mg2+ נראה. התמונות הללו היו במידה רבה בלתי ניתנות להבחנה ממבנים קודמים שהופקו בנוכחות ATP ו-Mg2+. יחד עם ניסויים ביוכימיים המראים שפירוק ה-ATP נעצר לחלוטין בלי Mg2+, התמונות תומכות בחלוקה פשוטה של העבודה: היקשרות ATP מעוררת את המעבר הקונפורמציוני שמזיז את הפפטיד, בעוד שפירוק ה-ATP התלוי ב-Mg2+ מבצע את שלב ההתאוששות.
תמונה ברורה יותר של אופן פעולת משאבות תאיות
על ידי צפייה בטרנספורטרים בודדים ופתרון המבנים שלהם, עבודה זו מביאה הכרעה לשאלה וותיקה על טרנספורטרים ABC: מהלך הכח המכנני שמזיז פפטיד מופעל על ידי היקשרות ATP עצמה, לא על ידי השלב הכימי של פירוק ATP בהמשך. Mg2+ נכנס לתמונה בעיקר כדי לאפשר שחבור ה-ATP, שביוזמתו הטרנספורטר נ מנקה ומאופס לעבודה נוספת. מעבר להבהרת פיסת יסוד בב ביולוגיה של התא, הגישה של מולקולה יחידה הזאת מציעה מתווה לניתוח מכונות ממברנליות אחרות התומכות בחיסון, עמידות לתרופות והרבה מחלות — מולקולה אחת וצעד העברה אחד בכל פעם.
ציטוט: Nocker, C., Pečak, M., Nocker, T. et al. Single-molecule dynamics reveal ATP binding alone powers substrate translocation by an ABC transporter. Nat Commun 17, 3038 (2026). https://doi.org/10.1038/s41467-026-70021-1
מילות מפתח: טרנספורטרים ABC, היקשרות ATP, FRET של מולקולה יחידה, העברה ממברנלית, TAP ו-TmrAB