Clear Sky Science · he
ננוחלקיקים של כחול פרוסי שמכוונים למספר מסלולים של PANoptosome-מתווך PANoptosis לטיפול בפגיעת איסכמיה-שיקום שריר הלב
מדוע חשוב להגן על הלב המתחדש
כאשר אדם עובר התקף לב, הרופאים ממהרים לפתוח מחדש את העורק החסום ולהשיב את זרימת הדם. צעד מציל-חיים זה, עם זאת, מגיע עם עלות סמויה: החזרת החמצן הפתאומית עלולה לפגוע בלב בעצמה, לגרום למות תאים ולהניח את היסודות לכשל לבבי. מחקר זה בוחן ננורפואה חדשנית שמטרתה להגן על הלב בזמן חלון פגיע זה על ידי חסימת מספר מסלולי מוות תאים משולבים בבת-אחת, מה שעשוי להוביל להחלמות עדינות יותר לאחר התקף לב.
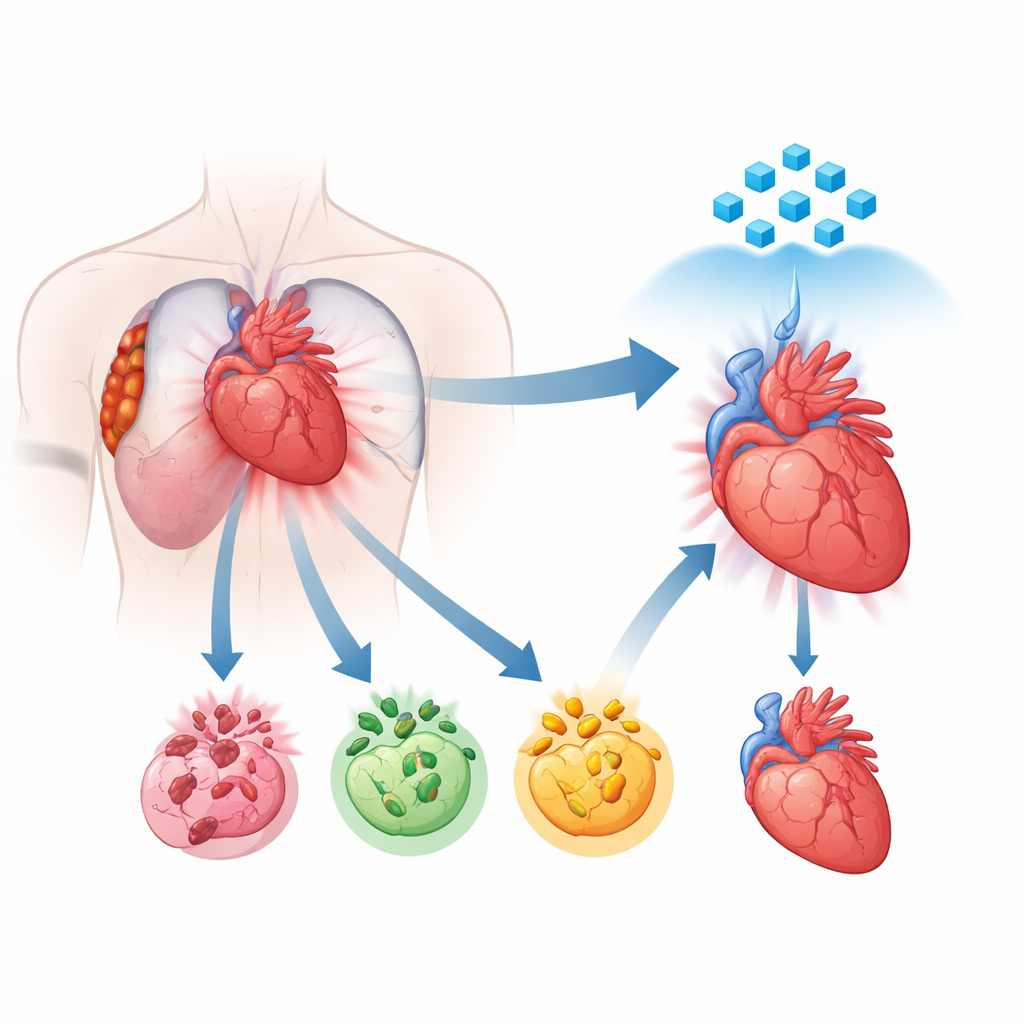
מבט חדש על האופן שבו תאי הלב מתים
במשך שנים מדענים ידעו שתאי לב פגועים יכולים למות דרך מסלולים מתוכנתים שונים, כולל אפופטוזה, נקרופטוזה ופירופטוזה. כל אחד מהם פועל לפי תסריט מולקולרי משלו, אך ראיות גוברות מראות שמסלולים אלה אינם פועלים בנפרד. במקום זאת, הם מתקשרים זה עם זה ויכולים להתמזג לתהליך משולב ובלתי נשלט המכונה PANoptosis. במצב זה מספר תוכניות מוות מופעלות יחד, מה שהופך טיפולים החוסמים רק מסלול אחד לחלשים ומאכזבים. הכותבים השתמשו בסיקוונסינג של RNA גרעיני יחיד מרקמת לב אנושית של מטופלים שעברו התקפי לב לאחרונה כדי למפות היכן ובאיזו עוצמה תוכניות המוות הללו מופעלות. הם מצאו כי באזורים המושפעים ביותר, תאי שריר הלב הראו מעבר חזק לכיוון מצב המוות המשולב הזה, מה שמצביע על PANoptosis כמניע מרכזי של הפגיעה.
עיצוב כלי קטן רב-תכליתי ללב הפגוע
כדי להתמודד עם תהליך כה מורכב, הצוות פנה לכחול פרוסי, תרכובת רפואית מאושרת זה מכבר הידועה בעיקר כנוגדת רעילות לשאיפת מתכות מסוימות. בקנה מידה ננו, חלקיקי כחול פרוסי מתנהגים כמו רובוטים קטנטנים קטליטיים שיכולים לכבות מולקולות מזיקות ולהשפיע על התנהגות תאים. באמצעות סימולציות ממוחשבות הראו החוקרים כי ננוחלקיקים אלה יכולים להתחבר ישירות לשלושה צירי חלבון מרכזיים—RIPK1, ZBP1 ו-AIM2—שמסייעים בהרכבת המכונות המולקולריות של PANoptosis. על ידי קשירה לצירים אלה בדרכים שונות, החלקיקים צפויים להפריע לבניית קומפלקסי המוות המפעילים את שלושת מסלולי המוות התאים.
הכוונת ננוחלקיקים ישירות לרקמת הלב הפגועה
ננוחלקיקים יעילים רק אם הם מגיעים למקום הנכון, לכן הצוות ציפה את חלקיקי כחול פרוסי בממברנות טבעיות שהופרדו מתאי טסיות הדם, התאים שמכוונים לכלי דם פגועים. ציפוי זה יצר PB@PM, נשא ביומימטי שמסתובב כמו טסית אך מוסר מטען תרפויטי. בעכברים שעברו התקף לב מבוקר ופתיחה מחדש של העורק, הדמיה הראתה כי PB@PM הצטבר באופן חזק יותר באזור הלב הפגוע מאשר חלקיקים לא מצופים, בעוד שהסתיר איברים בריאים ברובם. חשוב מכך, החלקיקים המצופים היו נסבלים היטב: בדיקות דם ובדיקות רקמות לא חשפו רעילות ברורה, מה שתומך בפוטנציאל שלהם לפיתוח נוסף.
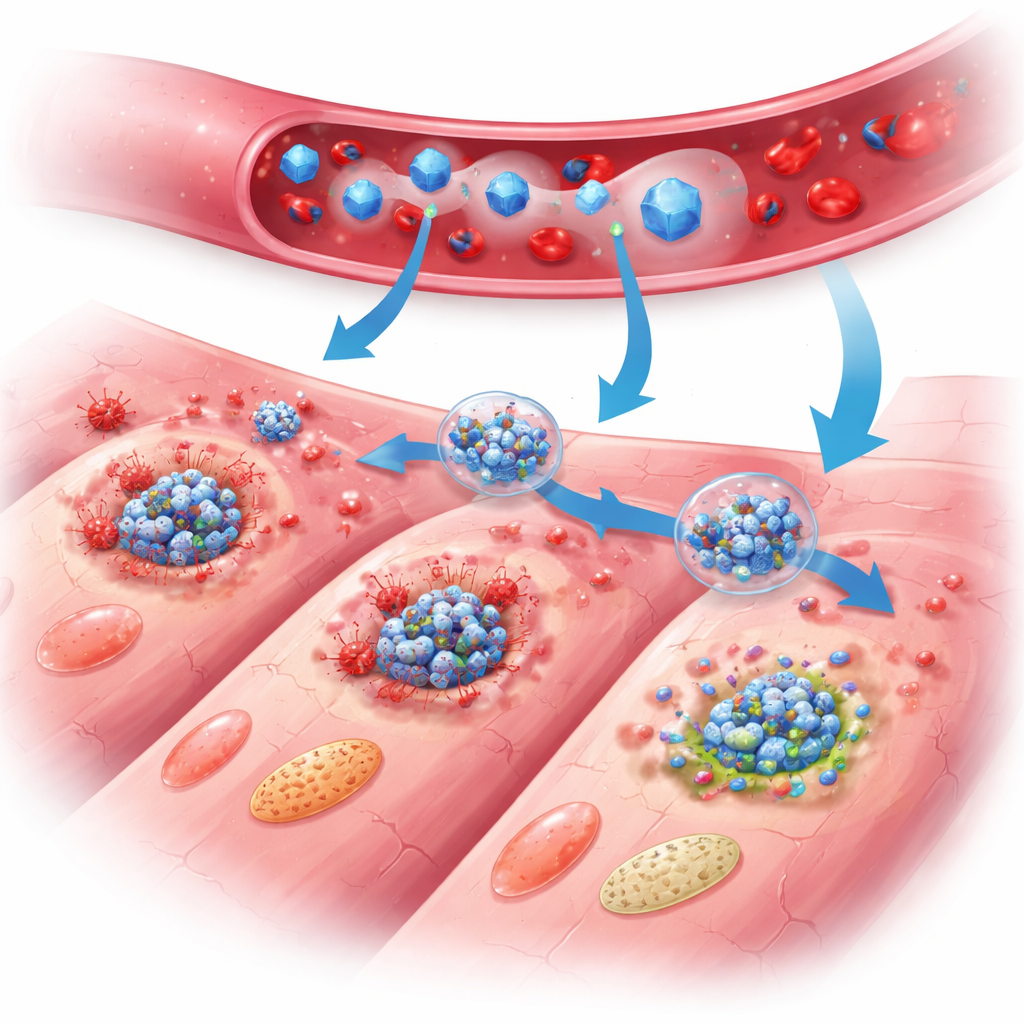
כיצד המגן הננו מגונן על הלב
בעכברים שטופלו, היתרונות של PB@PM נראו בבהירות לאורך ימים ושבועות. תפקוד המשאבה של הלב השתפר, גודל הצלקת הצטמצם וקיר הלב החמיש פחות בהשוואה לחיות שלא טופלו. מחקרי רקמה מפורטים חשפו פחות תאי לב מתים, תאים דלקתיים רגועים יותר ורקמת תיקון ממוסדת טוב יותר עם צמיחת כלי דם בריאה יותר ופחות הגדלה חריגה של תאים ששרדו. ברמה מולקולרית, פרופיל הבעה גנטית נרחב ומדידות חלבון הראו כי PB@PM השתקו בו-זמנית את שלושת מסלולי המוות המתוכננים העיקריים, הפריעו להרכבת קומפלקסי PANoptosis רב-חלבוניים והפחיתו רמות של מולקולות איתות המניעות דלקת. החלקיקים גם קלטו סוגי חמצון תגובתיים מזיקים, יצבו את המיטוכונדריה—תחנות הכוח של התא—ושחזרו מטבוליזם אנרגטי קרוב לנורמה, והסירו טריגרים מרכזיים שהיו דוחפים תאים להרס עצמי.
מה זה עשוי להשפיע על טיפול העתידי בהתקף לב
פשוטו כמשמעו, עבודה זו מראה שננוחלקיק מהונדס בחוכמה יכול לפעול כמגן רב-חוד עבור הלב, מטשטש קשר של אותות מוות הרסניים במקום לרדוף אחר מסלול אחד בכל פעם. על ידי כוונון לרקמת לב פגועה, קשירה לחלבוני בקרה מרכזיים והפחתת סטרס חמצוני ודלקתי, PB@PM הפחית בצורה ניכרת את תגובת השרשרת של אובדן תאים וצלקת שלעיתים קרובות מתרחשת לאחר פתיחת עורק חסום. אמנם נדרש עוד מחקר רחב לפני שאסטרטגיה זו תוכל להגיע לחולים, המחקר מציע הוכחת רעיון שכוונון PANoptosis כמכלול—וביצועו באמצעות חלקיקים חכמים בהשראה ביולוגית—עשוי לפתוח פרק חדש בהגנה על הלב לאחר התקף לב.
ציטוט: Xu, L., Jiang, L., Wu, R. et al. Prussian blue nanoparticles targeting multiple PANoptosome-mediated PANoptosis for myocardial ischemia-reperfusion injury therapy. Nat Commun 17, 2329 (2026). https://doi.org/10.1038/s41467-026-70012-2
מילות מפתח: שיקום איסכמיה של שריר הלב, טיפול בננוחלקיקים, מוות תאי מתוכנת, דלקת לבבית, הגנה מיטוכונדריאלית