Clear Sky Science · he
חיקויי פפטידוגליקן כיראליים פונים למולקולות בניית דופן החיידק להתערבות מול פתוגנים
דרך חדשה לצידת חיידקים מזיקים
זיהומים עמידים לאנטיביוטיקה מתרבים ברחבי העולם, ועדיין חסרים לרופאים כלים שיכולים לזהות ולהתקיף באופן מדויק חיידקים מסוכנים מבלי לפגוע בתאים שלנו. המחקר הזה מציג "פיתיון" מולקולרי מתוחכם המדמה אבנית מפתח בדפנות החיידקים. המולקולות המעוצבות האלה יכולות גם להאיר זיהומים לצורכי דימות וגם לשאת אנטיביוטיקה ישירות למיקרובים, ומציעות אסטרטגיה חדשה להילחם בפתוגנים שקשה לטפל בהם.
חיקוי השריון החיידקי
החיידקים עטופים ברשת חזקה הנקראת דופן תא, הבנויה מסוכרים וחומצות אמינו מיוחדות במראה מראה (אינה-שחזורית) ששאוּתנו כמעט שלא משתמשים בהן. החוקרים ניצלו את ההבדל הזה על ידי יצירת שרשראות ארוכות מבוססות סוכר המעוטרות בצורה מראה ספציפית של אלאנין, חומצת אמינו נפוצה. שרשראות אלו, הקרויות חיקויי פפטידוגליקן כיראליים, תוכננו להידמות במדויק לרכיבים הטבעיים שבהם החיידקים משתמשים לבניית דופנם, אך נעדרות מרקמות יונקים. על-ידי כוונון כמות האלאנין בצורת D שהוספה, הצוות ייצר גרסאות שהיו להן העדפה חזקה לחיידקים על פני תאים אנושיים.
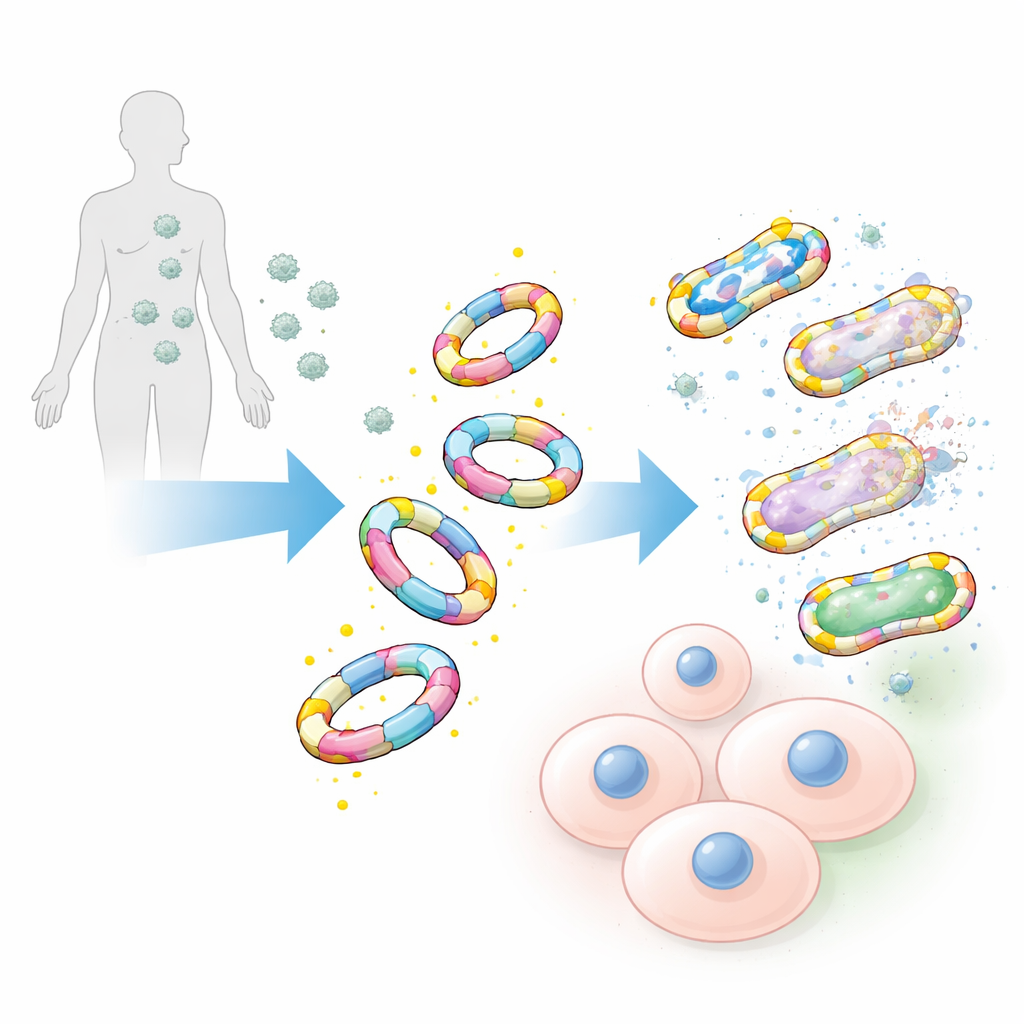
ניקוד לחיידקים, לא לתאים שלנו
בעת בדיקה מול טווח רחב של פתוגנים, כולל זנים בית-חולים ידועים כמו Staphylococcus aureus עמיד למתיצילין וחיידקי ESKAPE אחרים, החיקויים המעוטרים ב-D-אלאנין התחברו למשטחי החיידקים ביעילות מרשימה. מקביליהם במראה הבנויים מצורת L של האלאנין, וכן שרשראות הסוכר המקוריות לבדן, הראו חיבור חלש או כמעט בלתי-מהותי. הצוות גם השווה בין חיקויים גדולים אלה לבין חיפושיות כימיות קטנות מסורתיות המבוססות על מולקולות D-אלאנין בודדות. אפילו כאשר החיפושיות הקטנות הוגברו בעוצמת האיתור שלהן, הן סומנו להרבה פחות חיידקים ונתנו אותות חלשים יותר, מה שמדגיש את כוחו של העיצוב הגדול והחיי-מראה יותר.
חטיפת קו הייצור של בניית הדופן
כדי להבין איך ההכרה הופכת כל כך חזקה, בחנו המדענים כיצד החיקויים מתקשרים עם מכונת הבנייה של דופן התא החיידקי. הם מצאו שהשרשראות המבוססות על D-אלאנין אינן רק נדבקות מבחוץ; הן נקלטות כאילו היו אבני בניין אמיתיות ומוזנות לאותם שלבים אנזימטיים שמחברים בדרך-כלל רכיבי דופן יחד. ניתוח כימי זיהה מולקולות ביניים חדשות שמופיעות רק כשחיקויים אלה קיימים, וסימולציות מחשב הראו שאנזימים מרכזיים בבניית הדופן אוחזים בחיקויים אפילו בחוזקה רבה יותר מאשר בתת-הנירטים הטבעיים. לאורך מספר סבבים של גדילה חיידקית, החיקויים הצטברו בדופן, עיוותו את מבנהו והפכו אותו לדולף.
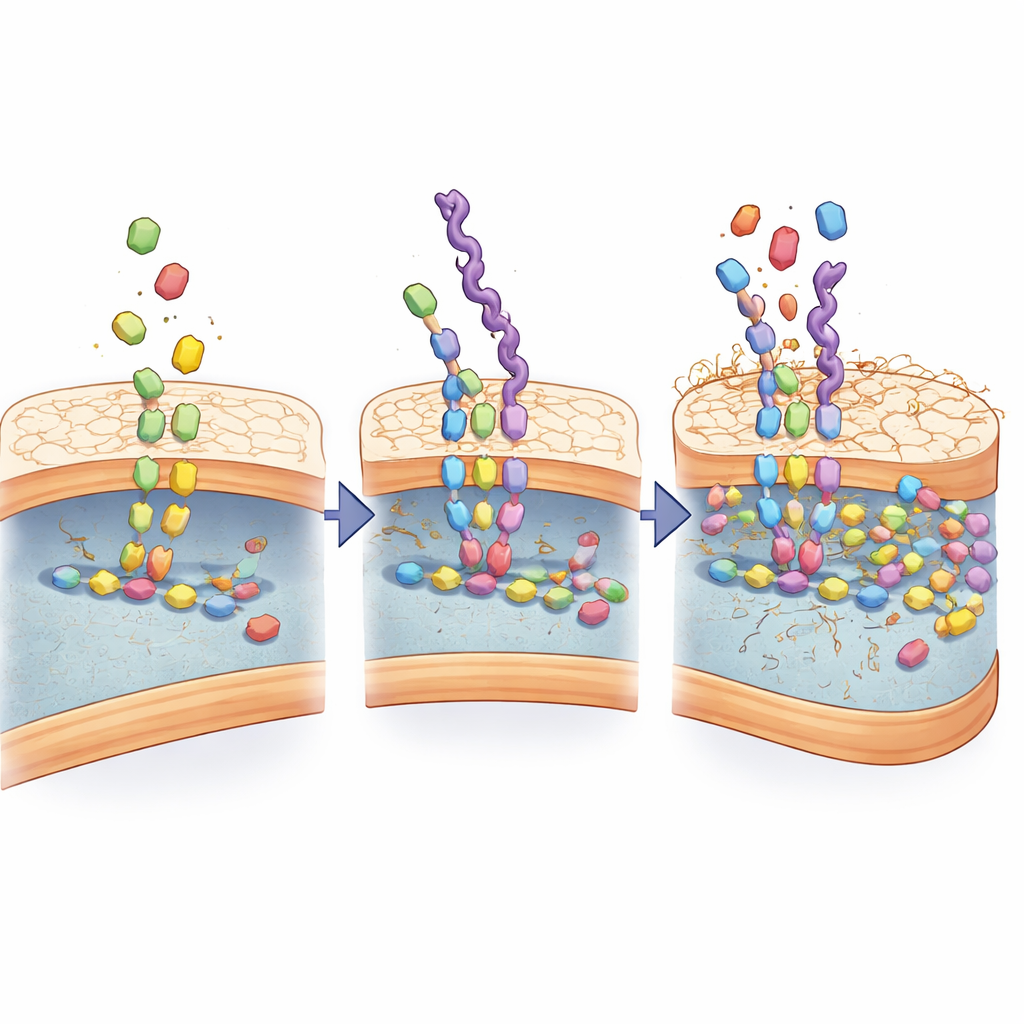
הפיכת החיקויים לנושאי תרופות חכמים
כי השרשראות האלה מצטברות באופן טבעי לחלקיקים זעירים במים ונושאות חיבורים כימיים רבים, הצוות השתמש בהן כסרגלי עבודה לצביעי דימות ואנטיביוטיקה. גרסאות פלואורסצנטיות תיארו בבירור את החיידקים בתרביות תאים, בעוד שהן כמעט שלא התקשרו עם תאים של יונקים שגודלו לצידן. החוקרים אז טעינו את האנטיביוטיקה טטרציקלין בתוך החלקיקים המבוססים על החיקוי. במבחנים במעבדה, האריזה הזאת הפכה את הטטרציקלין ליעיל בכמה מונים, והרגה גם זנים עמידים במינונים נמוכים בהרבה מהתרופה החופשית. מיקרוסקופיה חשפה שחיקויים המטענים אנטיביוטיקה דחסו על החיידקים, חדרו את מעטפותיהם והפעילו מוות תאי נרחב בהשוואה לנוסחים לא ממוקדים.
מלחמת זיהומים בתוך הגוף
המבחנים התובעניים ביותר נערכו במודלים של עכברים עם פצעים עור מקומיים וזיהומים בטניים מסכני-חיים. בפצעים מזוהמים, החיקויים הפלואורסצנטיים סעו לעבר החיידקים העמוקים ברקמה וכאשר נשאו טטרציקלין, ניקו כמעט לגמרי את המיקרובים. זה הוביל להחלמה מהירה יותר, עור חדש עבה יותר, הפרשת קולגן מסודרת יותר וצמיחה משובחת של כלי דם זעירים. במודלי זיהום מערכתית, החיקויים הצטברו ספציפית באיברים מזוהמים כגון הטחול והריאות, שם הם הפחיתו בחוזקה את ספירת החיידקים כשהיו טוענים אנטיביוטיקה. חשוב לציין כי מינונים גבוהים של החיקויים לבדם הראו בטיחות טובה, ללא נזק ברור לאיברים מרכזיים או לכימיה של הדם.
מה זה עשוי להצביע לגבי טיפולים עתידיים
על-ידי בניית דמיון כימי קרוב לרכיבי דופן התא של החיידק, עבודה זו מדגימה דרך חדשה "להיטמע" בחילוף החומרים של פתוגן במקום רק לתקוף מבחוץ. חיקויים כיראליים אלה משמשים גם כמקורות דיוק גבוה לדימות וגם ככלי תחבורה חכם שמכוון אנטיביוטיקה ישירות ליעדיה המיקרוביאליים, כולל זנים עמידים, תוך שמירה על תאי יונקים. אם יתורגמו לכלים קליניים, פלטפורמות ביומימטיות כאלה יכולות לעזור לרופאים לראות בדיוק היכן מסתתר זיהום ולטפל בו ביעילות רבה יותר במינוני תרופה נמוכים יותר, והן מציעות נשק מבטיח מול האתגר ההולך וגובר של התנגדות למיקרואורגניזמים אנטימיקרוביאליים.
ציטוט: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
מילות מפתח: התנגדות לאנטיביוטיקה, דופן תא חיידקי, העברת תרופה ממוקדת, דימות מולקולרי, נאנו-רפואה