Clear Sky Science · he
ניתוח רב־ממדי של פתולוגיית TDP-43 ספציפית לסוגי תאים בקורטקס המוטורי
מדוע המחקר הזה חשוב לאנשים
טרשת צליאית צדית (ALS) ודמנציה פרונטו-טמפורלית (FTD) הן מחלות מוח הרסניות שלוקחות מאנשים את היכולת לזוז, לדבר ואת אישיותם. אצל רוב החולים ב‑ALS ורבים מאלה עם FTD קיים סימן מיקרוסקופי משותף: שקיעת גושים של חלבון בשם TDP-43 במקום בו הם לא אמורים להיות. מחקר זה שואל שתי שאלות מעשיות עם משמעויות גדולות לטיפולים עתידיים: אילו תאי מוח ספציפיים נפגעים הכי חזק מבעיה ב‑TDP-43, ומה משתבש בתוך אותם תאים ברמת ויסות ה‑DNA ופעילות הגנים?
מעקב אחרי הנזק למרכז התנועה במוח
החוקרים התמקדו בקורטקס המוטורי הראשוני, הרצועה ברקמת המוח שאחראית על תנועה רצונית. באמצעות דגימות מוח מתורמות אחרי המוות מאנשים עם ALS, ALS‑FTD וביקורות נוירולוגיות תקינות, הם בידדו גרעיני תאים בודדים וקראו הן אילו גנים היו פעילים והן כמה הצפוף את ה‑DNA המקומי. גישה "מולטי‑אומית" זו, שהוחלה על יותר מ‑180,000 גרעינים, אפשרה להם לסווג תאים לסוגים מדויקים: מספר מחלקות של נוירונים מעוררי ומעכבים, וכן תאי תמיכה כמו אסטרוציטים, אוליגודנדרוציטים ומיקרוגליה. לאחר מכן הם שילבו זאת עם מפות מרחביות של ביטוי גנים ממאגר מוח אנושי נוסף כדי לשבץ את סוגי התאים הללו חזרה במבנה השכבות המוכר של הקורטקס.
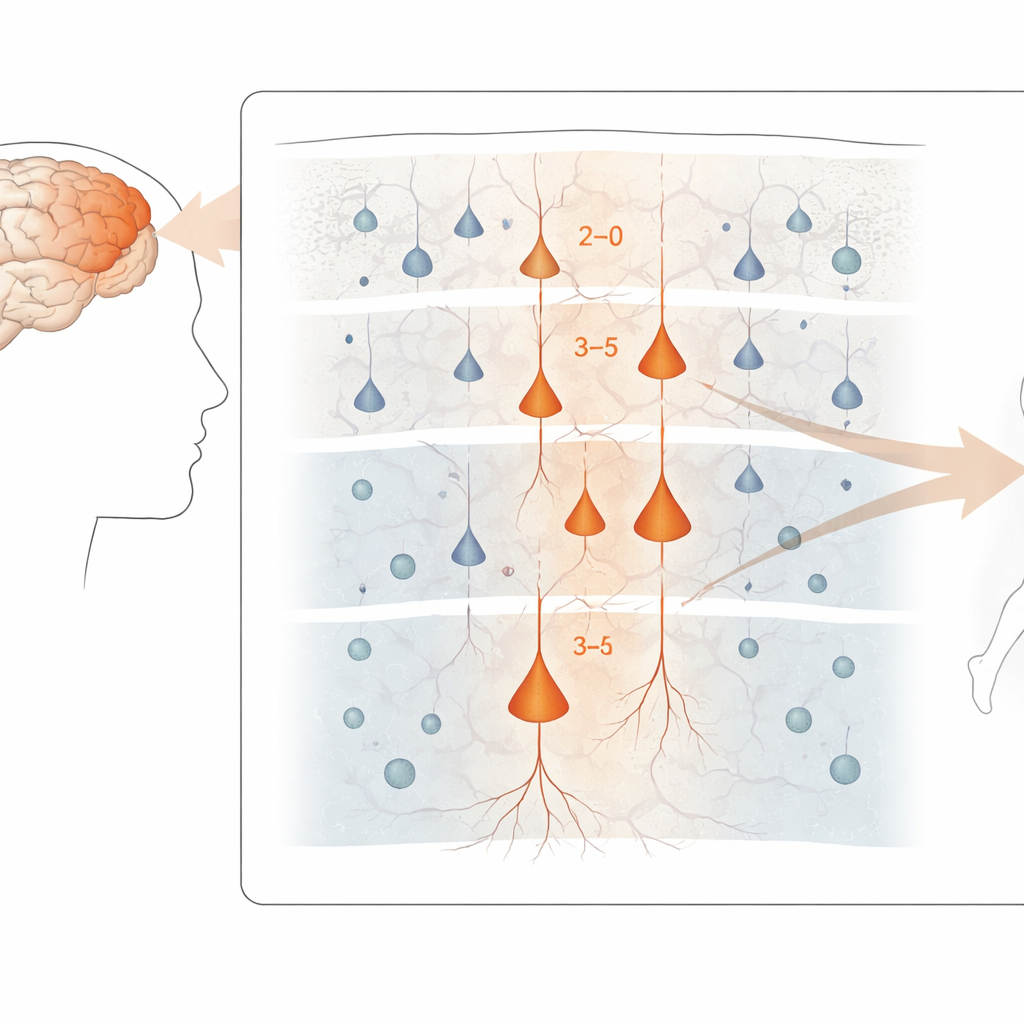
זיהוי הנוירונים הפגיעים ביותר
בכל רחבי הקורטקס המוטורי, השינויים החזקים ביותר ברמת הביטוי הגנטי הופיעו בנוירונים מעוררי (excitatory), התאים שמניעים פעילות לאורך המעגלים המוחיים. באופן מיוחד, נוירונים בשכבות העליוניות והאמצעיות שמתחברים בתוך הקורטקס, וכן תאים מסוימים בשכבות עמוקות ששולחים אותות מחוץ לקורטקס — לרבות תאי "בץ" (Betz) הגדולים השולטים על נוירוני השדרה — הראו את השינויים הבולטים ביותר. בהשוואה לכך, אינטרנוירונים מעכבים ורבים מתאים גליקליים הושפעו פחות ברמת ביטוי הגן, אף שלחלקם נצפו שינויים עדינים יותר. על אף הפרעה מולקולרית זו, התמהיל הכולל של סוגי התאים הגדולים ברקמה היה דומה באופן מפתיע בין חולים וביקורות, מה שמעיד שהנזק קשור יותר לאופן תפקוד התאים מאשר פשוט לאובדן מספרם.
כיצד TDP-43 מעצב מחדש את פעילות הגנים מבפנים
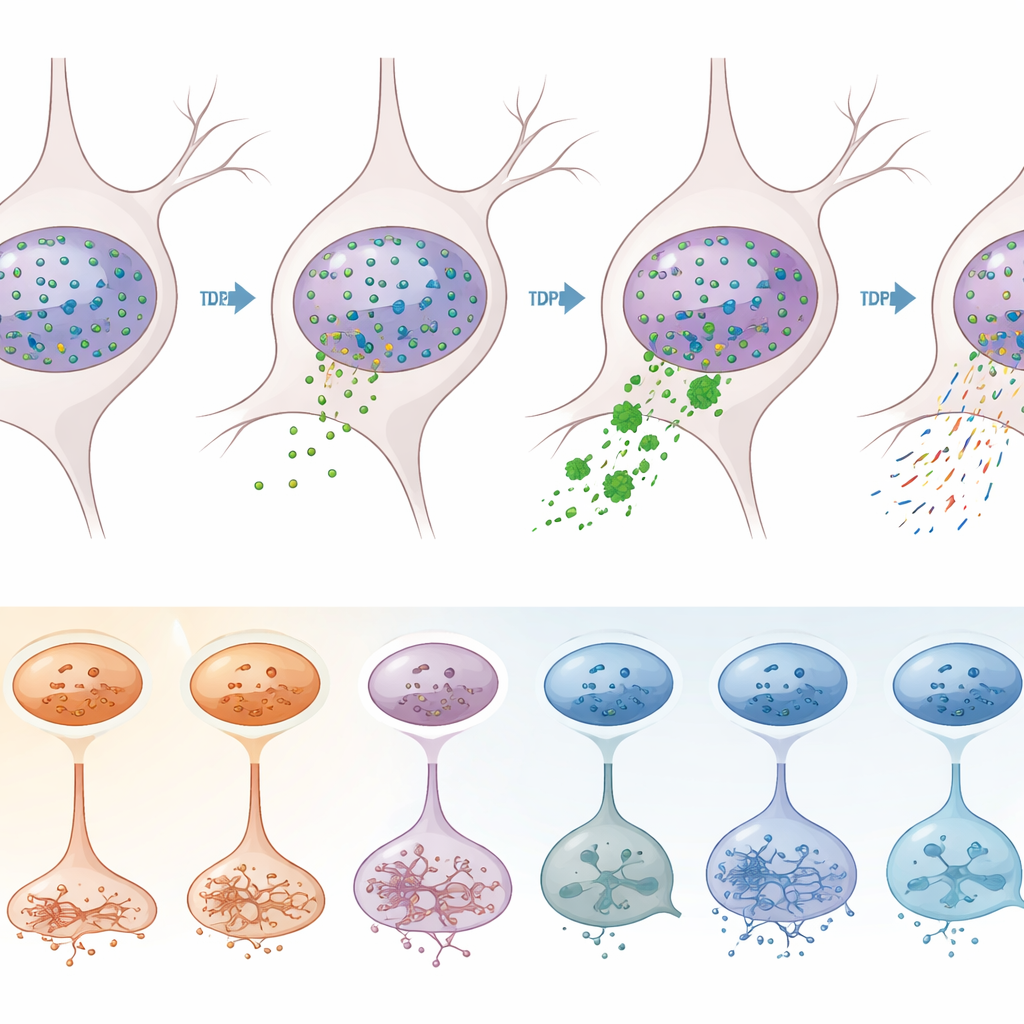
כדי להפריד בין השפעות הנובעות ישירות מ‑TDP-43 לבין תהליכים מחלתיים אחרים, הצוות השתמש באסטרטגיית מיון מתוחכמת. הם תייגו גרעינים בנוגדנים נגד TDP-43 וסמן נוירונלי, ואז השתמשו בציטומטריית זרימה כדי להפריד נוירונים שמגרעיניהם נעלם TDP-43 (סימן לפתולוגיה) מאלו ששמרו אותו. רצף של יותר מ‑12,000 גרעינים אלה חשף שאובדן TDP-43 מתרחש באופן גורף בנוירונים מעוררי, במיוחד תת‑סוגים ספציפיים בשכבות 2–3, 3–5, 5 ו‑6. בנוירונים הרגישים הללו מאות גנים היו בלתי מיוסדרים כראוי, כולל רבים שכבר נקשרו ל‑ALS. חתימות מולקולריות קלאסיות של תפקוד לקוי של TDP-43 — כגון הופעה של מקטעי "קריפטיים" בטרנסקריפטים של הגנים STMN2 ו‑KALRN, ושינויים במיקומי חיתוך וזנבות ה‑RNA — נמצאו מועשרות בבירור בגרעינים החסרים TDP-43.
רימודלינג אפיגנטי: לא כל שינוי נובע מ‑TDP-43
מכיוון שהם מדדו גם פעילות גנים וגם פתיחות כרומטין באותם גרעינים, המחברים יכלו לזהות אילו שינויים קשורים לשינויים באריזת ה‑DNA. הם מצאו עשרות אלפי מקומות בגנום שבהם נגישות הכרומטין המקומית עקבה אחר ביטוי הגן. רבים מהגנים ששונו ב‑ALS וב‑ALS‑FTD שכנו באזורי כרומטין כאלה, מה שמצביע שחלק מהחתימה המחלתית משקפת רימודלינג אפיגנטי רחב יותר ולא אך ורק השלכות ישירות של אובדן TDP-43. מעניין שהשינויים המקושרים לכרומטין ריכזו לעתים קרובות במסלולי איתות המעורבים בתקשורת בין תאים והכוונת אקסונים, והם היו חזקים במיוחד בנוירונים מעוררי מסוימים ובאוליגודנדרוציטים. כאשר הצוות השווה שינויים גנטיים שקשורים לפתולוגיית TDP-43 לאלה הקשורים לשינויים בכרומטין, הם מצאו כי יש ביניהם חפיפה חלקית אך ברובם זו שכבות הפרעה נבדלות.
מה משמעות הממצאים עבור טיפולים עתידיים
לקורא שאינו מומחה, המסר המפתח הוא ש‑ALS ו‑ALS‑FTD אינם פוגעים בקורטקס המוטורי באופן אחיד. במקום זאת, הם פוגעים בסוגי נוירונים מעוררי מסוימים ובמידה פחותה בתאי תמיכה מסוימים, ומשנים את תוכניות הגנים שלהם בדרכים התלויות הן בהתנהגות הלקויה של TDP-43 והן בשינויים רחבים יותר באופן אריזת וקריאת ה‑DNA. ממצאים אלה מציעים שטיפולים יעילים עשויים לדרוש גם מיקוד לפי סוג תא וגם לפי מסלול — לדוגמה, שחזור תפקוד TDP-43 או תיקון שגיאות הספלייסינג שלו בנוירונים הפגיעים ביותר, ובמקביל טיפול נפרד בשינויים אפיגנטיים ובשינוע האותות החוצים סוגי תאים. על ידי מיפוי הנוף המורכב הזה ברזולוציה גבוהה, המחקר מספק שרטוט לתכנון התערבויות מדויקות יותר שמטרתן להאט או למנוע את אובדן השליטה בתנועה ב‑ALS וב‑ALS‑FTD.
ציטוט: Ruf, W.P., Kühlwein, J.K., Meier, L. et al. Multi-modal dissection of cell-type specific TDP-43 pathology in the motor cortex. Nat Commun 17, 2406 (2026). https://doi.org/10.1038/s41467-026-69944-6
מילות מפתח: ALS, דמנציה פרונטו-טמפורלית, TDP-43, נוירונים של הקורטקס המוטורי, מולטי־אומיקס גרעיני יחיד