Clear Sky Science · he
עיכוב תרגום תלוי‑הקשר כמודול טיפולי לסרטן
לפנות את מפעלי החלבון נגד הסרטן
תאי סרטן שורדים על ידי ייצור קבוע של כמויות גדולות של חלבוני "מניע" קצרים וחסרי‑יציבות שמסייעים להם לגדול ולהתחלק. המחקר הזה בוחן גישה חדשה להילחם בסרטן על‑ידי סתימה עדינה של מכונות יצירת החלבון של התא — הריבוזומים — רק כשהן מנסות לבנות רצפי חלבון מסוימים, במיוחד אלה הנמצאים באונקוגנים שקשה לתקוף כמו MYC. התערבות סלקטיבית כזו עשויה להרוג תאי גידול תוך חיסכון ברוב ייצור החלבון התקין.
כיצד תאים בונים חלבונים — והיכן דברים עלולים להשתבש
כל תא תלוי בריבוזומים, מפעלים מולקולריים זעירים שקוראים מסרים גנטיים (mRNA) וקושרים חומצות אמינו ליצירת חלבונים. רוב התרופות הקיימות שפוגעות בריבוזומים, כמו אנטיביוטיקות או תרופות סרטן ישנות, פועלות ככלים גסיים: הן מדכאות באופן רחב את סינתזת החלבון, מה שעלול לפגוע בתאים בריאים ולגרום לתופעות לוואי קשות. החוקרים הניחו שבהתחשב בכך שלכל שרשרת חלבון בראשיתה יש רצף ותכונה כימית ייחודיים, ייתכן שניתן לעצב מולקולות קטנות שחוסמות את הריבוזום רק כאשר רצף מסוים נמצא במכונה, ומשאירות את שאר ייצור החלבון בתא כמעט ללא שינוי.
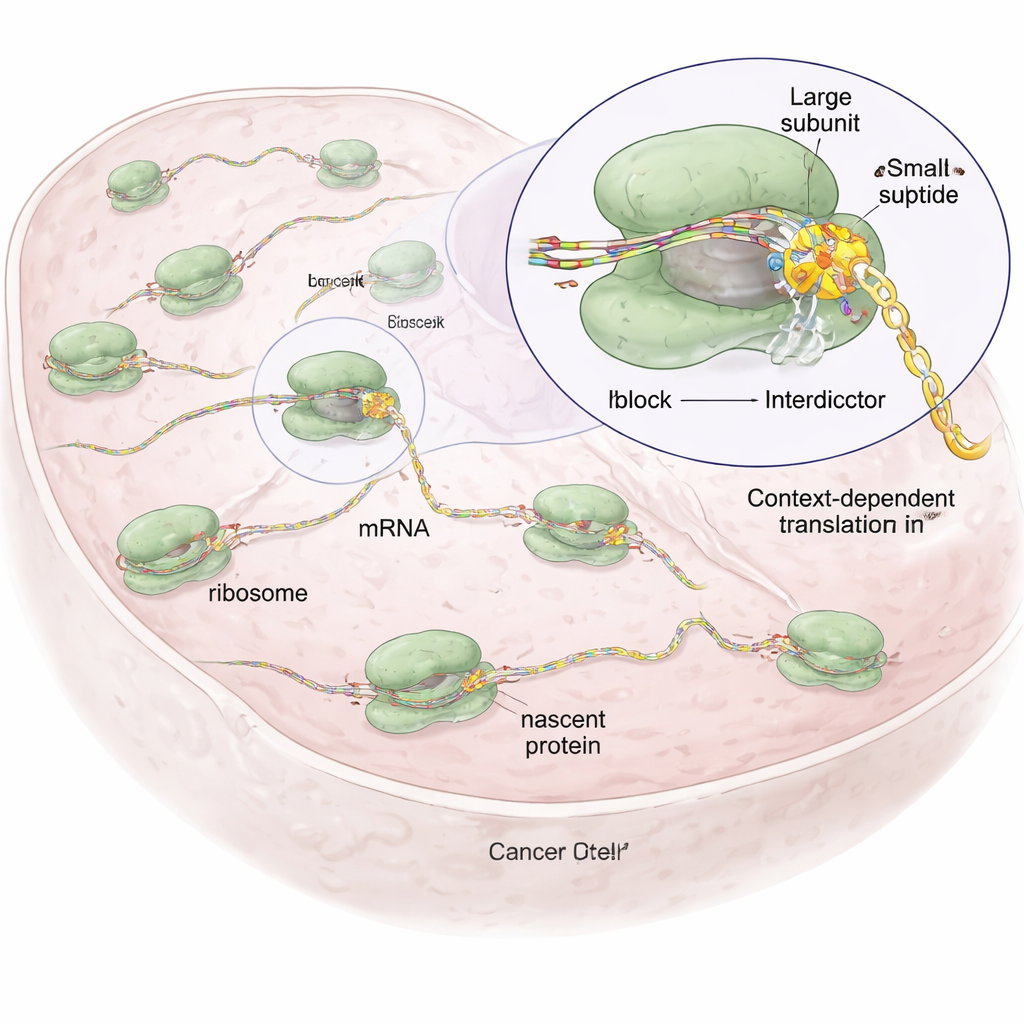
מולקולות מעוצבות שמעכבות רק רצפי חלבון מסוימים
בהתבסס על תרכובת טבעית שנקראת אניסומיצין, הקושרת את ליבת הקטליזה של הריבוזום שבה נוצרות הקשרים הפפטידיים, החוקרים יצרו משפחה של מולקולות סינתטיות שהם מכנים "אינטרדיקטורים". כולן חולקות שלד ליבה שמעגן אותן בתוך הריבוזום, אך הן שונות בקבוצות צד שפונות לעבר שרשרת החלבון המתארכת. קבוצות הצד האלה מכויילות להעדיף סוגים מסוימים של חומצות אמינו — למשל, אינטרדיקטור אחד (IDB‑001) נמשך לשאריות בעלות מטען שלילי, בעוד שאחר (IDB‑002) מעדיף שאריות קטנות ושומניות (הידרופוביות). באמצעות טכניקה שנקראת פרופיילינג של ריבוזומים, שממפה באופן גלובלי היכן הריבוזומים נעצרים על mRNA בתאים, הצוות הראה שכל תרכובת גורמת לעצירות במוטיבים קצרים מובחנים בשרשרת המתארכת, לעתים קרובות בנקודת האמינו‑חומצה המשנית (−1), מה שמדגים פעולה תלויה‑רצף במקום השראה גורפת.
צפייה במפגש בין התרופה לריבוזום אטום‑אטום
כדי לראות כיצד הסלקטיביות הזו פועלת בפרט, המחברים קפאו ריבוזומים אנושיים בפעולת התרגום של רצפי פפטיד מעוצבים וצילמו אותם במיקרוסקופ אלקטרונים קירוגני ברזולוציה כמעט‑אטומית. הם ראו את האינטרדיקטור משובץ באתר הפעיל של הריבוזום ויוצר מגעים מדויקים עם מספר אמינו‑חומצות אחרונות של השרשרת המתארכת. במבנה אחד, קבוצת צד הידרופובית של IDB‑002 מוחזקת על ידי שאריות קטנות שאינן מגושמות בפפטיד, מה שמסביר מדוע שרשראות גדולות יותר שם אינן מועדפות. במבנה אחר, קבוצת צד חומצית שמקורית מ‑MYC מתהפכת ליצירת גשר מלח עם קבוצה טעונה בחיוב על IDB‑001. נוכחות התרופה גם דוחפת בסיסי rRNA סמוכים למיקומים חדשים שמצמצמים את האתר הפעיל וחוסמים חלקית את כניסת ה‑tRNA הבא, ותורמת להקפאת מארג ההארכה באותם רצפים מועדפים.
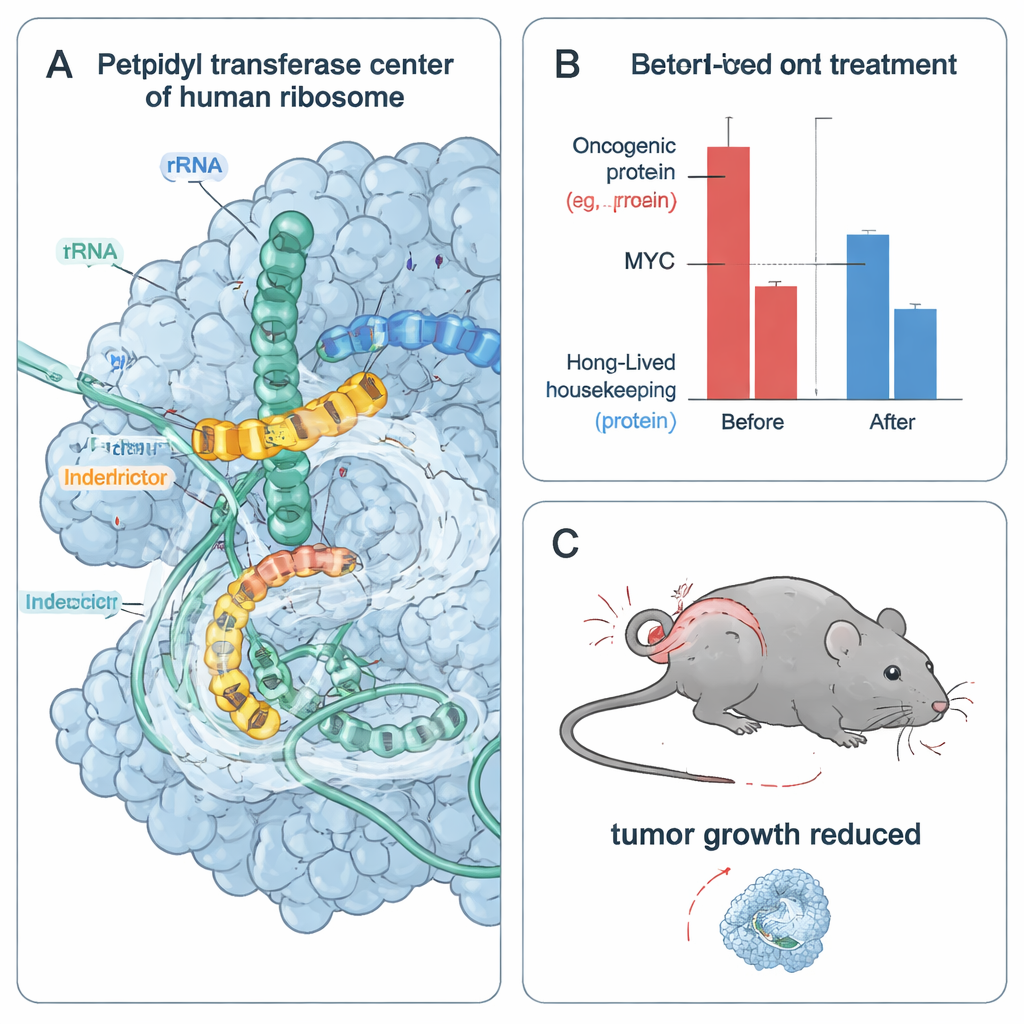
ממצבים של ריבוזומים תקועים אל תאי גידול במצב מתח ומתים
מכיוון שתאים המתמזגים במהירות תלויים במידה רבה בחלבוני אונקוגן קצרים וחסרי‑יציבות כמו MYC ו‑CCND1, הצוות בחן כיצד אינטרדיקטורים משפיעים על הישרדות תאי גידול. במספר קווי תאים סרטניים התלויים ב‑MYC, IDB‑001 ו‑IDB‑002 הורידו את כשירות התאים בריכוזים בננומולאריים עד מיקרומולאריים נמוכים. אנלוג משופר נוסף, IDB‑003, היה אף יותר חזק ומתאים למתן אוראלי. בתאים, תרכובות אלה רוקנו במהירות את רמות MYC וחלבוני אונקוגן دیگرים בעלי מחזור חיים מהיר אך השאירו חלבוני בית‑משמר ארוכי‑חיים יציבים יחסית באותו חלון זמן. התרופות גם עוררו תגובות מתח תאיות המקושרות להתנגשות ריבוזומים, אך חסימת מסלולי איתות המתח הללו לא ביטלה את אובדן הכשירות, מה שמרמז כי חוסר ישיר בחלבוני אונקוגן חיוניים הוא גורם מרכזי למות תאי הגידול.
הוכחת עיקרון במודל קשה של סרטן השד
כדי לבדוק האם הגישה עובדת בחיות, המחברים טיפלו בעכברים הנושאים גידולים אנושיים של סרטן השד המשולש‑שלילי במתן אוראלי של IDB‑003. לאורך 28 יום, הגידולים המטופלים גדלו הרבה יותר לאט מאשר באורוות‑בקרה, עם עיכוב גדילה של עד 80% במינונים גבוהים וללא דיווח על רעילות חמורה במחקר זה. ניתוח ביטוי גנים של הגידולים הראה דיכוי חזק של תוכניות הגנים המופעלות על‑ידי MYC, בהתאמה לפעילות MYC מופחתת בחי. יחד, התוצאות הללו מצביעות על כך שעצירת ריבוזומים בצורה סלקטיבית על רצפי חלבון מסוימים יכולה להחליש גידולים התלויים במניעים אונקוגניים בלתי‑יציבים ובאותו זמן להימנע מהרעילות הרחבה של מדכאי תרגום קלאסיים.
מדוע זה חשוב לטיפולים עתידיים בסרטן
עבודה זו מציגה סוג חדש של תרופת מולקולה קטנה: תרופה שפועלת לא על‑ידי קשירה לחלבון הגמור, אלא על‑ידי יירוטו בזמן הייצור ורק כאשר נוכח רצף "תג כתובת" קצר. מאחר שרבים מהחלבונים המעודדים סרטן הם גמישים, קצרים, בעלי חיי‑מדף קצרים או חסרי כיסים ברורים לתרופות רגילות, פגיעה בסינתזתם ישירות בריבוזום עשויה לפתוח נתיב לטיפול בגידולים שמונעים על‑ידי גנים שכרגע נחשבים ל'לא‑ניתנים‑לתרופה' כמו MYC. המחקר גם מציע שברחבת התאמת הכימיה של האינטרדיקטורים, ניתן יהיה לתכנן תרופות עתידיות המתמקדות במוטיבים רצף שונים ובמטרות מחלה מגוונות, ולהרחיב את האסטרטגיה הזו מעבר לאונקולוגיה למצבים אחרים שבהם הורדה סלקטיבית של חלבונים מסוימים עשויה להשיב את הבריאות.
ציטוט: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
מילות מפתח: טיפול בסרטן המכוון לריבוזומים, עיכוב תרגום, גידולים מונעים על‑ידי MYC, מולקולות קטנות התלויות בהקשר, סרטן השד המשולש‑שלילי