Clear Sky Science · he
הנדסה מקומית של TRIM13 מעלה את היכולת האנטי‑דלקתית של CAR‑M לטיפול בפיברוזיס כבד
תכנות מחדש של צוות הניקיון של הכבד
פיברוזיס כבד, תהליך הצלקת שיכול להוביל לצירוזיס ולכשל כבד, משפיע על מיליוני אנשים וכיום ישנם מעט טיפולים יעילים. מחקר זה בוחן דרך לרתום ולתכנת מחדש את תאי החיסון של הכבד כך שלא רק יסירו את התאים היוצרים הצלקת אלא גם יחלישו דלקת מזיקה, ובכך עשוי להציע טיפול בטוח ויעיל יותר למחלה כרונית של הכבד.
מדוע צלקת בכבד קשה לעצירה
כאשר הכבד נפגע שוב ושוב—על ידי וירוסים, אלכוהול או מחלות מטבוליות—הוא מנסה להחלים על‑ידי בניית רקמת צלקת. תאים מיוחדים שנקראים תאי כוכב כבדיים (hepatic stellate cells) עוברים למצב "מופעל" ומשחררים סיבים קשיחים, ממש כמו בנאים שמפזרים בטון. עם הזמן הצלקת, המכונה פיברוזיס, מעוותת את האיבר ומפחיתה את תפקודו. תאי חיסון שנקראים מקרופאגים עומדים בלב התהליך הזה. בכבד פגוע הם יכולים להתנהג כמו סכין עם שני חודים: במצב אחד הם מזינים דלקת ומפעילים את תאי הכוכב, ובמצב אחר, מחלֵב יותר, הם מסייעים לפרק את הרקמה הצלקתית ולהחזיר איזון.
הפיכת אותות מזיקים לאותות מועילים
החוקרים התמקדו באיתות סכנה מרכזי בכבדים מפוצעים: DNA מיטוכונדריאלי שנדלף מתאים פגועים. מקרופאגים מזהים DNA זה דרך מסלול הידוע כ‑cGAS‑STING, שמדחף אותם למצב פרו‑דלקתי ומעודד פיברוזיס. חלבון בשם TRIM13 בדרך כלל מסייע לרסן את STING על‑ידי תיוגו להרס. הקבוצה הניחה כי העלאת רמת TRIM13 בתוך מקרופאגים בכבד יכולה להפוך אותם חזרה למצב מרגיע ותומך בהחלמה. במקביל רצו שכאשר הם עושים זאת, התאים יזהו ישירות ויחסלו את תאי הכוכב המייצרים צלקת. לשם כך השתמשו בקונספט של קולטן אנטיגן כימרי (CAR), שאומץ מטיפולי סרטן: רצפטור סינתטי המאפשר לתאי חיסון לזהות מטרות נבחרות—במקרה הזה חלבון בשם FAP הנמצא בשפע על תאים כוכביים מופעלים.
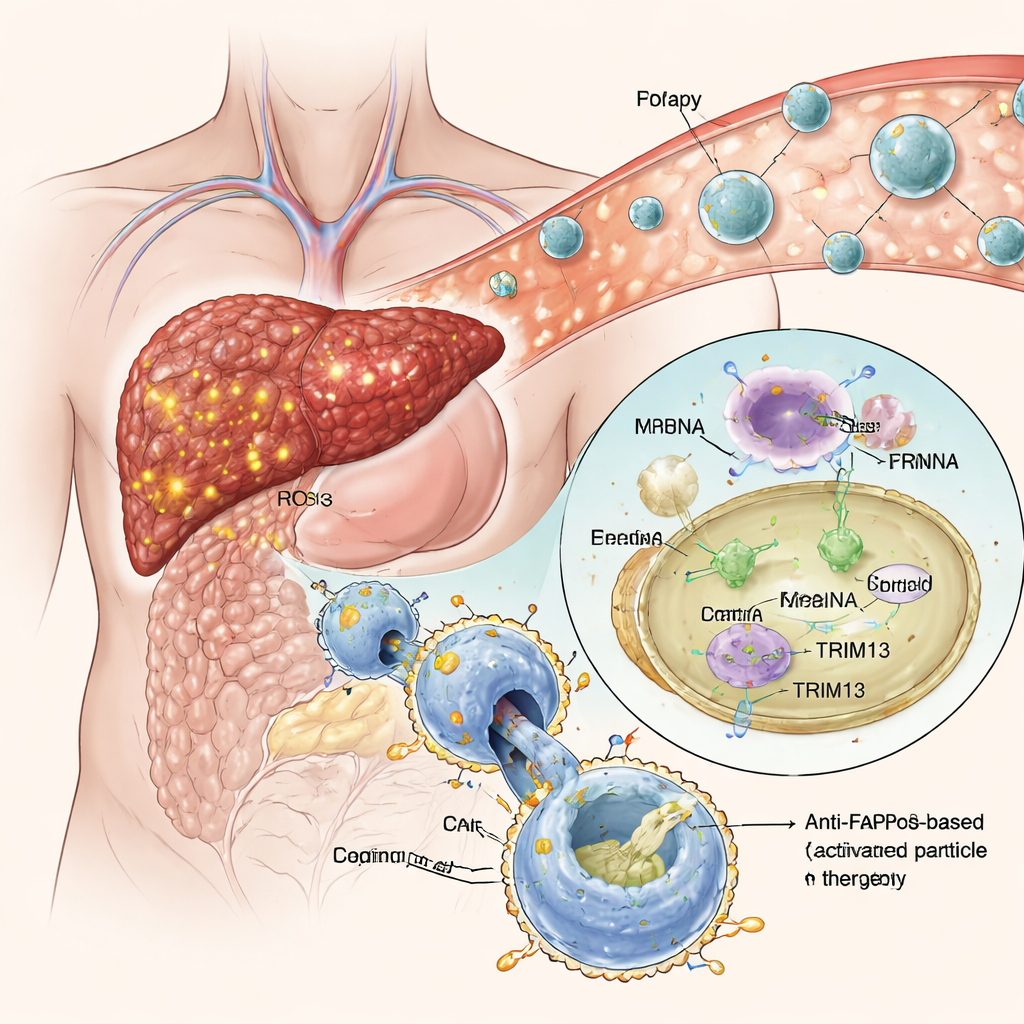
ננו‑חלקיקים חכמים שממוקדים לרקמה החולה
במקום למהנדס מקרופאגים מחוץ לגוף, הקבוצה בנתה ננו‑חלקיקים שומניים "נוצצים‑אפרוציטוזה"—כדורים זעירים מבוססי שומן הנושאים הוראות גנטיות כ‑mRNA. חלקיקים אלה צופים בצורת מוסווה של פוספטידילסרין, אות טבעי של "אכול‑אותי" שתאים גוססים מציגים כדי למשוך מקרופאגים. בסביבה חמצונית גבוהה של רקמת כבד פיברוטית, המסווה מוסר והאות נחשף, מה שמעודד מקרופאגים סמוכים לבלוע את הננו‑חלקיקים. ברגע שהם בפנים, ה‑mRNA משתחרר ונקרא על‑ידי התא, מה שמוביל לייצור גם של TRIM13 וגם של CAR נגד FAP. בתרביות תאים הגישה הזו הצליחה לדחוף מקרופאגים למצב אנטי‑דלקתי ולתת להם תיאבון חזק וסלקטיבי לתאים חיוביים ל‑FAP המייצרים צלקת, מבלי לפגוע ביכולתם הרגילה לנקות שאריות אחרות.
מכבד חולה לכבד מתחדש בעכברים
הצוות בדק אחר כך את האסטרטגיה הזו במודלים עכבריים של פיברוזיס כבד שנגרם או על‑ידי חומר רעיל או על‑ידי תזונה שומנית ודלה בחומרים מזינים. ננו‑חלקיקים שהוזרקו סיסטמית הגיעו בצורה יעילה אל הכבד ובמיוחד אצל בעלי הפיברוזיס נבלעו בעיקר על‑ידי מקרופאגים. שם, התאים המהונדסים הפגינו פעילות מופחתת של מסלול STING וייצור נמוך יותר של מולקולות דלקתיות, יחד עם הגדלה של היכולת להרוג תאי כוכב מופעלים. ניתוחי רקמות הראו ירידות חותכות בקולגן וסמנים אחרים של צלקת, מבנה מטריקס חוץ‑תאי עדין יותר ונורמלי יותר, ושיפור בבדיקות דם של תפקוד הכבד. כבדי העכברים המטופלים הפגינו יותר תאים מתחלקים ושחזור ארכיטקטורת כבד בריאה יותר, מה שמרמז על תיקון אמיתי של האיבר ולא רק על דיכוי זמני של הדלקת.
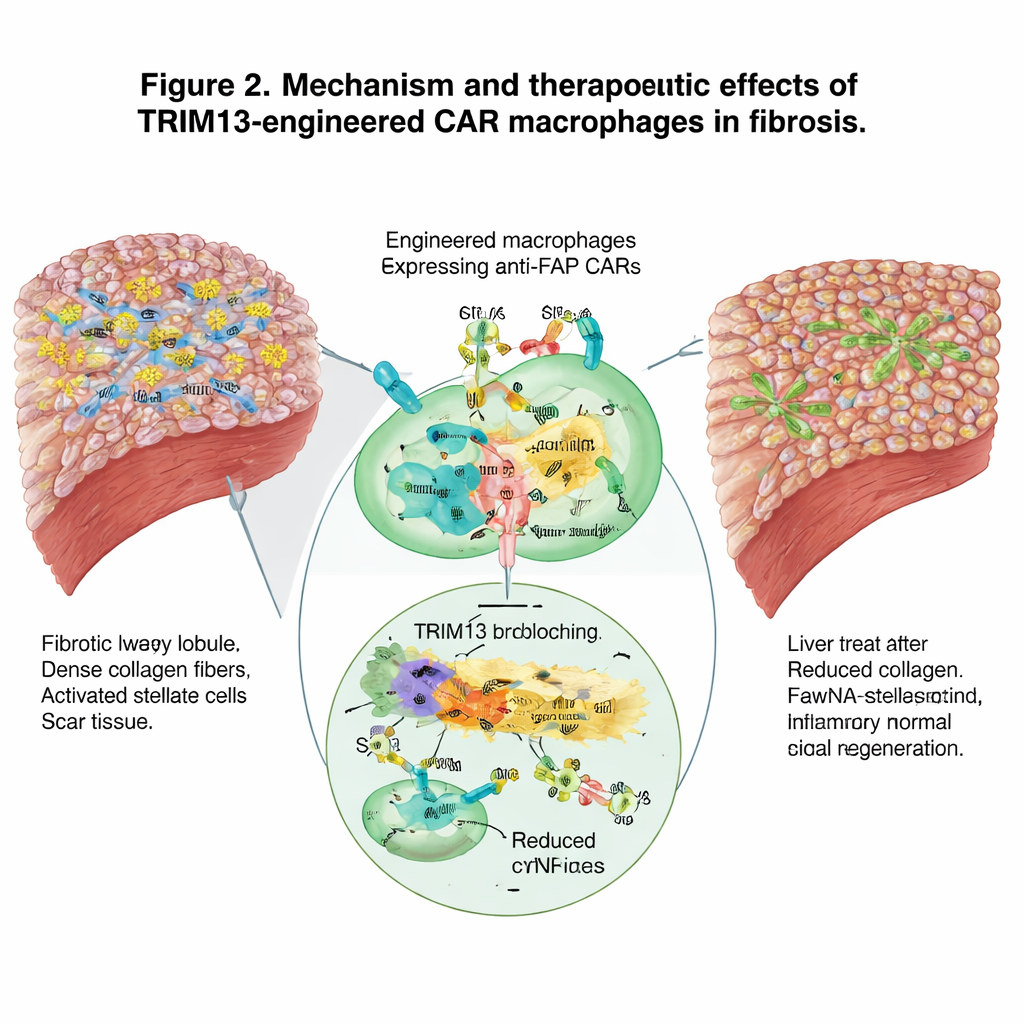
גיוס מערכת החיסון הרחבה
מעבר להסרת הצלקת ישירה, המקרופאגים המהונדסים עיצבו מחדש את נוף המערכת החיסונית הרחב יותר. הם עברו מפרופיל תוקפני ומזיק לפרופיל יותר פותר ומרפא והורידו אותות דלקתיים בדם. במקביל, על‑ידי לעיסה של תאים היוצרים צלקת הם נראו כמורים למערכת החיסון המותאמת, משכים נויטרופילים, תאי דנדריט ותאי T ומעודדים תגובה מתואמת נגד רקמת הפיברוזיס. ריצוף RNA חד‑תאי של תאי החיסון בכבד אישר מעבר מתוכניות גנטיות פרו‑דלקתיות לכיוון קיבולת מוגברת לבליעה וניקוי של תאים ושאריות מזיקים.
מה זה עשוי להצביע לחולים
לרואה שאינו מומחה, המסר הוא שעבודה זו מצביעה על דרך ל"ללמד מחדש" את תאי האיסוף של הכבד כך שהם גם מפרקים את רקמת הצלקת וגם מכבים את אותות האזעקה הכרוניים ששומרים על ההרס. על‑ידי שימוש בהוראות mRNA קצרות־מועד הארוזות בננו‑חלקיקים חכמים, הטיפול נמנע משינוי קבוע של תאים ומגביל את הפעילות לאזורים חולים, מה שעשוי לצמצם תופעות לוואי. למרות שדרושים מבחנים רבים יותר לפני שניתן יהיה לנסות זאת בבני אדם, האסטרטגיה מציעה מתווה מבטיח לטיפול בפיברוזיס כבד—ואולי גם במחלות פיברוטיות אחרות—בידי הפיכת מערכת החיסון ההיא לגורם מעודד ריפוי במקום דוחף צלקת.
ציטוט: Gao, J., Yang, Z., Song, Y. et al. TRIM13 in situ engineering boosts anti-inflammatory capacity of CAR-Ms for liver fibrosis therapy. Nat Commun 17, 2077 (2026). https://doi.org/10.1038/s41467-026-69858-3
מילות מפתח: פיברוזיס הכבד, טיפול באמצעות מקרופאגים, העברת mRNA בננו‑חלקיקים, קולטן אנטיגן כימרי, TRIM13 נתיב STING