Clear Sky Science · he
היווצרות תחום ה‑PIN המשולב של SMG5‑SMG6 חיונית ל‑NMD
כיצד התאים מגינים על עצמם מפני הודעות פגומות
התאים שלנו קוראים באופן קבוע הודעות גנטיות (mRNA) כדי לייצר חלבונים. אך הודעות אלה לעתים מכילות אותות עצירה מוקדמת שיכולים להפיק חלבונים מקוצרים והרסניים. התהליך שמחריב הודעות פגומות כאלה נקרא דגרדציית mRNA בתיווך עצירת שגיאה (NMD). המאמר חושף כיצד שני חלבונים מרכזיים, SMG5 ו‑SMG6, משתפים פעולה באופן פיזי כדי לנתק הודעות פגומות, ומבהיר תעלומה ותיקה בתפקוד בקרת האיכות התאית.
גילוי השותפות הנסתרת
שנים אחדות מדענים ידעו ש‑SMG6 יכול לחתוך RNA ישירות, בעוד ש‑SMG5 נתפס כ"מת ללא פעילות קטליטית" ועיקר תפקידו כסקלטון או עוזר. ובכל זאת, ניסויים בתאים הראו תמונה מבלבלת: SMG6 לא פעל כראוי בלי SMG5, ו‑NMD קרס אם אחד מהם נעדר. המחברים השתמשו בחיזוי מבני מתקדם (AlphaFold), בבדיקות ביוכימיות עם חלבונים מטוהרים וניסויים גנטיים בקווי תאים אנושיים כדי לפתור את הסתירה. המודלים שלהם חזו שראשי הזנב של SMG5 ו‑SMG6, המכונים תחומי PIN, משתחלים זה לצד זה ויוצרים מבנה משותף. יחידה זו המשולבת — שכונתה "cPIN" — הוצעה כמכונת החיתוך האמיתית ב‑NMD. 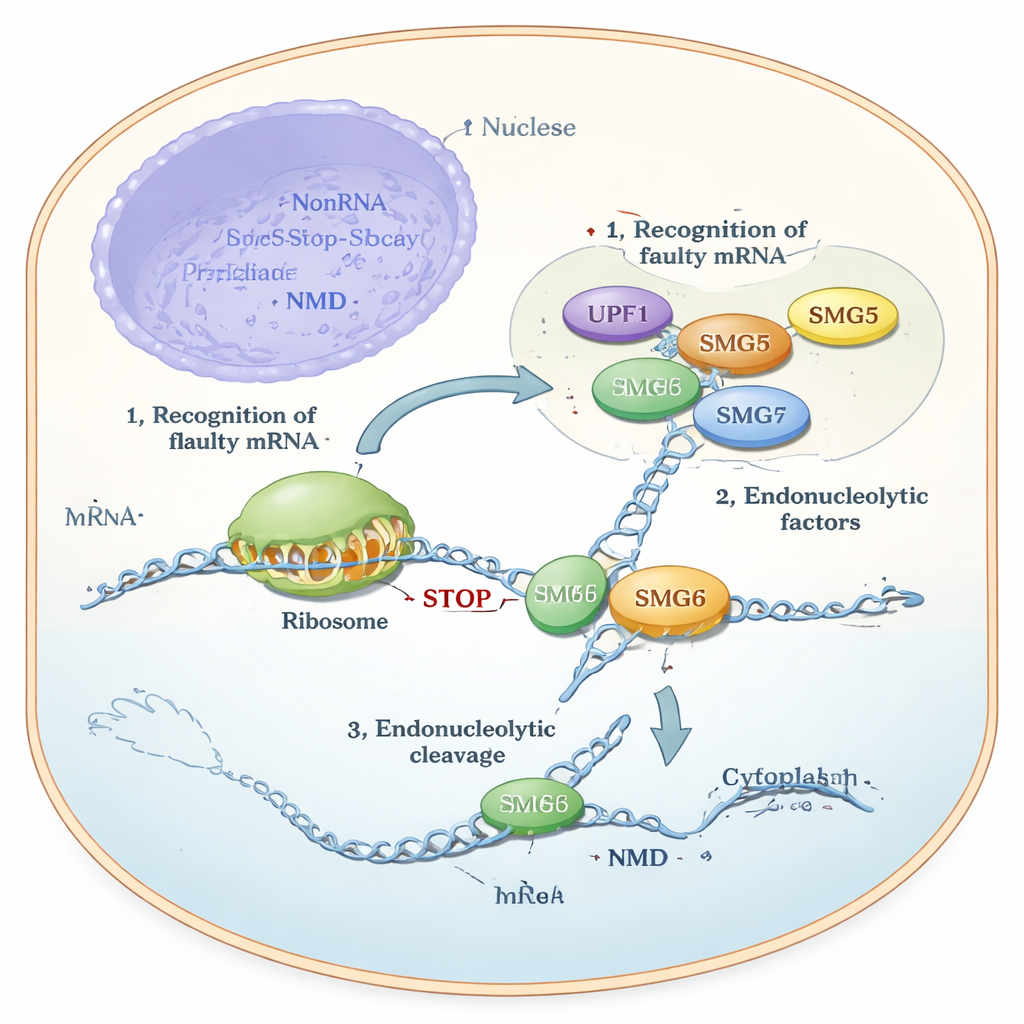
שחזור המספרים המולקולריים בצינור הבדיקה
כדי לבדוק את הניבוי, הצוות ייצר קטעים של SMG5 ו‑SMG6 אנושיים בחיידקים וטיהר אותם. כשכל אחד מהם לבד, SMG6 הפגין יכולת חיתוך חלשה בלבד על תת‑מטרה RNA מתוכננת, ו‑SMG5 כמעט ולא הציג פעילות. אך כאשר שני הקטעים הומצאו יחד, פעילות החיתוך גדלה בחדות, גם בתנאים שבהם ממיר חלבוני זיהום סביר שלא היה משחק תפקיד. אותו אפקט הופיע על מולקולות בדיקה מבוססות RNA קוויות ומעגליות, מה שמצביע על כך שהחיתוך המוגבר בא אכן מצמיחת זוג SMG5–SMG6. חיבור כימי וניתוח ספקטרומטריה של מסה הראו עוד שהשניים באים במגע הדוק, ותומכים ברעיון של שותפות ישירה, גם אם חולפת.
השלמת הלהב החותך
המודלים המבניים הציעו בדיוק כיצד SMG5 משפר את SMG6. SMG6 תורם ארבע חומצות אמינו חומציות שמחזיקות יוני מתכת במרכז אתר החיתוך, כפי שמקובל במשפחה זו של אנזימים. באופן מפתיע, המודלים מיקמו שארית חומצית נוספת מ‑SMG5 סמוך אליהן, ובכך הרחיבו למעשה את הכיס הקטליטי. שאריות טעונות במטען חיובי ב‑SMG5 צפויות לאחוז בגב הכללי של ה‑RNA ולעזור למקם אותו לחיתוך. כאשר החוקרים מוטטו חומצות אמינו קריטיות ב‑SMG5 או ב‑SMG6, הקומפלקס המשולב איבד רוב כוח החיתוך שלו במסלול מבחנה. אותן מוטציות נכשלו גם בהצלת NMD בתאים אנושיים מהונדסים שבהם החלבון הרגיל הוזל, וקשרו בחוזקה את המודל המבני לפעולה תאית ממשית. 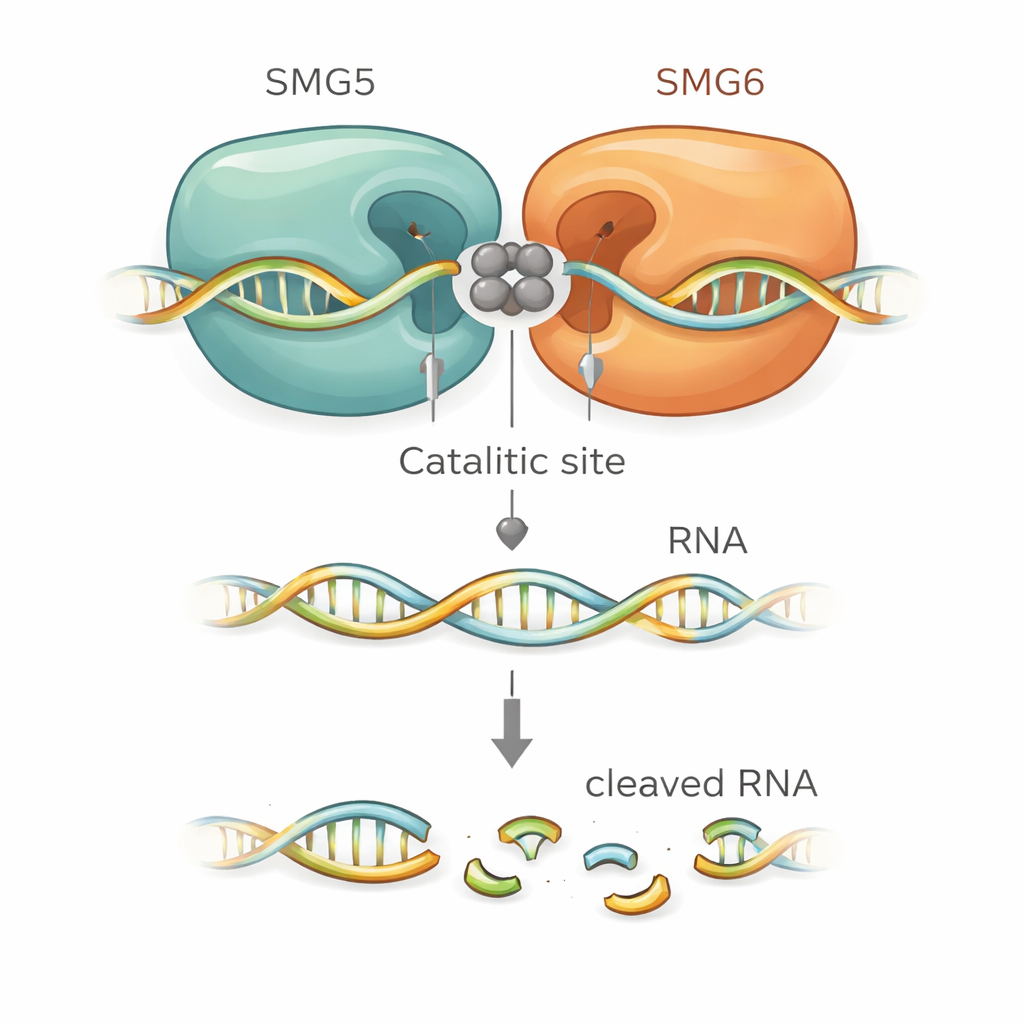
הוכחה ששני השותפים חיוניים בתאים
מכיוון שהסרה מוחלטת של SMG5 או SMG6 הורגת תאים, הצוות השתמש במערכת "דגרון" המאפשרת לתייג כל חלבון כך שיהיה ניתן להשמידו במהירות בעזרת מולקולה קטנה. שילוב שיטת ההריסה המהירה עם התערבות RNA איפשר הסרה כמעט מוחלטת של SMG5, SMG6 או רגולטור מרכזי שנקרא UPF1. רצף RNA ברמת הגנום גילה אז מה קורה ל‑NMD כאשר כל גורם כזה נעדר. דילול SMG5 או UPF1 הניב שינויים כמעט זהים ב‑RNA התאי, עם הצטברות חזקה של טקסטונים פגומים הרגישים ל‑NMD. הסרת SMG6 נתנה אפקט דומה, אם כי מעט מתון יותר. נתונים אלה מראים ש‑SMG5 ו‑SMG6 אינם מסלולים מקבילים אופציונליים; הם פועלים ביחד עם UPF1 כמרכיבים ליבה של נתיב דגרציה עיקרי אחד.
מדוע זה חשוב לבריאות התאית
במילים פשוטות, המחקר מראה ש‑SMG5 ו‑SMG6 מצטרפים יחד ליצירת זוג מספריים מולקולריים אחד וחזק המחתך הודעות גנטיות פגומות. SMG6 מספק את רוב הלהב, אך SMG5 מוסיף את קצה החסר ועוזר להחזיק את ה‑RNA במקומו, מה שהופך חותך חלש ליעיל. ה‑"cPIN" המשולב הזה מסביר מדוע התאים זקוקים לשניהם כדי לשמור על טוהר הודעות ה‑RNA. בהבהרת המנגנון שבו שלב החיתוך המרכזי ב‑NMD מופעל רק כשזוהו הודעות פגומות, העבודה מציעה תמונה ברורה יותר של האופן שבו התאים מונעים הצטברות חלבונים מקוצרים ורעילים וכיצד הם מכוונים בעדינות את ביטוי הגנים.
ציטוט: Kurscheidt, K., Theunissen, S., Pasquali, N. et al. Composite SMG5-SMG6 PIN domain formation is essential for NMD. Nat Commun 17, 1934 (2026). https://doi.org/10.1038/s41467-026-69819-w
מילות מפתח: דגרדציית mRNA בתיווך עצירת שגיאה (NMD), בקרת איכות RNA, SMG5 SMG6, פיקוח על mRNA, ויסות ביטוי גנים