Clear Sky Science · he
דגימה יעילה של מסלולי מעבר בקנה מידה גדול וקונפורמציות ביניים במורכבים חלבוניים תת-מיקרוסקופיים
צפייה בחלבונים בתנועה
רבים מהמולקולות ששומרות על חיינו מתנהגות פחות כמו לבני לגו קשיחות ויותר כמו מכונות זעירות שמשנות צורה כל הזמן. תנועות אלה מניעות תהליכים כמו ייצור אנרגיה, תיקון DNA ומאפשרות לווירוסים להיכנס לתא. ניסויים כמו קריו-אלקטרון-מיקרוסקופיה מסוגלים היום "להקפיא" כמה מהצורות הללו, אבל לא את השלבים החולפים שביניהן. המאמר הזה מציג את eBDIMS2, שיטה מחשבית חדשה שיכולה "להשלים את הפריימים החסרים" של תנועת חלבון אפילו עבור מכונות מולקולריות עצומות שהן בעבר היו גדולות ומורכבות מדי כדי לדמות אותן במחשב רגיל.
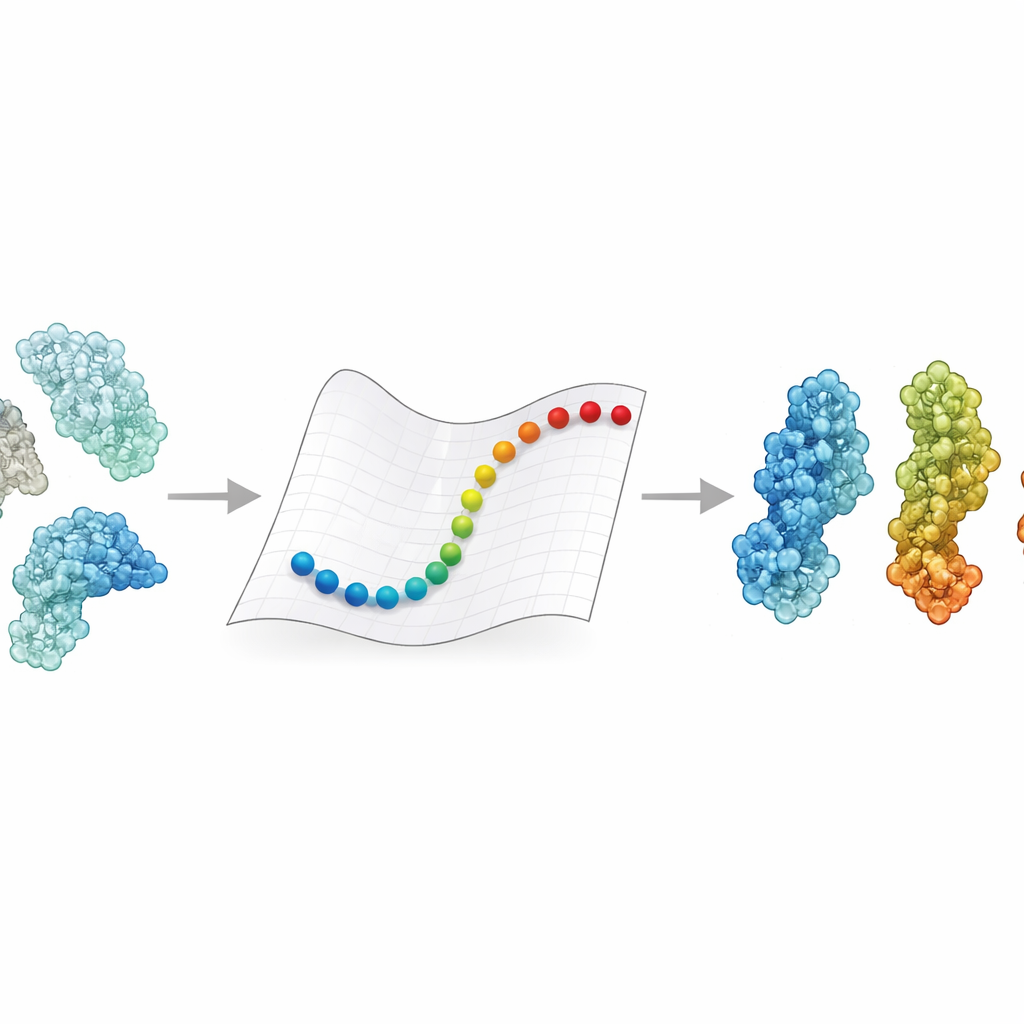
מדוע שינוי צורת החלבון חשוב
חלבונים נדירים נשארים נעולים במצב אחד. הם נפתחים ונסגרים, מסתלסלים ומתעקמים בתגובה לאותות כמו שינוי במתח, pH או קשירת מולקולה שותפה. שינויים אלה יכולים להכריע האם אנזים פעיל או לא, או האם קולטן ייאחז בווירוס או ישחררו. ניסויים נותנים לנו תמונות מפורטות של כמה צורות מרכזיות, וסימולציות דינמיקת מולקולות יכולות בעקרון לקשר ביניהן על ידי מעקב אחרי כל אטום עם הזמן. אבל מעקב כזה אחרי תנועה של המורכבים העצומים שנצפים כיום בקריו-EM, שמשקלם לעתים מאות אלפי עד מיליוני דלטונים, דורש בדרך כלל מחשבי-על ושבועות של חישוב. כתוצאה מכך, עבור רבים מהג׳אנטים הרלוונטיים רפואית, עדיין איננו יודעים כיצד מצב אחד הופך לאחר.
נתיב מהיר יותר בנופים של חלבון
eBDIMS2 נוקטת קיצור דרך על ידי פישוט האופן שבו מייצגים חלבונים וכיצד מחושבת תנועתם. במקום לעקוב אחרי כל אטום, כל חומצת אמינו מיוצגת כנקודה בודדת המחוברת בקפיצים ברשת אלסטית. קפיצים אלה משקפים כיצד חלקים שונים של החלבון נוטים לנוע ביחד. השיטה משתמשת בדינמיקת בראון — חוקים מתמטיים המדמים זיזוז בנוזל — כדי לדחוף את המבנה ממצב ניסוי ידוע אחד לעבר מצב אחר. בעקרון, eBDIMS2 מתמקדת רק באינטראקציות שבאמת חשובות, ומשתמשת בסף מרחק ובחישוב במקביל כדי לצמצם עלויות. זה משפר את סקלת התהליך מכפולה-סבירה לכמעט ליניארית ביחס לגודל החלבון. בפועל משמעות הדבר היא שניתן לחקור מעברים עבור מצבורי ענק המתקרבים לשני מיליון דלטון תוך שעות על שולחן עבודה, במקום להיות בלתי נגישים למעשה.
בדיקת המסלולים מול חלבונים אמיתיים
כדי לבדוק האם הנתיבים המהירים הללו הגיוניים מבחינה ביולוגית, המחברים הרכיבו אנסמבלים של 47 חלבונים גדולים ועוד 15 קומפלקסים נוספים, בסך הכל מאות מבנים שנפתרו בעיקר על ידי קריו-EM. הם השתמשו בניתוח רכיבים עיקריים, כלי סטטיסטי החוטב את דרכי התנועה הדומיננטיות של כל חלבון, כדי לארגן את המבנים לנופים של קונפורמציות כמו פתוח, סגור, פעיל או לא פעיל. לאחר מכן ביקשו מ-eBDIMS2 לקשר זוגות מצבי קצה על פני נוף זה. הנתיבים המתקבלים הוקרנו חזרה לאותם מפות ממימד נמוך, כדי לבדוק האם הם עוקבים אחר מסלולים חלקים החולפים קרוב לאמצעיים שנצפו ניסויית. ביותר מ-30% מהמערכות, הנתיבים המדומים עברו קרוב — בתוך כמה אנסטרומים — למבני ביניים שלא ניתנו כקלט. במקרים תובעניים כמו האנזים לתיקון DNA DNA-PKcs או חלבון הספק של קורונה, הנתיבים המיוצגים בקנה גס חפפו היטב גם עם סימולציות ברמת האטום הרבה יותר יקרות, כולל דינמיקת מולקולות ממוקדת וריצופי דגירה משופרים מתקדמים.
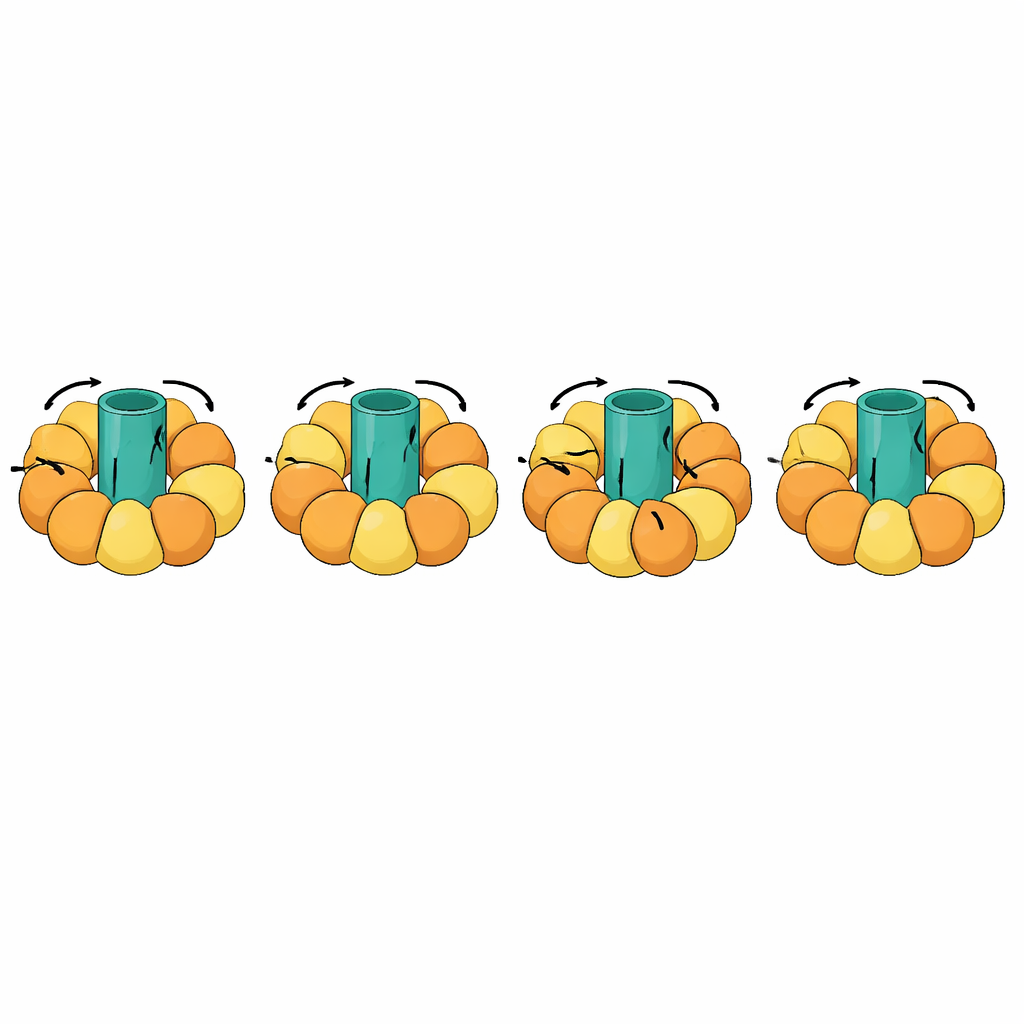
מעקב אחרי מכונות מולקולריות ענקיות
אחת הבדיקות הבולטות כללה מכונות סיבוביות כמו ATP סינתאזות, המייצרות את מטבע האנרגיה של התא על ידי צימוד רוטור מסתובב בממברנה לתנועות פתיחה וסגירה בתת-יחידות הסובבות. המעברים הללו מורכבים בצורה יוצאת דופן: חלקים מהמולקולה חייבים להישאר קשיחים ולהסתובב כיחידה, בעוד שאחרים מתעקמים במחזור מתוזמר. eBDIMS2 מציעה טיפול מיוחד בחלקים קוואזי-קשים כאלה וכן בדגמי ניסוי חסרים עם קטעים חסרים, שניהם נפוצים בקריו-EM. עם התכונות הללו ניתן לדמות מחזורים סיבוביים מלאים של ATP סינתזות ומורכבים עצומים אחרים כמו צ'פרונים מולקולריים, קולטנים והרכבות ויראליות. לאורך כל הדרך, המבנים הביניים שנוצרו נמנעים מעיוותים קשים שמייצרות לעתים שיטות מתחרות וניתנים לניקוי לתבניות אטומיות המתאימות לחישובי תכנון תרופות או לסימולציות ארוכות ומפורטות יותר.
מה משמעות הדבר לביולוגיה ולרפואה
המחקר מראה ש-eBDIMS2 מסוגלת לתאר באופן אמין את המסלולים העיקריים בין צורות חלבון ידועות עבור מערכות שהיו מעבר להישג יד של סימולציות מסורתיות. היא לא מחליפה סרטים מפורטים ברמת האטום או מספקת אנרגיות וזמנים מדויקים, אבל היא מציעה דרך מהירה ומבוססת-פיזיקה למיפוי כיצד מכונות מולקולריות גדולות עלולות לנוע, באמצעות זוג מצבי ניסוי בלבד כקלט. ככל שמאגרי המבנים מתמלאים במצבים מרובים של הרכבות חלבוניות גדולות הקשורות לסרטן, זיהומים ומחלות אחרות, גישה זו מעניקה לכלים נגישים לחוקרים לחבר את הנקודות, להציע מצבי ביניים סבירים ולהנחות היכן לחפש בהמשך בשיטות ברזולוציה גבוהה יותר או בעיצוב תרופות מכוון.
ציטוט: Scaramozzino, D., Lee, B.H. & Orellana, L. Efficient sampling of large-scale transition pathways and intermediate conformations in sub-mesoscopic protein complexes. Nat Commun 17, 2202 (2026). https://doi.org/10.1038/s41467-026-69809-y
מילות מפתח: דינמיקת חלבונים, סימולציות מולקולריות, קריו-EM, נתיבי קונפורמציה, מניפולציה בקנה גס