Clear Sky Science · he
הפעלת IRF3 באורגנלות הלב פוגעת בפעילות החמצונית המיטוכונדריאלית באמצעות עיכוב PGC-1α ודוחפת לכשל לבבי
מדוע לבבות תחת מתח ותאים מותשים חשובים
כשל לב מתואר לעתים כ"בלאי" של הלב, אך מתחת לפני השטח זו גם תופעה של דלקת כרונית וכשל תחנות הכוח בתוך תאי שריר הלב. המחקר עוסק בשאלה שנראית פשוטה אך בעלת השלכות רחבות: האם יש מתג מולקולרי בודד בתוך תאי הלב שמקשר בין דלקת מזיקה לירידה בייצור האנרגיה — ואם כן, האם שינוי במתג הזה יכול לשנות את מהלך הכשל הלבבי? במעקב אחר חוט זה מצאו החוקרים שחקן מרכזי והראו כי הגברה עדינה של תוכנית האנרגיה של הלב יכולה במידה חלקית להציל לבבות נכשלות בעכברים.
מתג מולקולרי בלבבות חולים אנושיים
החוקרים התרכזו בחלבון בשם IRF3, הידוע בעיקר בתפקידו בסיוע לתאים להגיב לזיהומים ויראליים. הם בדקו רקמות מאנשים עם קרדיומיופתיה איסכמית, צורה נפוצה של כשל לב הנגרמת עקב הפחתת זרימת הדם אחרי התקפי לב. בלבבות נכשלות אלו, IRF3 לא היה רק נוכח — הוא היה מופעל כימית באתרי fosforylation ספציפיים, סימן לכך שהוא הפעיל תוכניות גנטיות. במקביל, המנגנון שמאפשר למיטוכונדריות להפוך דלק לאנרגיה באמצעות זרחון חמצוני היה מוחלש במידה ניכרת. דפוס דומה הופיע במודלים עכבריים של התקף לב: כאשר קשרו עורק כלונרי, IRF3 בתאי שריר הלב הופעל בעוצמה והגנים הנשלטים על ידו נדלקו. אפילו חלקיקי DNA מיטוכונדריאלי — שמשתחררים ממיטוכונדריות פגועות ומשמשים כ"אותות סכנה" פנימיים — הספיקו להפעיל את IRF3 בתאי לב מבודדים.
כביית IRF3 מגנה על הלב
כדי לבדוק האם פעילות IRF3 בתאי שריר הלב דווקא מחמירה את המחלה, הצוות הנדס עכברים שבהם ניתן היה להסיר את IRF3 רק מקרדיומיוציטים, בעוד תאי מערכת החיסון ותאי התמיכה נשארו שלמים. לאחר גרימת התקף לב, לעכברים אלה הייתה פונקציית שאיבה טובה יותר ופחות צלקת לעומת עכברים רגילים, למרות שהתאונה הראשונית הייתה זהה. בתאים לביים שגודלו במעבדה, השתקת IRF3 הורידה את ביטוי הגנים הדלקתיים מבלי לשבש חלבונים קשורים אחרים. יחד, תוצאות אלה תומכות בכך ש-IRF3 בתוך תא הלב עצמו אינו רק צופה מצד — הוא מעצים דלקת ונזק מבני לאחר איסכמיה ותורם למעבר לכשל לבבי.
כש-IRF3 "מדליק" תמידית, מערכת הדלק קורסת
המחברים הפכו את הניסוי: הם יצרו עכברים שבהם ניתן לכפות על IRF3 בקרדיומיוציטים להיות במצב פעילות תמידי באמצעות תחבולה גנטית "פוספומימטית". גם בלי גירוי חיצוני, עכברים אלה פיתחו במהירות החמרה חמורה בתפקוד הלב, רמות גבוהות של שליחים דלקתיים בדם ואותות לנזק תאי. בדיקה מעמיקה של רקמת ליבם הראתה שכאשר IRF3 פעיל כרונית, הוא מדכא מתאם אנרגיה מרכזי הנקרא PGC-1α. מולקולה זו בדרך כלל מקדמת מיטוכונדריות בריאות, שריפת שומנים יעילה ואיזון אנרגטי תאי. כאשר PGC-1α דוכא, מספר חלבונים מיטוכונדריאליים ירד, שרשרת העברת האלקטרונים התקלקלה, והעדפות הדלק של הלב השתנו: קרניטין ומרכיביו לשימוש בשומן ירדו, שימוש בקטונים נפגע והטיפול בגלוקוז התעקם. אפילו יחס ה-NAD⁺ ל-NADH — אינדיקטור מרכזי לאיזון החמצון-חיזור התאי — נטה לכיוון הבעייתי.
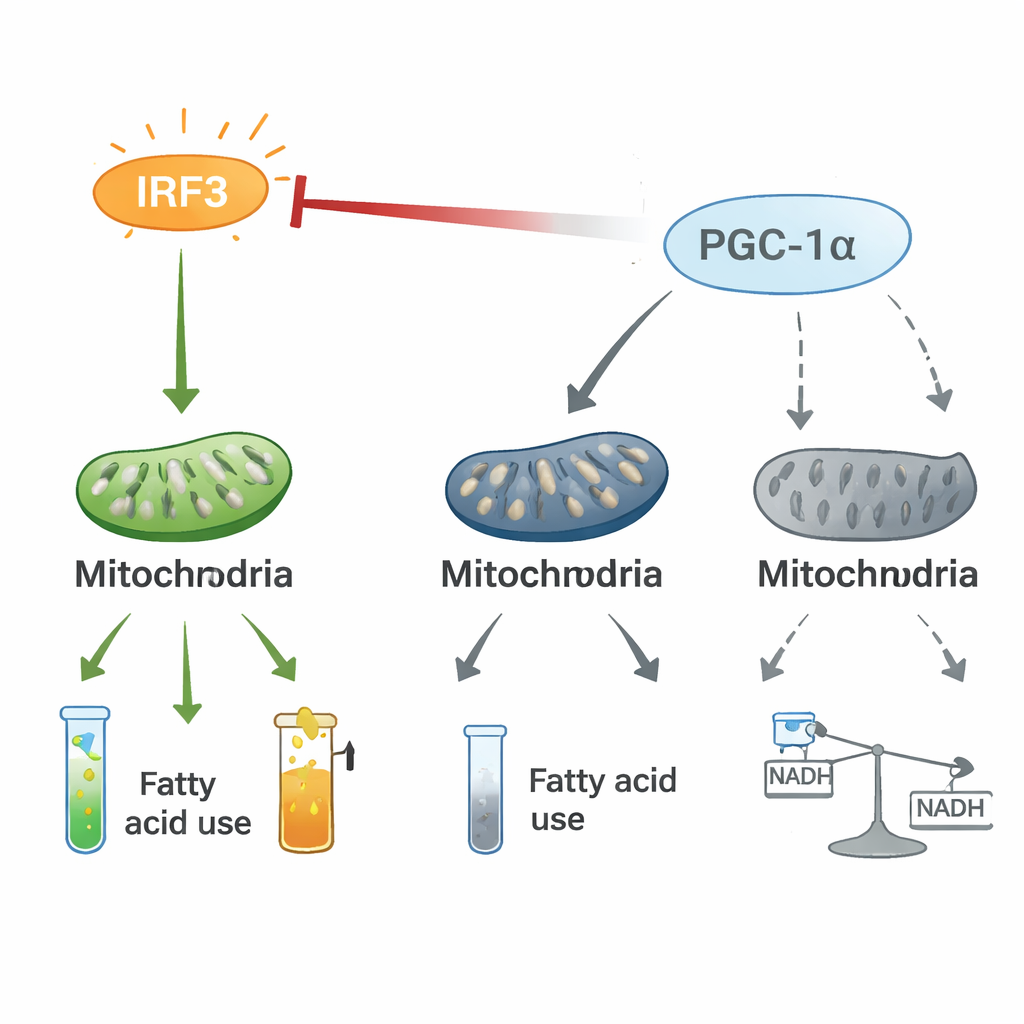
משיכת חבל בין דלקת לשליטה אנרגטית
ניסויים מכאניים חשפו כי IRF3 ו-PGC-1α יוצרים ציר רגולציה דו-כיווני. בתאי לב, IRF3 המופעל קשור באופן פיזי ל-PGC-1α ומחליש את יכולתו להפעיל גנים לשריפת שומנים. דיכוי IRF3 מעלה את רמות ופעילות PGC-1α, בעוד הגברה של PGC-1α מכבה גנים דלקתיים מונעי IRF3 ומשחזרת סימני מיטוכונדריה, גם תחת תנאי מאמץ כמו חוסר חמצן או רעלני חיידקים. מעקב איזוטופי יציב הראה שהפעלת IRF3 מנתבת מחדש פחמן ממסלולי ייצור אנרגיה רגילים דרך מעגל החומצה הציטרית למסלול חלופי — מסלול הפנטוזות־פוספט — ומפרה את זרימת המטבוליטים. משיכת החבל הזאת בין מתג פרו-דלקתי (IRF3) לבין שותף אנרגטי (PGC-1α) נראית כמעצבת את המטבוליזם של הלב בדרך שמעדיפה דלקת ואובדן אנרגיה.
טעינה עדינה של הסוללות של הלב
לבסוף, הצוות בדק האם דחיפה עדינה של PGC-1α חזרה למעלה יכולה לנטרל את הנזקים של IRF3. הם השתמשו בווקטור גנטי ממוקד לב כדי להעלות את PGC-1α במידה מתונה — אך לא מופרזת — באותם עכברים עם IRF3 היפראקטיבי. ההגברה הצנועה הזו שיפרה את פונקציית השאיבה, הגדילה חלבונים מיטוכונדריאליים, החזיקה גנים לשריפת שומנים ולמטבוליזם NAD, והקטינה ביטויי גנים דלקתיים ופיברוטיים. בניסויים תאיים, ביטוי משותף של PGC-1α עם IRF3 פעיל החזיר איזון בריא יותר של NAD⁺/NADH והחזיר את השימוש בדלק לכיוון שומנים. עבור קורא כללי, משמעות הדבר היא שטעינה זהירה של "מערכת ניהול הסוללה" של הלב יכולה לקזז חלקית את ההשפעות המזיקות של מתג דלקתי כרוני שנתקע במצב "מדלוק".
מה משמעות זה לטיפול עתידי בכשל לב
עבודה זו מציבה את IRF3 כקשר מרכזי בין דלקת לכשל אנרגיה בתוך תאי שריר הלב. במקום לטפל בדלקת ובמטבוליזם כבעיות נפרדות בכשל לב, המחקר מרמז שהן משולבות דרך ציר IRF3–PGC-1α. אמנם הממצאים מתקבלים בעכברים ובתאים, אך הם מעלים את האפשרות שטיפולים עתידיים יוכלו או לכבות את פעילות IRF3 או לחזק את PGC-1α ואת תפקוד המיטוכונדריה כדי להאט או למנוע כשל לב לאחר התקף. במילים פשוטות, להרגיע מערכת אזעקה תאית פעילה יתר על המידה ולתמוך בתחנות האנרגיה של הלב עשויים להיות אסטרטגיה משולבת חזקה כדי לשמור על לבים מוחלשים פעילים לאורך זמן.
ציטוט: Kumari, M., Evangelakos, I., Deshpande, A. et al. Activation of IRF3 in cardiomyocytes impairs mitochondrial oxidative function through PGC-1α inhibition and drives heart failure. Nat Commun 17, 2051 (2026). https://doi.org/10.1038/s41467-026-69792-4
מילות מפתח: כשל לב, דלקת, מיטוכונדריה, תאי לב (קרדיומיוציטים), PGC-1α