Clear Sky Science · he
אנלוגים לא־מתכלים של אצטילליזין לחקר אצטילציה של חלבונים מבחוץ ובתאים
מדוע תגיות כימיות זעירות על חלבונים חשובות
בתוך כל תא, חלבונים עוברים באופן מתמיד שינוי עם תגיות כימיות קטנות שפועלות כמו מפסקי הדלקה/כיבוי או דימרים לפעילותם. אחת מהתגיות החשובות הללו נקראת אצטילציה, שיכולה לשנות את התנהגות החלבון מבלי לשנות את הקוד הגנטי הבסיסי שלו. קשה להבהיר בדיוק מה עושה אצטילציה בנקודה ספציפית על חלבון מסוים, כי תאים מסוגלים להסיר תגיות אלה מהר כמעט באותה מהירות שבה מוסיפים אותן. עבודה זו מציגה מחדל כימי חכם לאצטילציה שאינו ניתן להסרה, ומעניק לכלים לקיבוע אותם מפסקים ולבחון מה קורה לאחר מכן.
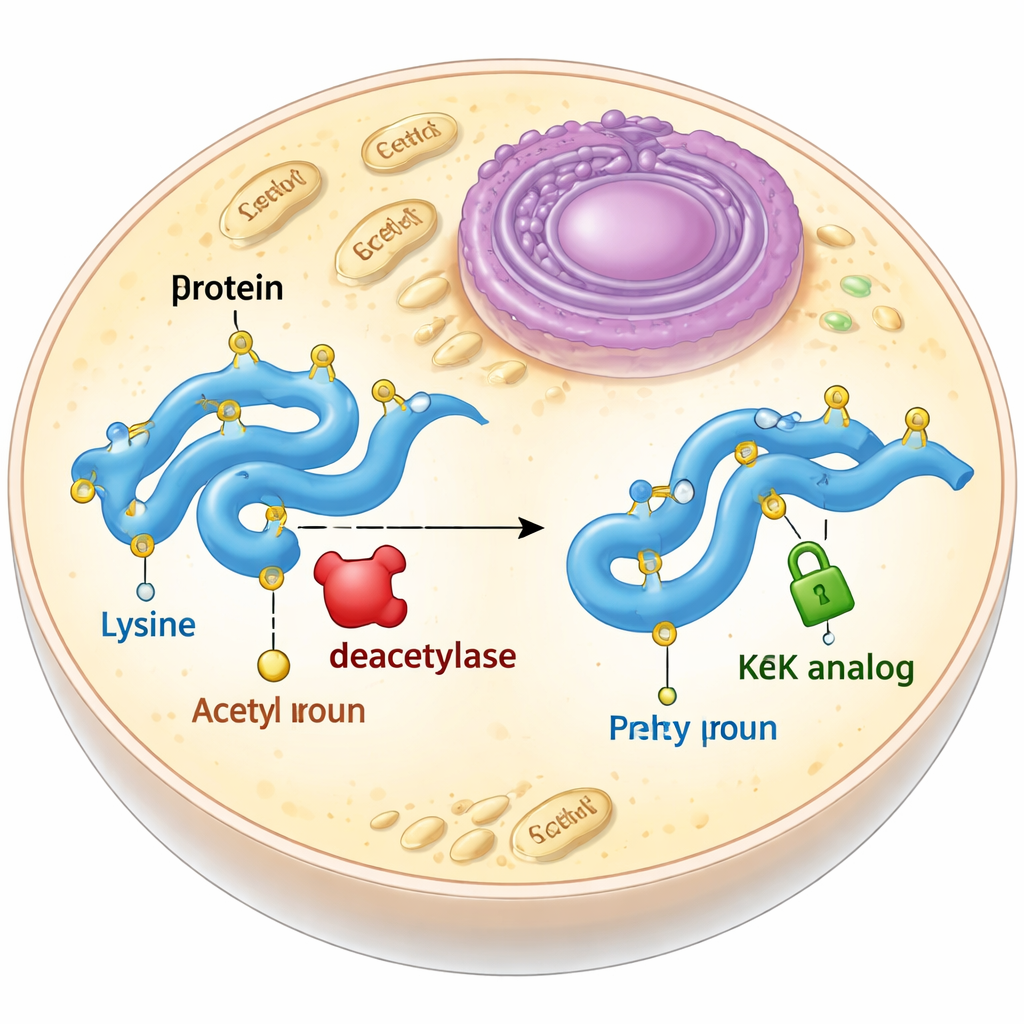
תחליף יציב לתג חמקמק
אצטילציה בדרך כלל מתרחשת על חומצת אמינו שנקראת ליזין. כאשר ליזין מוסרכת באצטיל, היא מאבדת את המטען החיובי ושרשרת הצד שלה מתארכת מעט. ביולוגים לעתים מנסים לדמות זאת על ידי החלפת ליזין בחומצת אמינו אחרת, גלוטמין, שאינה טעונה אך קצרה יותר, או על ידי הכנסת אצטילליזין אמיתי באמצעות הרחבת הקוד הגנטי. לשתי הגישות יש חסרונות: גלוטמין אינו משחזר במלואו את השינויים הצורתיים שגורמת האצטילציה, ואצטילליזין אמיתי מופרד במהירות על־ידי אנזימים בשם דיאצטילאזות בתוך תאים. החוקרים שאפו לתכנן ולבחון אנלוגים של אצטילליזין שומרי צורה ונפח אך אינם ניתנים להסרה.
בדיקת חיקויים כימיים חדשים על חלבון מודל
הצוות התמקד תחילה בווביקוויטין, חלבון קטן ונחקר היטב שמקבל עצמו סימונים רבים. באמצעות הנדסה גנטית מתקדמת הם הציבו וריאנטים של ליזין במיקום אחד בווביקוויטין: אצטילליזין טבעי, שני אנלוגים שאינם ניתנים להסרה בשם TFAcK וקטוליזין (KeK), וכן תחליפים נפוצים כגון גלוטמין, אלנין וארגינין. לאחר מכן בחנו כיצד השינויים האלה השפיעו על הצורה והתפקוד של הוביקוויטין. מדידות NMR ברזולוציה גבוהה הראו שאצטילליזין, TFAcK ו‑KeK יצרו שינויים מבניים כמעט זהים, בעיקר סביב הליבת ההליקס, בעוד שגלוטמין ומוטציות פשוטות אחרות לא עשו זאת. מבחני תפקוד באמצעות אנזים בשם HDM2 חשפו שהוביקוויטין הנושא אצטילליזין, TFAcK או KeK התנהג באופן דומה זה לזה ושונה מגרסת הגלוטמין, מה שמדגיש שאורך ונפח שרשרת הצד — לא רק מטען — הם קריטיים.
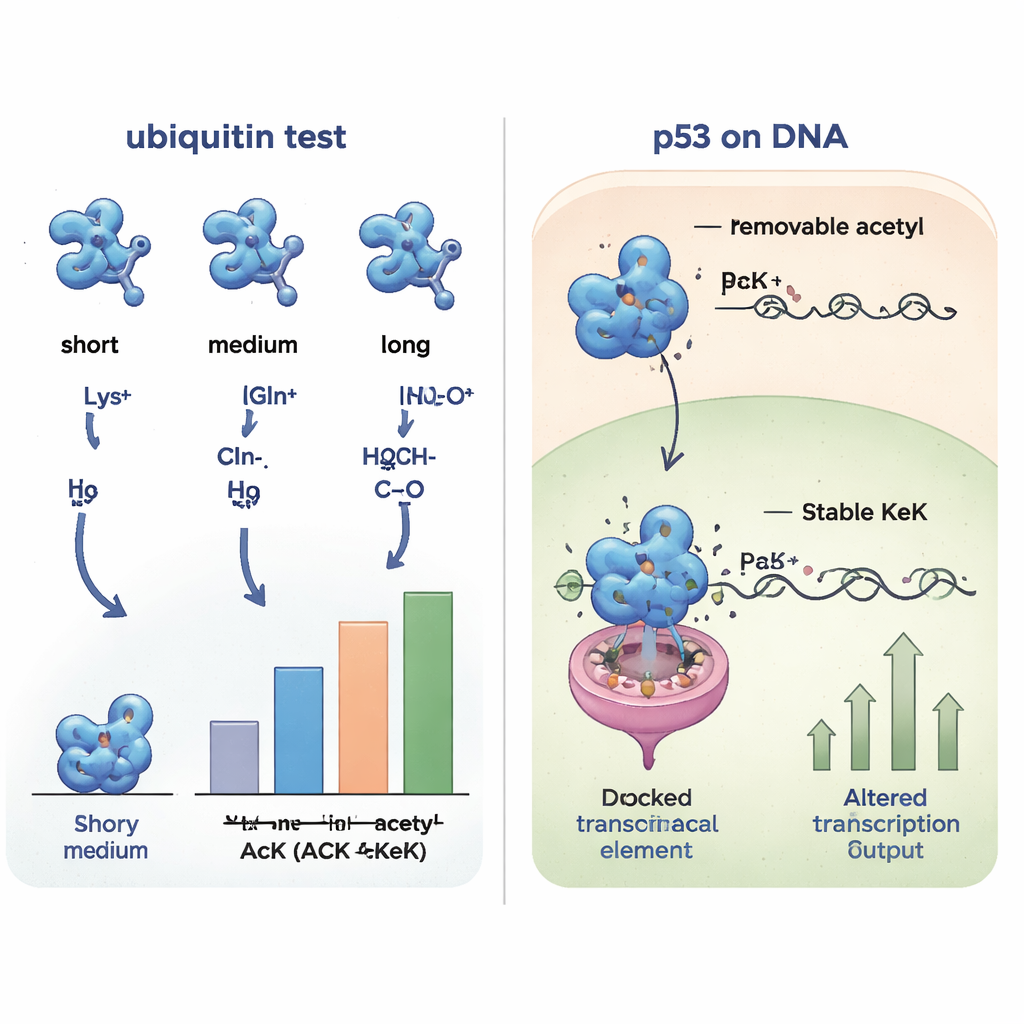
בדיקת שותפויות חלבון ברחבי התא
מכיוון ששינויים מבניים קטנים יכולים לשנות אילו שותפים חלבון יתקשר איתם, החוקרים השוו לאחר מכן כיצד גרסאות הוביקוויטין השונות קושרות חלבונים אחרים מתוך תמציות תאים אנושיות. על ידי שליפת שותפי קשירה וזיהוים במסת ספקטרומטרית, הם מצאו שהוביקוויטין המכיל אצטילליזין, TFAcK או KeK חלק דפוסי אינטראקציה דומים מאוד, בעוד שצורות המכילות גלוטמין או אלנין התקבצו יחד ונראו שונות. וריאנטים בעלי מטען חיובי (ליזין או ארגינין) יצרו קבוצה נוספת. השוואה שיטתית זו הראתה כי האנלוגים הבלתי־נמחקים TFAcK ובמיוחד KeK מחקים הן את המבנה והן את התנהגות הקשירה של אצטילציה אמיתית טוב בהרבה מההחלפה המסורתית בגלוטמין.
קיבוע אצטילציה על מדכא הגידולים p53
כדי לבדוק האם כלים אלה פועלים בתוך תאים חיים, החוקרים פנו ל‑p53, מדכא גידולים מרכזי הנקרא לעתים קרובות "שומר הגנום". ליזינים ספציפיים באזור הקושר‑DNA של p53 יכולים לעבור אצטילציה, מה שמזיז את קבוצת הגנים שהוא מפעיל, כגון אלו שעוצרים את מחזור התא או מפעילים מוות תאי. הצוות מהנדס תאים אנושיים כך ש‑p53 ישלב אצטילליזין, TFAcK או KeK בשני מיקומי ליזין חשובים (120 ו‑164) רק כאשר חומצת האמינו הלא‑סטנדרטית המתאימה ניתנה. את שלושתן היה ניתן לשלב ב‑p53, אך מדידות מדוקדקות הראו שבתאים קבוצות האצטיל וה‑TFAcK הוסרו ברובן על‑ידי דיאצטילאזות, בעוד ש‑KeK נשאר שלם. כאשר בדקו את יכולת p53 להפעיל גן מדווח ואת הגן הטבעי p21, הווריאנטים הנושאים KeK באתרים אלה היו פחות פעילים במידה רבה, התואם למה שמצפים כאשר אצטילציה באותם מיקומים מקובעת, בעוד שאצטילליזין ו‑TFAcK התנהגו יותר כמו p53 הרגיל כי הוסרו מהם האצטילים.
מסקנות לגבי חקר החלטות תאיות
בסך הכל, המחקר מראה ש‑KeK הוא תחליף נאמן ובלתי־ניתן־להסרה של אצטילליזין: הוא משחזר בצמוד את השינויים המבניים, העדפות הקשירה והתוצאות התפקודיות של האצטילציה, אך אינו ניתן למחיקה על‑ידי אנזימי התא. לקהל שאינו מומחה, משמעות הדבר היא שלחוקרים יש כעת דרך "להקפיא" מתג כימי הפיך במקום יחיד על חלבון ולראות כיצד זה משפיע על תהליכים כמו ויסות גנים והחלטות גורל תאיות. זה אמור להקל מאוד על הפרדת התפקידים הספציפיים של אצטילציה מאלו של שינויים חופפים אחרים, ועלול בסופו של דבר להבהיר כיצד אצטילציה של חלבונים המופרעת תורמת למחלות כמו סרטן.
ציטוט: Kienle, S.M., Sigg, M., Schneider, T. et al. Non-hydrolyzable acetyllysine analogs to study protein acetylation in vitro and in cells. Nat Commun 17, 1985 (2026). https://doi.org/10.1038/s41467-026-69782-6
מילות מפתח: אצטילציה של חלבונים, שינוי אחרי־תרגום, וביקוויטין, p53, הרחבת הקוד הגנטי