Clear Sky Science · he
שכתוב דינמי של הטרנסקריפטום בתאי אבות עצביים אנושיים מושתלים חושף מנגנונים לשימור הראייה במודל עכברוש של רטיניטיס פיגמנטוזה
למה חשוב להגן על ראייה שנחלשת
רטיניטיס פיגמנטוזה היא קבוצה של מחלות תורשתיות שמדירות באיטיות את הראייה של האנשים, לעתים מתחילות בעיוורון לילה ומתקדמות לעיוורון חוקי. מאחר שמאות מוטציות גנטיות שונות עלולות לגרום למצב זה, קשה לטפל בכל אחת מהן בנפרד באמצעות טיפול גנטי. המחקר בוחן גישה רחבה יותר: השתלת תאי אבות עצביים אנושיים — תאים עצביים לא בשלבים שגודלו במעבדה — לעין כדי להגן על התאים החושיים שנותרו. הבנת האופן שבו התאים המושתלים מתנהגים וכיצד הם מסייעים לשימור הראייה יכולה לעצב טיפולים עתידיים לא רק לרטיניטיס פיגמנטוזה אלא גם להפרעות עיוורון אחרות.
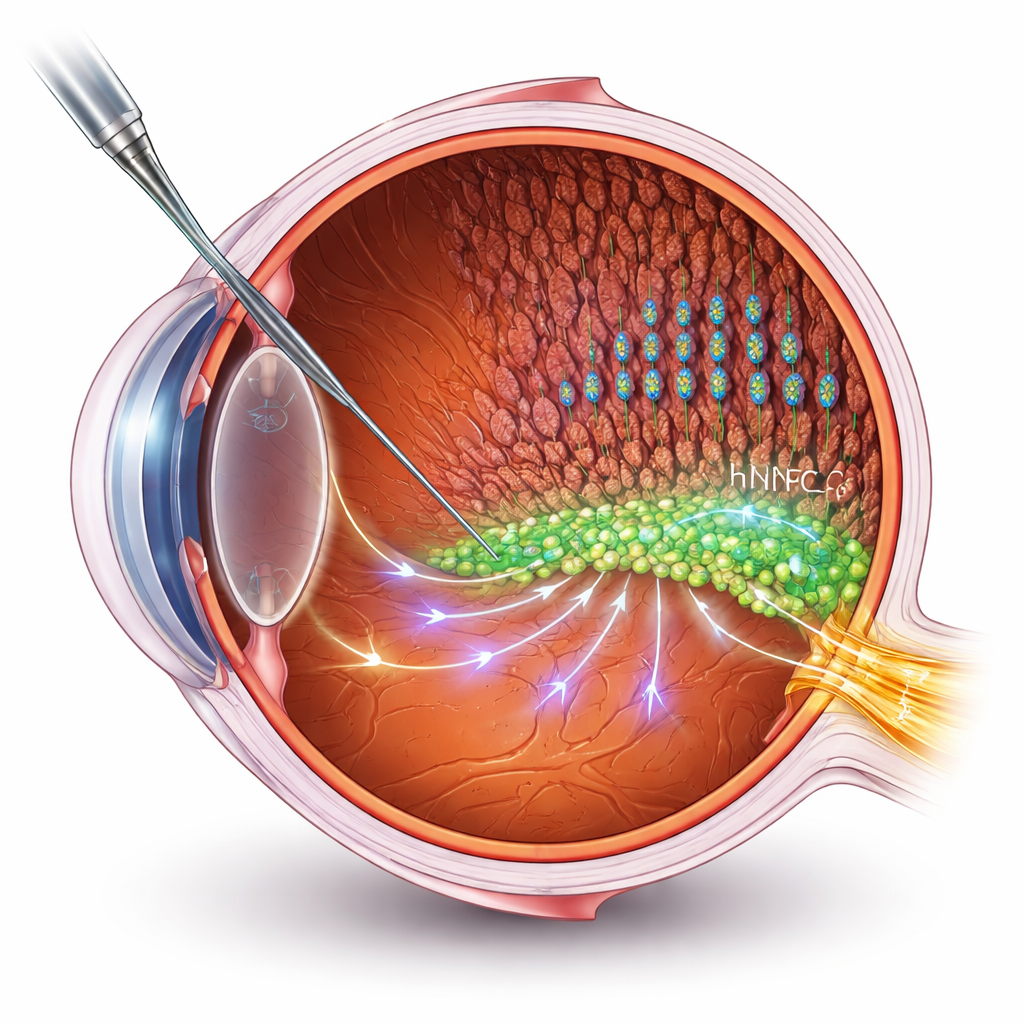
לעזור לתאים במקום להחליפם
רבות מהתרפיות בתאי גזע שואפות להחליף תאים מתים או פגועים. אך במחלות רשתית מתקדמות, יצירת חיבורים חדשים למוח מהווה אתגר טכני מרכזי. כאן החוקרים נוקטים גישה אחרת: שימוש בתאי אבות עצביים אנושיים (hNPCs) כ"עוזרים" שתומכים בתאי הרשתית של הנבדק. הם השתילו hNPCs במרחב התת-רשתיתי במודל עכברוש ידוע של רטיניטיס פיגמנטוזה, ולאחר מכן מדדו ראייה באמצעות הקלטות חשמליות ומבחני התנהגות. החולדות שטופלו שמרו על תפקוד ראייה טוב יותר ועל שכבות פוטורצפטורים (מקלות וקנים) שלמות יותר מאשר בעלי חיים שלא טופלו, אף על פי שהניוון המשיך להתקדם לאט.
כיצד התאים המושתלים משתנים בתוך העין החולה
כדי להבין מה קורה ברמת המולקולות, השתמשו החוקרים בריצוף RNA חד-תאי, טכניקה שמאפיינת אילו גנים מופעלים באלפי תאים בודדים. הם עקבו אחר ה-hNPCs המושתלים בשני נקודות זמן, בערך בשלבים מוקדמים ומאוחרים אחרי ההשתלה. במקום להפוך לפוטורצפטורים חדשים, רוב התאים המושתלים בגרו לתאים תומכים דמויי אסטרוציטים, כאשר חלק קטן הראה סימנים של אוליגודנדרוציטים או נוירונים בלתי בשלים. עם הזמן התאים האלה התייצבו, ואימצו תכונות המצביעות על התאמה לשרוד בסביבה מתישה ומתנוונת וגם על יכולת אינטראקציה קרובה עם תאי רשתית סמוכים.
אותות מגן, מטבוליזם וניקוי
ה-hNPCs ייצרו תערובת עשירה של חלבונים מגנים הידועים כגורמי תזונה (trophic factors). בתוכם נמצאו MANF ו-MYDGF, הקשורים להישרדות תאים, להקטנת מתח חמצוני ולהרגעת דלקת, וכן גורמים אחרים כמו מידקין ופליאוטרופין התומכים בצמיחה ותנועה של תאים עצביים. מולקולות אלו נראות פועלות הן על הגרף עצמו והן על הרשתית שמסביב. בחולדות שטופלו, מקלות וקנים הראו דפוסי ביטוי גנטי הקרובים יותר לבקרים בריאים, עם שיפור בתמיכה של סיגנול חזותי ותחזוקת תאים. התאים המושתלים גם חיזקו מסלולים המעורבים בניקוי שברי תאים ובהתאמת מטבוליזם, מה שמרמז שהם מסייעים לפוטורצפטורים להתמודד עם דרישות אנרגטיות וחומרי לוואי רעילים המצטברים במהלך המחלה.
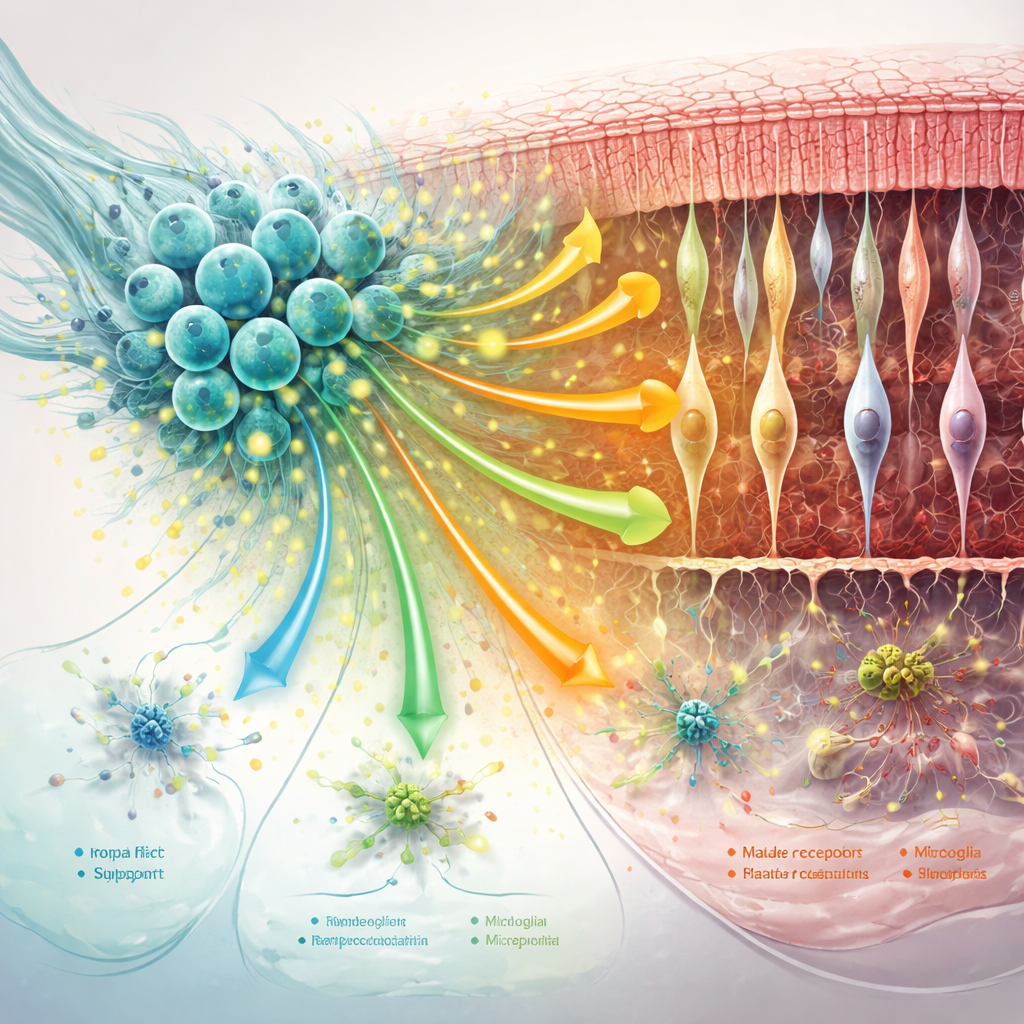
הרגעת תאי תמיכה ושינוי סביבת הרשתית
רשת התמיכה של הרשתית — גליה של Müller, מיקרוגליה ומטריצת החלבונים הסובבת — משחקת תפקיד מרכזי בהחמרת או בהאטת הניוון. המחקר מצא שטיפול ב-hNPC האט סימני מפתח של שינויים "ריאקטיביים" מזיקים בגליה של Müller והטה את המיקרוגליה ממצבים דלקתיים-יתר, במיוחד בנקודות הזמן המוקדמות. במקביל התחזקו אותות תקשורת המסייעים לייצוב סינפסות, להיצמדות התאים זה לזה ולשמירת המצע סביב הפוטורצפטורים. כאשר המחלה התקדמה, חלק מהיתרונות הללו דעכו: התקשורת בין תאים נחלשה באופן כללי, מסלולי הגנה מסוימים — כולל אותות הקשורים ל-MANF — ירדו, ותאי התמיכה נטו יותר לפרופילים ממוקדי לחץ וחיסון.
משמעות הדבר לטיפולי עיניים בעתיד
ללא-מומחה, המסר המרכזי הוא שתאי אבות עצביים אנושיים מושתלים יכולים לפעול כמו "מגיבים ראשונים" מקומיים ברשתית המתנוונת. הם לא בונים מחדש את הרשתית מאפס, אבל משחררים מולקולות מגנות, מותאמים מטבולית, מרגיעים דלקת מזיקה ועוזרים לשמור על המבנה המקומי — כל אלה מאטים את איבוד הראייה. עם זאת, האפקט המגן פוחת עם הזמן ככל שהסביבה נעשית עוינת יותר ודיאלוג בין הגרף לתאי המאחסן נחלש. המחברים מציעים שהגברת גורמים מרכזיים כגון MANF ושיפור בריאות הרשתית של המאחסן — יתכן באמצעות הנדסה גנטית של הגרף או טיפולים משולבים — עשויים להיות חיוניים כדי להפוך את ההקלה הזמנית לשימור ראייה ממושך.
ציטוט: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
מילות מפתח: רטיניטיס פיגמנטוזה, טיפול בתאי גזע, ניוון רשתית, הגנה עצבית, ריצוף RNA חד-תאי