Clear Sky Science · he
חתימות הכללת אקסונים מאפשרות הערכה מדויקת של פעילות גורמי החיתוך
קריאת סימני העריכה הנסתרים של התא
כל תא בגופנו עורך באופן מתמיד את הודעות ה‑RNA שלו לפני שהופכת אותן לחלבונים. עריכה זו, הנקראת ספלייסינג, מסייעת להחליט האם תא נשאר בריא או הופך לסרטני. המחקר שמאחורי מאמר זה מראה כי על ידי בחינה מדויקת של אילו חלקי RNA נשמרים או מדלגים עליהם — המכונים חתימות הכללת אקסונים — מדענים יכולים להסיק במדויק את פעילות ה"עורכים" המולקולריים השולטים בספלייסינג, גם במצבים מורכבים כמו סרטן.
איך תאים גוזרים ומדביקים את ההודעות שלהם
גנים אינם נקראים כרצף רציף אחד. במקום זאת התאים מסירים מקטעים שאינם מקודדים ומחברים ביחד מקטעים מקודדים, המוכרים כאקסונים, כדי לבנות את הודעות ה‑RNA הסופיות. חלבונים מיוחדים הנקראים גורמי חיתוך מנחים את תהליך הגזירה וההדבקה הזה, וקובעים אילו אקסונים ייכללו. התנהגותם מושפעת מהרבה שכבות של ויסות: כמה מRNA שלהם ומחלבון שלהם מיוצר, אילו שינויים כימיים עוברים, היכן הם ממוקמים בתא וכיצד הם מתקשרים עם חלבונים אחרים. מכיוון שיש כל כך הרבה מנגנונים שיכולים לשנות את התנהגות גורמי החיתוך, מדידה של סוג נתון אחד בלבד — כמו ביטוי גני — נוטה שלא לחשוף מה הם באמת עושים.
הפיכת דפוסי אקסון לקריאות פעילות
בהשראת עבודות קודמות על גורמי שעתוק, המחברים מציעים אסטרטגיה שונה: במקום לנסות למדוד את גורמי החיתוך ישירות, לקרוא את פעילותם מהשפעותיהם. כאשר גורם חיתוך משתנה, הכללה של האקסונים המטרה שלו משתנה בדפוסים המזהים בקלות. הצוות ריכז מאות ניסויים שבהם גורמי חיתוך ספציפיים הושתקו, הוסרו או הובאו לביטוי גבוה, והשתמש בנתונים אלה כדי לבנות "רשתות אמפיריות" המקשרות כל גורם לאקסונים שהוא משפיע עליהם בבירור. לאחר מכן הם התאימו מסגרת חישובית שנקראת VIPER כדי לקרוא חתימת הכללת אקסונים חדשה ולתעד את מידת הפעילות של כל גורם חיתוך הנדרשת כדי להסביר את הדפוס הנצפה.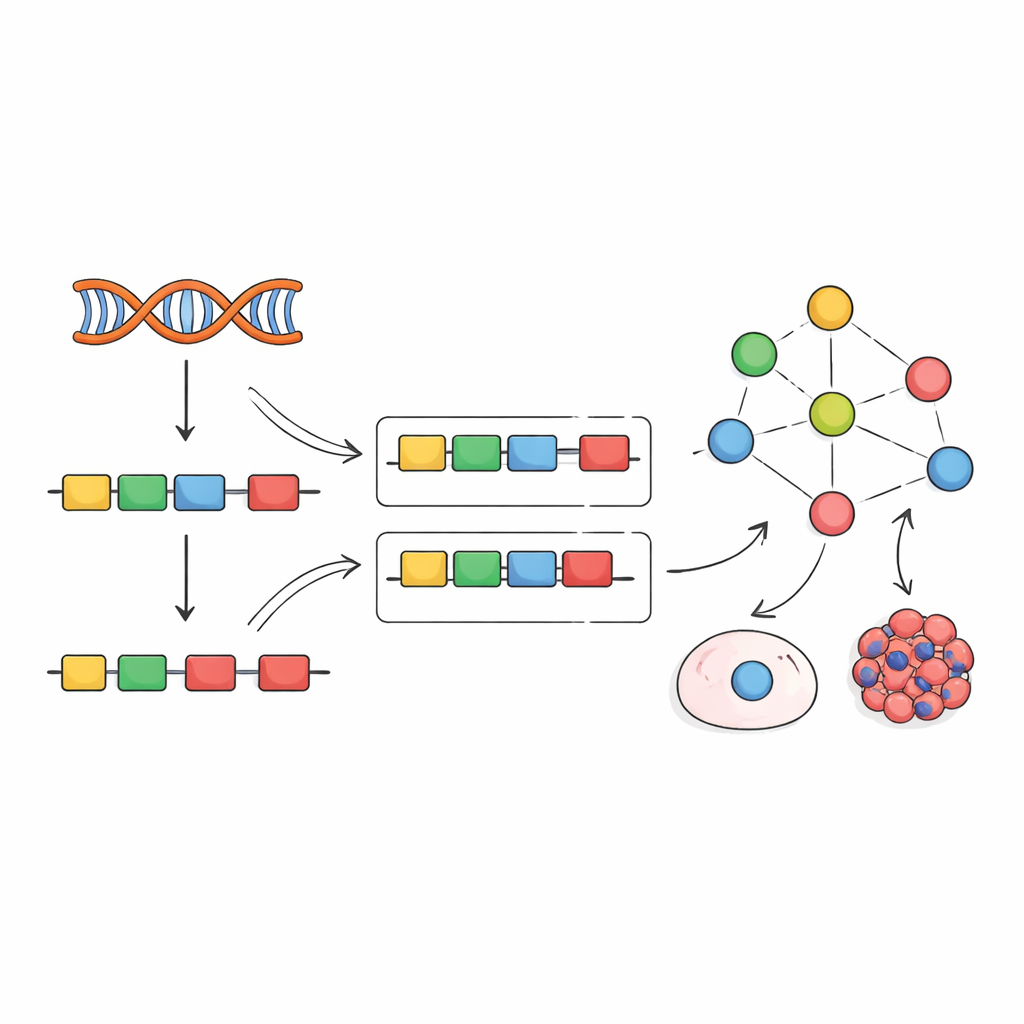
בדיקת השיטה בהפרעות מהעולם האמיתי
כדי לבדוק האם גישה זו עובדת, החוקרים בדקו מספר דרכים לבניית רשתות ולחישוב ציון פעילות. רשתות אמפיריות שמקורן ישירות בניסויי הפרעה, בצירוף ניתוח ההעשרה של VIPER, עלו בבירור על חלופות המבוססות על הסקת מסקנות סטטיסטית בלבד. השיטה זיהתה נכון את גורם החיתוך שהופרע בניסוי ברוב המבחנים, גם בין סוגי תאים ומחקרים שונים. היא גם לקחה בחשבון מנגנוני ויסות עדינים יותר. לדוגמה, תרופה נגד סרטן בשם Indisulam גורמת לפירוק חלבון גורם החיתוך RBM39 בעוד שרמות ה‑RNA שלו עולות, כנראה בניסיון פיצוי. ניתוח ביטוי מסורתי עשוי להטעות ולרמוז ש‑RBM39 פעיל יותר, אך ציון הפעילות המבוסס על אקסונים חשף נכון אובדן תפקוד חזק, התואם את מנגנון הפעולה הידוע של התרופה.
חשיפת תכניות חיתוך חבויות בסרטן
מצוידים בכלי זה, המחברים פנו ל־The Cancer Genome Atlas, ניתחו נתוני רמה‑אקסון ממספר סוגי גידולים ורקמות בריאות תואמות. הם גילו שתי תכניות חיתוך רחבות וחוזרות. תוכנית אחת כוללת גורמי חיתוך שנטו להיות פעילים יותר בגידולים ומשויכת להישרדות לקויה של המטופלים — תוכנית הדומה לתכונות אונקוגניות. השנייה מאופיינת בגורמים שפועלים באופן שיטתי פחות בגידולים וקושרת לתוצאות טובות יותר, בדומה לחלבוני מדכאי גידול. תכניות אלה משפיעות על גנים המעורבים במאפיינים בסיסיים של סרטן כגון חלוקה תאית מהירה ויכולת הגידול להתחבא ממערכת החיסון. לדוגמה, כמה אקסונים שמווסתים תוכנית הדומה לחלבוני מדכאי גידול נראים משפיעים על מידת התגובה של מטופלים לטיפולי חיסון עיכוב נקודות בדיקה, מה שמצביע על סמנים חדשים או נקודות התערבות אפשריות.
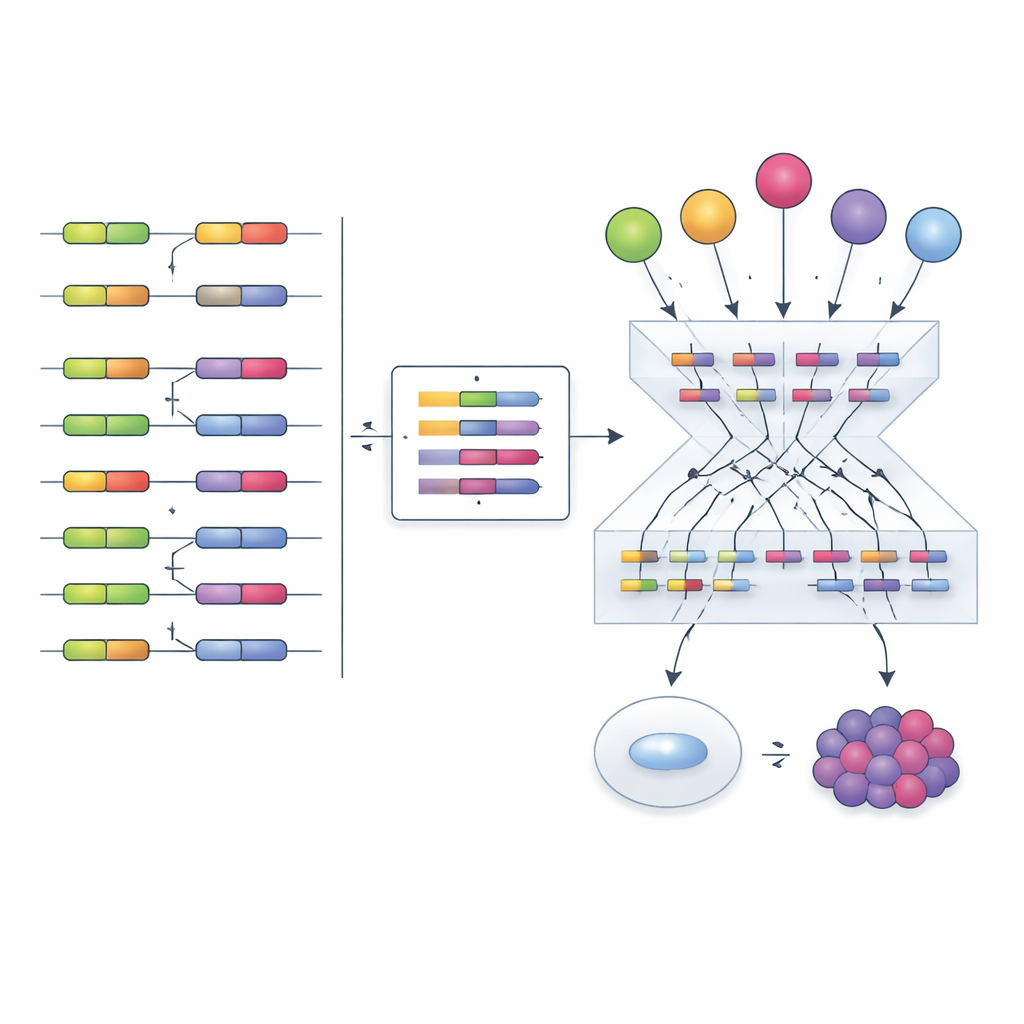
מעקב אחר שינויים בחיתוך לאורך הדרך אל הסרטן
הצוות בדק גם מודל שלב‑אחר‑שלב של תאים אנושיים המתקדמים ממצב נורמלי דרך אימורטליזציה, היווצרות גידול ובסופו של דבר גרורות. הם גילו שתוכנית החיתוך הדומה לאונקוגנית הופכת פעילה יותר ככל שהתאים צוברים מוטציות המניעות סרטן, בעוד שתוכנית הדומה למדכאי גידול דועכת. על‑ידי שילוב שכבות נתונים מרובות — רמות RNA, שפע חלבונים, שינויים כימיים ושינויים בחיתוך בתוך גורמי החיתוך עצמם — הם זיהו סט ממוקד של אירועים מולקולריים מועמדים שעשויים להניע את המעברים בתכניות הללו, והציעו רשימה ממומנת לניסויים עתידיים.
מדוע זה חשוב למטופלים ולמחקר עתידי
בעצם, המחקר מראה שניתן לדחוס את ההתנהגות המורכבת של גורמי החיתוך לציון פעילות אחד, ניתן להבנה, הנגזר מאופן הכללת או דילוג על אקסונים. זה מאפשר לחקור ויסות חיתוך בקohortes גדולות של מטופלים ובניסויים מגוונים בעזרת נתוני רצף RNA סטנדרטיים בלבד, מבלי לדרוש פרופיל מולטי‑אומיקס יקר. עבור קורא שאינו מומחה, המסר המרכזי הוא שדפוסים באופן שבו גנים נחתכים ומודבקים נושאים מידע עשיר על מערכות הבקרה הנסתרות של התא, ופיענוח דפוסים אלה יכול לחשוף מנועי סרטן חדשים, לשפר פרוגנוזה ולהנחות את החיפוש אחרי טיפולים מדויקים יותר.
ציטוט: Anglada-Girotto, M., Segura-Morales, C., Moakley, D.F. et al. Exon inclusion signatures enable accurate estimation of splicing factor activity. Nat Commun 17, 1994 (2026). https://doi.org/10.1038/s41467-026-69642-3
מילות מפתח: חיתוך RNA, גורמי חיתוך, גנומיקה של סרטן, טרנסקריפטומיקה, אבחון פעילות חלבון