Clear Sky Science · he
אותות סידן פירימידינרגיים מקשרים בין מטבוליזם של השופכן לצלקתיות במחלות כליה
מדוע צלקות בכליה חשובות
מחלת כליה כרונית משפיעה בשקט על מאות מיליוני אנשים בעולם ולעתים מסתיימת בכך שהכליות נהיות מקועקעות ונוקשות. ברגע שהצלקתיות, הנקראת פיברוזיס, משתלטת, קשה להשיב את תפקוד הכליה שאבד. ועדיין לרופאים אין תרופות שמכוונות באופן ספציפי לעצירת הפיברוזיס. המחקר הזה שואל שאלה בסיסית אך מכרעת: כיצד נזק קצר־טווח לצינורות הסינון של הכליה הופך בהדרגה לרקמת צלקת מתמשכת, והאם קטיעת השרשרת הזו יכולה להאט או למנוע את כשל כליה?
צינורות כליה עסוקים והכימיה המוסתרת שלהם
הנפרונים המוצאיים של הכליה הם יחידות זעירות שעושות את מרבית העבודה בשחזור מים וחומרים מזינים שסוננו מתוך הדם. כדי להניע את העבודה הזו, פעילות הכימיה בתאים אלה גבוהה מהרגיל. בניתוח ביטוי גנים בתא בודד בכליות עכברים, החוקרים מצאו שתאי הצינור עשירים במיוחד בגנים הקשורים בניהול פירימידינים, משפחה של מולקולות קטנות שתפקידן בנייה ותיקון של DNA ו‑RNA. בתאים פגועים בצינורות, אנזים אחד במסלול "הצלה" — דזמינאז של ציטידין — הוגבר באופן חד, מה שמרמז שתאים פגועים מארגנים מחדש את השימוש בפירימידינים כדי לשמור על רמות של כמה אבני בניין עשירות באנרגיה, כולל מולקולה בשם UDP.
אותות שנשפכים מתוך תאים פגועים
כאשר הצוות פגע בתאי צינור אנושיים מדומים במעבדה ברעלים המדמים כימותרפיה או מנת יתר של חומצה פולית, התאים שיחררו UDP לנוזל שמסביבם. בכליות עכבר שנחשפו לפגיעה, צביעת פרוסות רקמה הראתה הן רמות גבוהות של האנזים המטפל בפירימידינים בצינורות והן סימנים שתאי תמיכה שכנים, הקרויים פיברובלסטים, התעוררו ומשנים צורה. פיברובלסטים בדרך כלל שוכנים ברוגע בין הצינורות, אך כשהם פעילים הם מתרבים ותורמים להפקיד קולגן וסיבים אחרים שמעבים ומקשיחים את רקמת הכליה. התצפיות הללו הציעו רעיון פשוט: יתכן שהצינורות הפגועים "שופכים" אותות מצוקה כימיים שהפיברובלסטים השכנים יכולים לחוש.
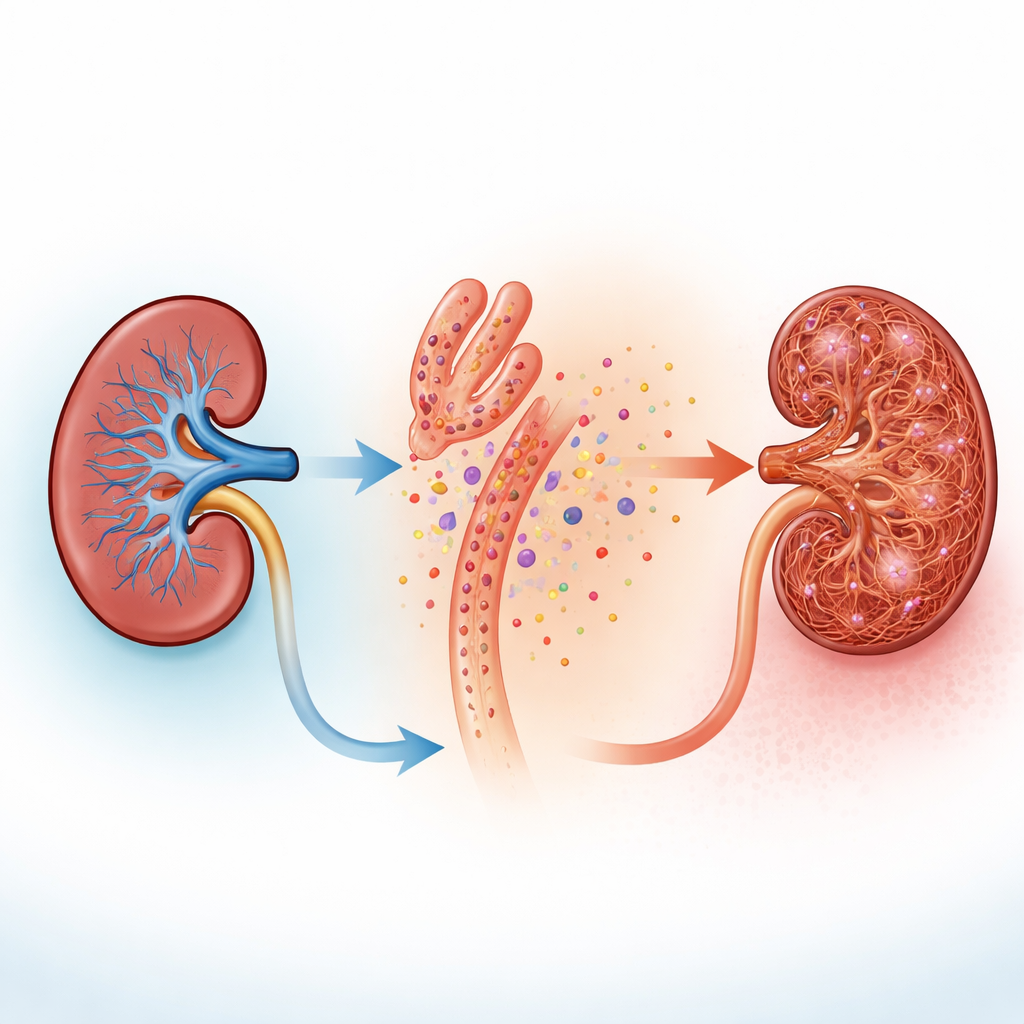
כיצד פיברובלסטים מקשיבים דרך פרצי סידן
"האוזניים" המחשדות על הפיברובלסטים הן קולטני P2Y6, חלבונים על פני השטח שמגיבים ל‑UDP. בכריית מספר מאגרי נתוני תא בודד, המחברים ראו כי P2Y6 מופיע בתאי סטרומה ועלה אף יותר במודלים של מחלת כליה כרונית בעכברים. מדידות ברחבי כליות שלמות אישרו עלייה חזקה ברמות P2Y6 בשני מודלים שונים של צלקתיות. בפרוסות כליה טריות ובפיברובלסטים תרביתיים שהונדסו להאיר כאשר ריכוז הסידן בתא עולה, הוספת UDP או חומר שמפעיל את P2Y6 יצרה התפרצויות מהירות של סידן. הפרצים האלו התחילו בתהליכים הארוכים והדקים העוטפים צינורות ואז עברו לגוף התא, והם נעלמו כאשר חסמו את P2Y6 או כאשר ספגו כימית את הסידן. בעכברים חיים, מיקרוסקופיה אינטרוותלית ברזולוציה גבוהה הראתה שפיברובלסטים סביב צינורות מציגים פעילות סידן תכופה ולא סדירה שמתגברת באופן דרמטי כשהצינורות נפגעים, גם כאשר תאי הצינור עצמם שותקים.
מאותות קצרים לצלקות מתמשכות
פרצי סידן בתוך תא אינם רק מופע ראווה; הם יכולים לתכנת מחדש התנהגות. כאשר פיברובלסטים בתרבית הושרו בחומר שמפעיל את P2Y6, הם התרבו מהר יותר, זזו בקלות רבה יותר והפעילו גנים הקשורים למצב תוקפני יותר של "מיאופיברובלסט". גנים אלה מקודדים חלבונים כגון פיברונקטין, וימנטין וקולגן התורמים ישירות להיווצרות צלקת. חסימת P2Y6 או מניעת עליות הסידן ביטלה את השינויים הללו, והדיכוי הגנטי של הקולטן החליש את התגובה. בעכברים, שתי צורות שונות של פגיעה בכליה — חסימת שופכן ונפרופתיה עקב חומצה פולית — הראו את אותה תמונה: כליות פגועות הכילו פיברובלסטים מתרבים יותר, סמני מיאופיברובלסט רבים יותר, יותר קולגן ואזורים גדולים יותר של פיברוזיס.
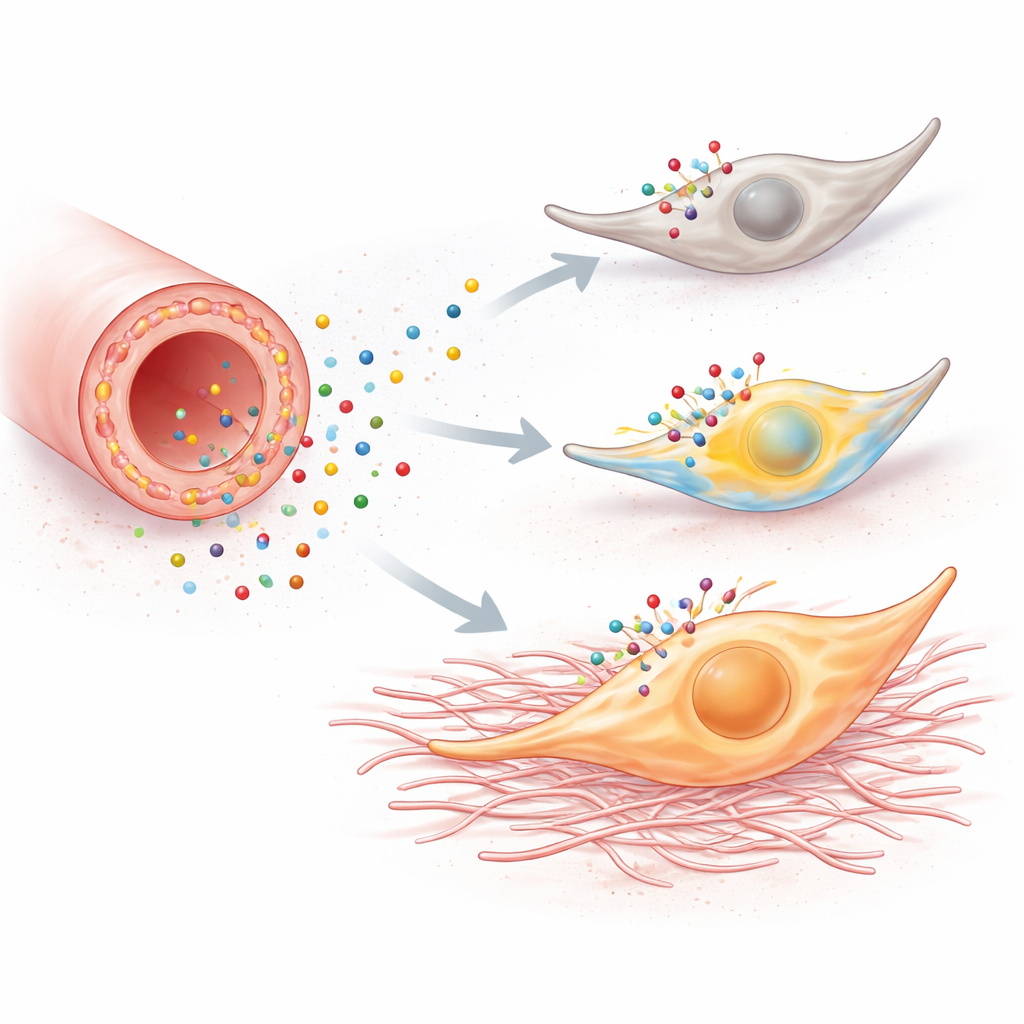
הנמכת עוצמת האותות המזיקים
כדי לבדוק האם המסלול הזה אינו רק קיים אלא אכן מזיק, החוקרים או הסירו את P2Y6 גנטית או חסמו אותו בתרופה. עכברים חסרי הקולטן פיתחו פחות פיברוזיס לאחר חסימת השופכן או נזק בחומצה פולית: הפיברובלסטים שלהם התרבו פחות, הפקידו פחות מטריקס סיבי וגייסו פחות תאים דלקתיים. בדיקות דם הראו שאצל בעלי החיים הללו נשמר גם תפקוד סינון כלייתי טוב יותר. טיפול בעכברים רגילים עם חומר חוסם P2Y6 סיפק הגנה דומה, כולל דיכוי פעילות הסידן בפיברובלסטים והפחתת צלקתיות, אם כי השיפורים במדדי הדם היו תזזיתיים יותר.
מה המשמעות לטיפולים עתידיים
בסך הכל, העבודה חושפת שרשרת אירועים פשוטה אך חזקה. כשהתאים בצינורות הכליה נפגעים, הם משנים את הכימיה הפנימית שלהם ומשחררים UDP לרקמה שסביבם. פיברובלסטים שכנים מזהים את המולקולה הזאת דרך קולטני P2Y6, מגיבים בפרצי סידן תוך תאיים ומעבירים את עצמם למצב של יצירת צלקת — הם מתרבים, נודדים ומפקידים קולגן. קטיעת איתות הסידן המבוסס על פירימידין הזה, ובמיוחד שלב ה‑P2Y6, מרפה משמעותית את הפיברוזיס במודלים שונים של עכבר. עבור מטופלים, זה מצביע על יעד תרופתי חדשני: תרכובות החוסמות באופן סלקטיבי את P2Y6 בכליה עשויות לעזור לשבור את הקשר בין פגיעות יומיומיות בכליה לבין ההצטברות האיטית והבלתי הפיכה של צלקתיות שמובילה למחלת כליה כרונית.
ציטוט: Figurek, A., Jankovic, N., Kollar, S. et al. Pyrimidinergic calcium signaling links tubular metabolism to fibrosis in kidney disease. Nat Commun 17, 3004 (2026). https://doi.org/10.1038/s41467-026-69602-x
מילות מפתח: מחלת כליה כרונית, צלקתיות כלייתית, אותות תאי סיבי, מטבוליזם פירימידינים, קולטן P2Y6