Clear Sky Science · he
גיוס כפול של שתי מולקולות CCM2 אל KRIT1 מדכא את הביטוי של KLF4
מדוע כלי הדם במוח זקוקים לבקרה מדוקדקת
כלי הדם במוח חייבים ללכת על חבל דק: הם צריכים להיות חזקים מספיק כדי למנוע דליפות אך גמישים מספיק כדי להגיב לצרכי הגוף. כאשר האיזון הזה קורע, אנשים עלולים לפתח מומים ססיליים מוחיים — אשכולות של כלי דם פגיעים בדמות בועות שעלולים להידמם ולגרום לפרכוסים או לשבץ. המחקר הזה חושף לחיצת יד מולקולרית שלא תוארה קודם בין שלוש חלבונים שעוזרת לשמור על יציבות כלי הדם במוח, ומראה כיצד שבירת לחיצת היד הזו עלולה להניע מחלה.
שומרי השער של בריאות כלי הדם
התאים המצפים את כלי הדם מסתמכים על סט של מתגים ראשיים, הנקראים KLF2 ו-KLF4, כדי לשלוט בגנים שמחזקים את כלי הדם ומגדירים את זהותם. אם מתגים אלו מופעלים יתר על המידה, הכלים הופכים לא-תקינים ורגישים לנזק. שני חלבונים נוספים, KRIT1 ו-CCM2, ידועים כשומרים על המערכת הזו. אנשים הנושאים וריאנטים פגומים של אחד החלבונים האלה נמצאים בסיכון גבוה למומים ססיליים מוחיים. עד כה, עם זאת, המדענים לא הבינו בדיוק כיצד KRIT1 ו-CCM2 פועלים יחד כדי לשמור על KLF4 תחת שליטה.
צוות מפתיע של שלושה
החוקרים השתמשו בתאים דמויי אנדותל אנושיים שגודלו במעבדה והפחיתו באופן סלקטיבי את כמות ה-CCM2 או ה-KRIT1 בעזרת כלים גנטיים. כאשר אחד מהחלבונים הופחת, רמות KLF4 זינקו, בהד המקביל למה שנצפה במודלים בעכברים ובחולים. החזרת רמות תקינות של CCM2 או KRIT1 החזירה את KLF4 לרמות נמוכות — אך רק אם החלבונים המשוחזרים יכלו עדיין להיצמד זה לזה. על ידי מהנדסים שינויים מדויקים באזורים שבהם CCM2 ו-KRIT1 באים במגע, הקבוצה הראתה כי המגע הפיזי הזה חיוני למניעת עליית KLF4. ניסויים אלה מציבים באופן החלטי את שותפות KRIT1–CCM2 בלב מערכת הבקרה של פקטור השעתוק העוצמתי הזה.
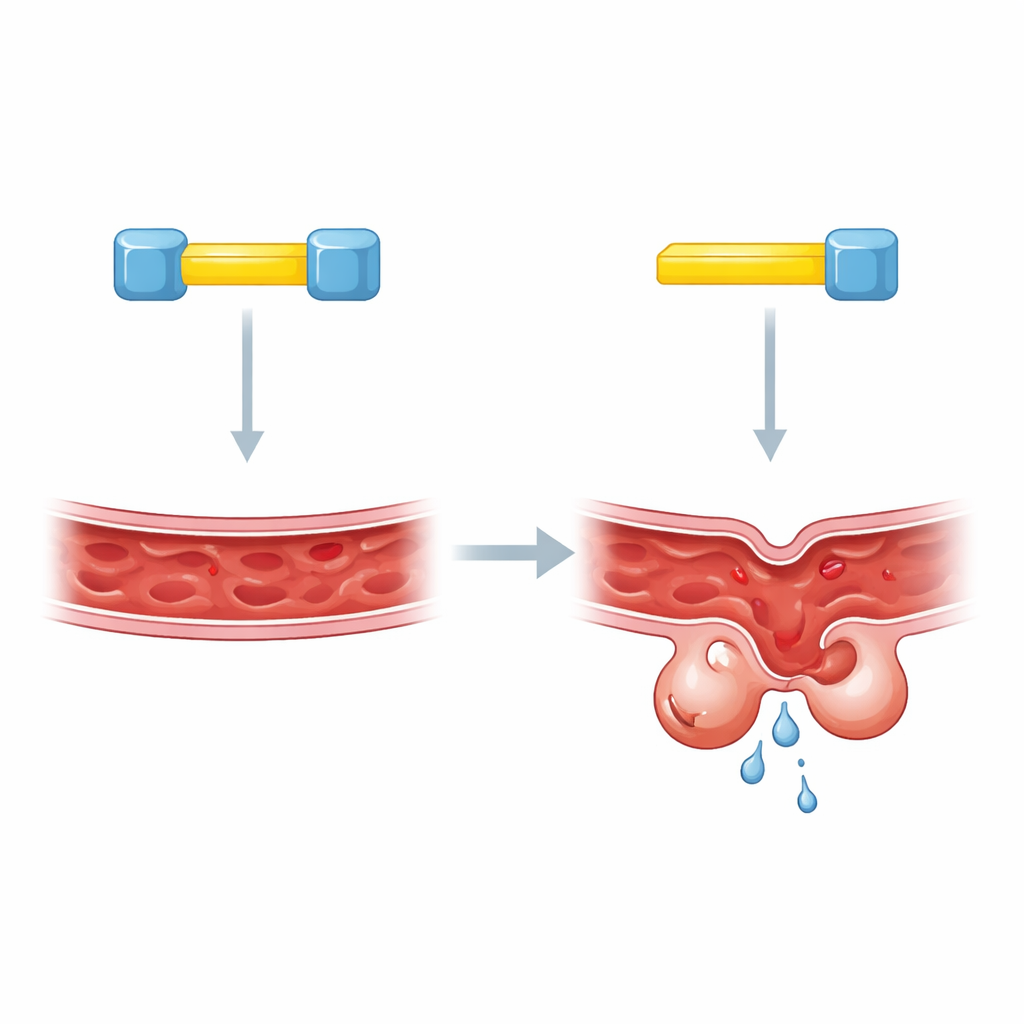
שני מנעולים עבור מפתח אחד
להעמיק את הבנתם, המחברים התמקדו בקטעים קצרים בתוך KRIT1 המשמשים אתרי עגינה מולקולריים. עבודות קודמות הציעו ש-CCM2 נקשר ל-KRIT1 באחד מהאתרים הללו, אך שיטות שונות הניבו תשובות סותרות לגבי מי האמיתי. המחקר החדש מגלה שהבלבול נבע מכך שהתמונה האמיתית מורכבת יותר: ל-KRIT1 יש שני מקטעי עגינה סמוכים, ושניהם נחוצים. כאשר אחד המקטעים הופרע, רמות KLF4 נותרו גבוהות באופן בלתי תקין, כאילו KRIT1 חסר לחלוטין. בדיקות ביוכימיות בתאים מהונדסים הראות כי מולקולת KRIT1 אחת יכולה לחבר שתי מולקולות CCM2 נפרדות בו־זמנית, לרמוז על איזשהו מארג תלת-חלקי בלתי צפוי.
מציגים את מהדק המולקולות בפירוט
הקבוצה טיהרה אז את החלקים הרלוונטיים של CCM2 ו-KRIT1 ובחנה כיצד הם מתכנסים בתמיסה ובגבישים. מדידות המסה של הקומפלקס הצביעו על כך ששתי עותקים מאזור מפתח של CCM2 נקשרים לרצועה יחידה של KRIT1 הנושאת את זוג אתרי העגינה. תמונות מבניות ברזולוציה גבוהה אישרו סידור של 2:1: פפטיד מורחב של KRIT1 משחלף בין שתי דומיינים של CCM2, כאשר כל אתר עגינה מתאים לכיס דומה על מולקולת CCM2 שונה. מקטע הלועין הקצר בין אתרי העגינה מסייע למקם את שני דומייני CCM2 אחד לצד השני, ויוצר מבנה הדוק בדמות מהדק. סוג המעורבות הכפולה הזה — שני דומייני קשירה הנצמדים לאתרים טנדם לאורך שותף אחד — לא תועד קודם עבור משפחה זו של מודולי חלבון.
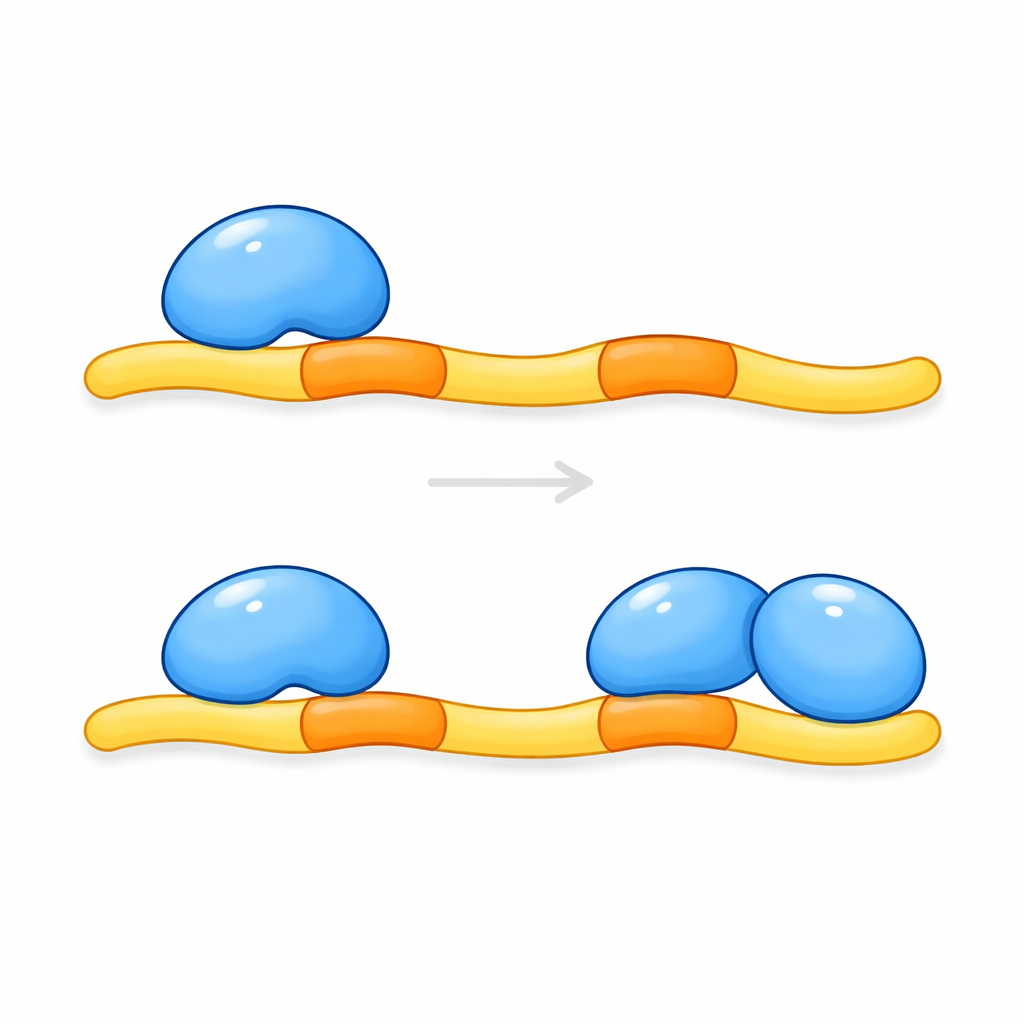
השלכות למחלות מוח ומעבר להן
ממצאים אלה מראים כי KRIT1 אינו נקשר פשוט למולקולת CCM2 אחת; במקום זאת הוא פועל כיסוד (scaffold) שמגייס זוג מולקולות CCM2. רק כאשר שני אתרי העגינה ב-KRIT1 תפוסים יכול הקומפלקס לעכב כראוי את הייצור של KLF4 ולחסום, בהרחבה, צמיחה של כלי דם פגיעים. מוטציות ב-KRIT1 שמפריעות לאחד מאתרי העגינה צפויות לפגוע במהדק המגן הזה ועלולות להסביר חלק מהצורות התורשתיות של המומים הססיליים המוחיים. מאחר שרבים מחלבוני האדם הנוספים נושאים מוטיבים תאומים דומים, המחקר גם מרמז על עיקרון רחב יותר: קשירה כפולה על ידי זוגות דומיינים קרובים עשויה להיות דרך נפוצה שבה תאים מדויקים את רשתות האיתות שלהם. הבנת האינטראקציה התלת-שותפית הזו עשויה בסופו של דבר להנחות אסטרטגיות לייצוב כלי דם באנשים בסיכון לדימומים מוחיים.
ציטוט: Huet-Calderwood, C., Fisher, O.S., Das, S. et al. Dual recruitment of two CCM2 molecules to KRIT1 suppresses KLF4 expression. Nat Commun 17, 2719 (2026). https://doi.org/10.1038/s41467-026-69595-7
מילות מפתח: מום ססילי מוחי (cerebral cavernous malformations), תאי אנדותל, KRIT1, CCM2, KLF4