Clear Sky Science · he
הכרה של מקדמים בתווך מהדק שיתופי על ידי פולימראז ה‑RNA הפוקסוויאלי ושותפו הדומה ל‑TBP/TFIIB
איך נגיף משנה את שליטת הגנים בתוך התאים שלנו
פוקסווירוסים, שאחד מהם ההיסטורי אחראי על אבעבועות רוח, מבצעים את כל ביטוי הגנים שלהם בציטופלזמה של התאים שלנו, מרחק רב ממרכז הבקרה על ה‑DNA של התא שבגרעין. כדי להצליח בכך הם מביאים איתם "מפעל גנטי" מיניאטורי משלהם. המחקר חושף, ברזולוציה אטומית, איך נגיף כזה, Vaccinia, מדליק גל ספציפי של גנים באמצע ההדבקה, באמצעות חלבון מפתיע בצורת מהדק שמשתף פעולה עם מכונת ההעתקה הויראלית.
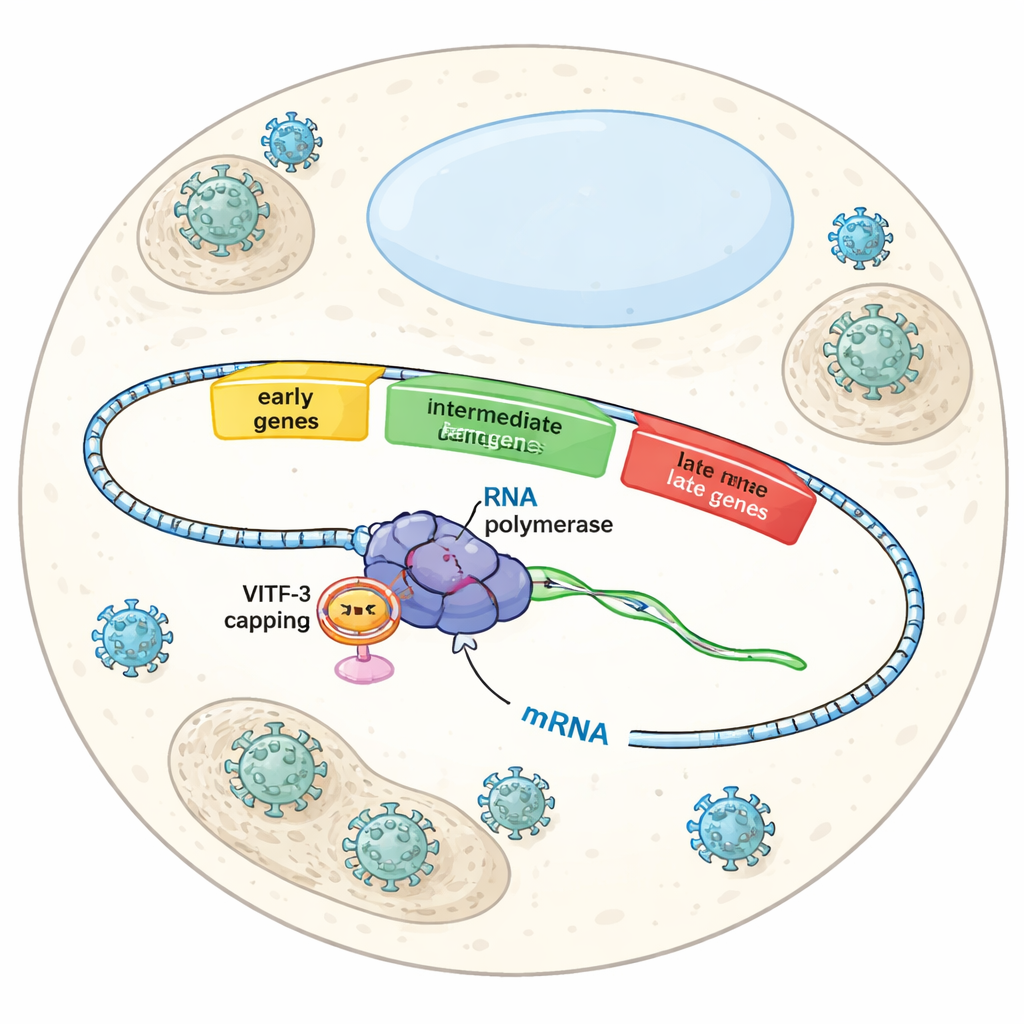
שלוש גלים בתפיסת התא על ידי הנגיף
כשה‑Vaccinia מדביק תא, הוא אינו מדליק את כל הגנים בבת אחת. במקום זאת הוא פועל לפי תסריט מתוזמן בקפידה הכולל גנים מוקדמים, בינוניים ומאוחרים. גנים מוקדמים מכינים את הקרקע לשכפול הויראלי, גנים בינוניים מסייעים בהרכבת המכונות לייצור חלקיקים חדשים, וגנים מאוחרים משלימים אריזה והרכבה. כל גל נשען על אותו פולימראז RNA ויראלי — האנזים שקורא DNA ומייצר RNA — אך גורמי עזר שונים אומרים לפולימראז איזו קבוצת גנים להפעיל בשלב הנתון. עד כה המדענים הבינו יחסית טוב את בקרת הגנים המוקדמים, אך כיצד הנגיף מזהה ומפעיל באופן סלקטיבי את הגנים הבינוניים נותרה תעלומה.
עוזר בצורת טבעת שזקוק לשותף
החוקרים התמקדו בחלבון דו‑חלקי בשם VITF‑3, הידוע כנחוץ להפעלת גנים בינוניים. אורגניזמים רבים, כולל בני אדם, משתמשים בזוג חלבונים שנקראים TBP ו‑TFIIB כדי להכווין את פולימראז ה‑RNA לנקודת ההתחלה המתאימה על ה‑DNA. הקבוצה הראתה כי VITF‑3 הוא גרסה מעודכנת מאוד של אותו זוג פרימורדי. עם זאת, בניגוד לקרובי המשפחה התאית שלו, VITF‑3 לבדו אינו נקשר ל‑DNA. במקום זאת, תתי היחידות שלו נשזרות ליצירת טבעת סגורה שהינה חסרת פעילות כלפי DNA אלא אם כן פולימראז ה‑RNA הויראלי נוכח. זה היה מפתיע, שכן ברוב המערכות הרכיב הדומה ל‑TBP נקשר קודם ל‑DNA ואז מגייס את הפולימראז; כאן, נראה כי הנגיף שינה את סדר האירועים.
צפייה במכונת התעתוק הבינונית בפעולה
כדי להבין איך ההגדרה הבלתי שגרתית הזו פועלת, המחברים בודדו את קומפלקס הקדם‑התחלה הבינוני המלא — ההרכבה המוכנה ממש לפני תחילת ייצור ה‑RNA — מתאים אנושיים מודבקים. באמצעות מיקרוסקופ אלקטרונים בקירור ברזולוציה גבוהה הם חזו את הקומפלקס ברמת כ־2.4 אנגסטרם, דיוק שמאפשר לראות שרשרות צד של חומצות אמינו ובסיסי DNA יחידים. התמונות חשפו את פולימראז ה‑RNA הויראלי אחוז ב‑DNA המקדמי, כאשר VITF‑3 יוצר טבעת הדוקה סביב רצף עשיר ב‑AT שבמעלה אתר ההתחלה. טבעת זו מכופפת במאורגן את ה‑DNA בזווית חדה של כ‑90 מעלות ומזנה אותו לתוך חריץ בפולימראז. במקביל, אנזים מצמיד של הוירוס — האחראי להוספת הכובע המגן בקצה 5′ של ה‑RNA הויראלי — מעוגן על הפולימראז, מוכן לשנות את הטרנסקריפטים חדשים ברגע שהם נוצרים.
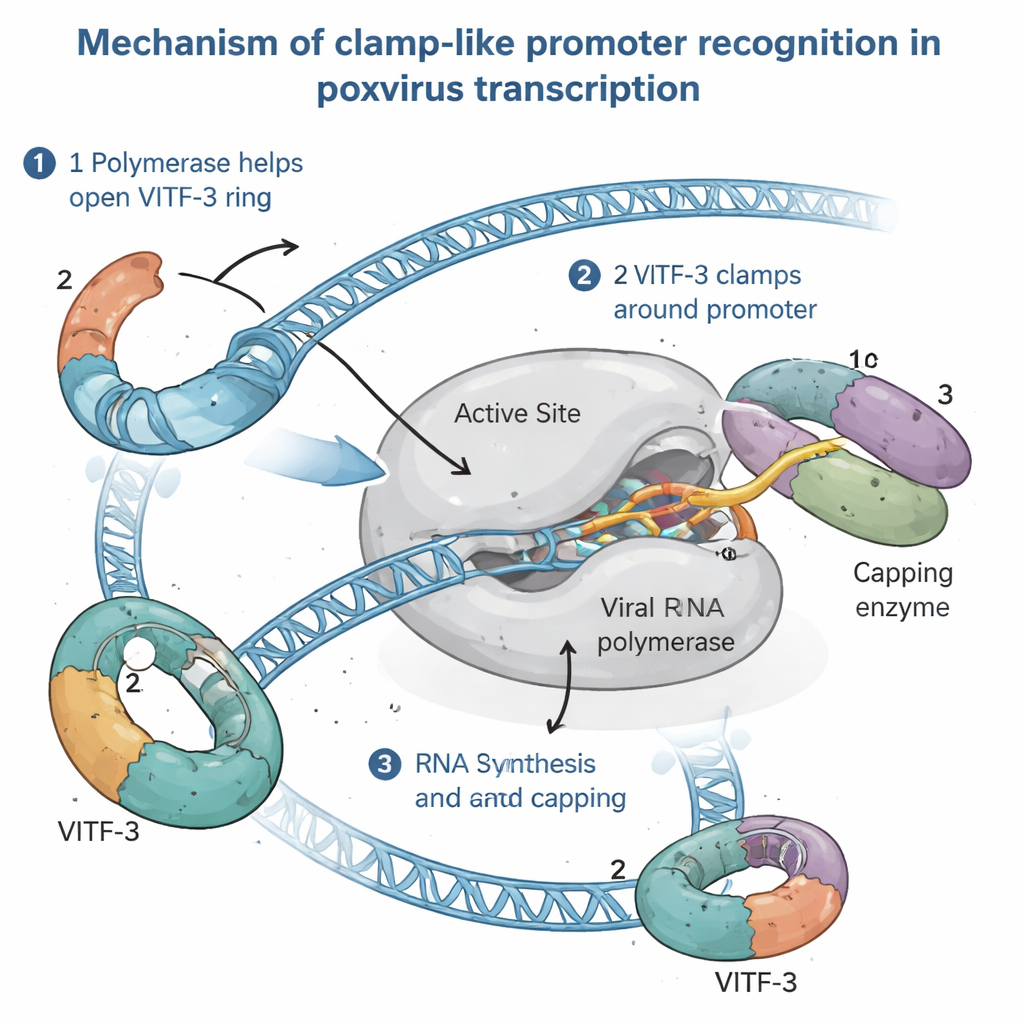
מנגנון הטענת מהדק שנשא בהשראה
על‑ידי שילוב תמונת מבנה עם מבחנים ביוכימיים, המחקר מציע שהפולימראז הויראלי טוען בפועל את VITF‑3 על ה‑DNA, פועל כמו "טוען מהדק". ראשית, הפולימראז נקשר למקדם הביניים ועוזר לפתוח את טבעת VITF‑3. אז, יחד עם אנזים ההצמדה, הוא סוגר את הטבעת סביב האזור העשיר ב‑AT, ומהדק את הקומפלקס במקום. ה‑DNA נמס בקרבת אתר ההתחלה, והפולימראז קורא ישירות אות קצר בעל ארבע אותיות (המוטיף TAAA) שמסמן בדיוק היכן יש להתחיל את סינתזת ה‑RNA. כאשר ה‑RNA גדל, הוא עוקב אחר אותו נתיב שתפס חלק מ‑VITF‑3 בקומפלקס ההתחלתי, כך שה‑RNA היוצא סביר שדוחף את VITF‑3 הצידה, ומאפשר לפולימראז להשתחרר מהמקדם ולהתקדם לאורך הגן בעוד VITF‑3 עשוי להישאר מאחור כדי להאיץ שימוש חוזר באותו מקדם.
מה משמעות הדבר להבנת פוקסווירוסים ולמטרות טיפוליות
במילים פשוטות, עבודה זו מראה כי נגיף Vaccinia הטמיע מחדש מודול אוניברסלי של בקרה גנטית לתוך מהדק שאוחז ב‑DNA רק כאשר פולימראז ה‑RNA שלו אומר לו לעשות זאת. הטריק החכם הזה מאפשר לנגיף להשתמש באנזים ליבה יחיד כדי להפעיל שלוש תוכניות תעתוק שונות, פשוט על‑ידי החלפת עוזרים ספציפיים לכל שלב. מאחר שגורמים מאותו סוג נשמרים ברחבי פוקסווירוסים רבים, כולל פתוגנים של בני אדם, מנגנון הטענת‑המהדק החדש שנחשף וטבעת הייחודית של VITF‑3 מציעים מטרות מבניות מוחשיות לאסטרטגיות אנטיויראליות שמטרתן להפריע ליכולתו של הנגיף לתזמן ולשלוט על גניו במהלך ההדבקה.
ציטוט: Jungwirth, S., Bartuli, J., Lamer, S. et al. Cooperative clamp-mediated promoter recognition by poxviral RNA polymerase and its TBP/TFIIB-like partner. Nat Commun 17, 1648 (2026). https://doi.org/10.1038/s41467-026-69571-1
מילות מפתח: תעתוק פוקסווויראלי, נגיף ה‑Vaccinia, פולימראז RNA, הכרה של מקדם, גורמי תעתוק