Clear Sky Science · he
המשמעות הפתופיזיולוגית של פגיעה באצטילציה של H3K14 התלויה ב‑KAT7 בזמן חסרון אבץ
מדוע תזונה מינורית חשובה לבריאות שלנו
אבץ הוא מתכת זעירה שהגוף שלנו צריך בכמויות מזעריות, ובכל זאת היא תומכת בשקט במאות חלבונים השומרים על תפקוד התאים. כאשר יש מחסור באבץ — בגלל תזונה, מחלה או הזדקנות — הוא נקשר לבעיות שמתחילות מפגיעה בצמיחה ומסתיימות בחיסון מוחלש ובמחלת כבד שומני. המחקר הזה שואל שאלה עמוקה יותר: איך תאים בעצם חשים שחסר אבץ, ואיך חוסר כזה מתורגם לשינויים ארוכי טווח בפעילות הגנים ובבריאות האיברים?
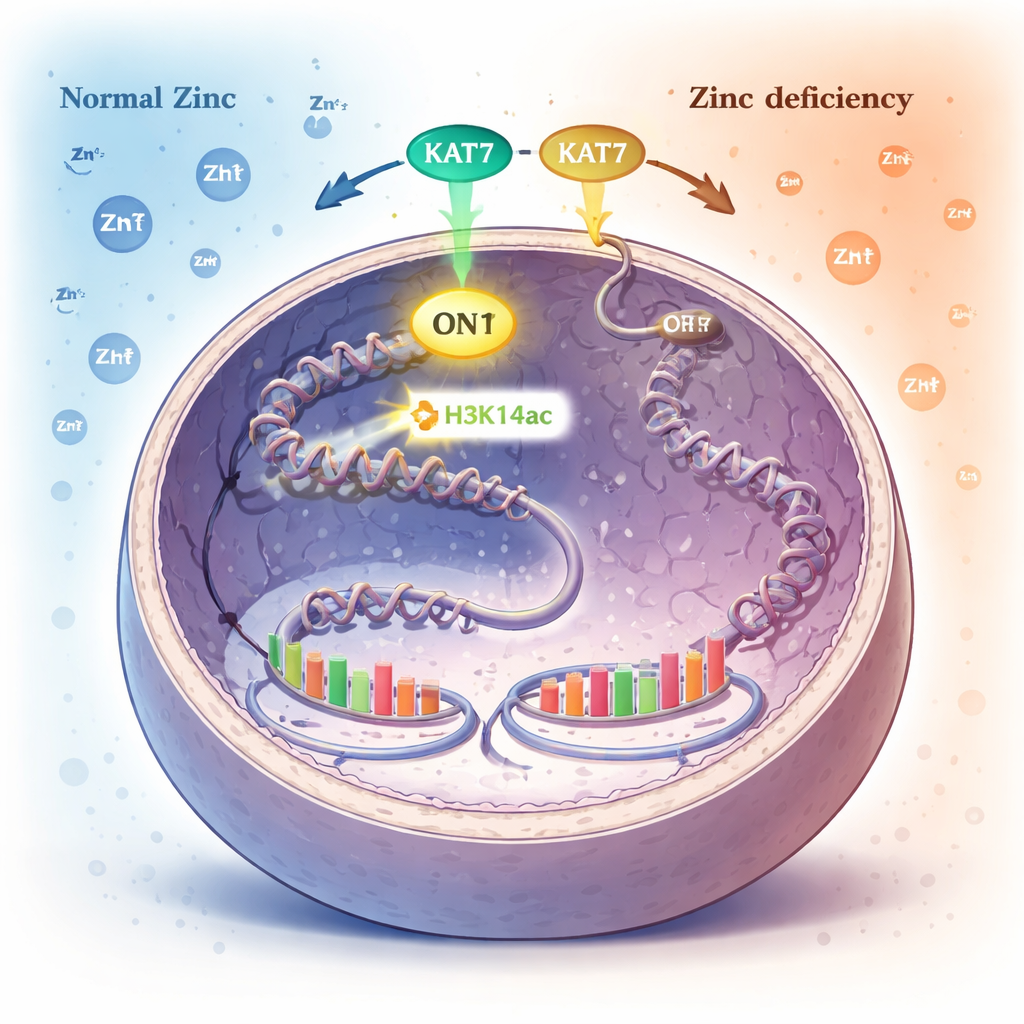
תג כימי על אריזת ה‑DNA כאזעקת אבץ פנימית
בתוך הגרעין ה‑DNA עטוף סביב גלגלי חלבון שנקראים היסטונים. התאים שותלים או מסירים תגיות כימיות קטנות מההיסטונים כדי לשלוט אילו גנים פעילים. אחת התגיות האלה, אצטילציה באתר מסוים על היסטון H3 (H3K14ac), מתווספת על ידי אנזים בשם KAT7. החוקרים גילו שכאשר אבץ נעשה כה מוגבל, רמות תג ה‑H3K14ac יורדות באופן דרמטי, בעוד תגיות היסטון רבות אחרות נשארות ללא שינוי. ממצאים אלה הצביעו על H3K14ac והאנזים KAT7 היוצר אותו כמנגנון חישה מרכזי למצב האבץ.
איך אבץ משאיר אנזים מרכזי דלוק
על ידי נטרול סיסטמטי של אנזימים שונים, החוקרים הראו ש‑KAT7 הוא המקור העיקרי ל‑H3K14ac בתאים אנושיים. ל‑KAT7 יש בתוכו מבנה קטן הקושר אבץ במרכז הפעיל שלו. כאשר התאים הוכנסו למחסור באבץ, היכולת של KAT7 להניח את תג ה‑H3K14ac פחתה, אף על פי שהחלבון עצמו נשאר בגרעין ונשאר קשור לשותפיו המסייעים. בדיקות מפורטות עם מקטעים מזוקקים של KAT7 חשפו כי קשר אבץ תקין באזור זה הכרחי לפעילותו; הפרעה בקשירת האבץ השתקה את האנזים, והוספה מבוקרת של אבץ החזירה את התפקוד. בפועל, KAT7 מתנהג כמפסק התלוי באבץ השולט על תג היסטון ספציפי.
הפיכת אובדן אבץ לשינויים בגנים שמחזירים את רמות האבץ
מה בעצם עושה אובדן תג היסטון זה? באמצעות מיפוי על‑רמת הגנום, הצוות הראה ש‑H3K14ac מרוכז במיוחד באזורי חיזוק (enhancers) — מקטעי DNA רגולטוריים שמכווינים באופן עדין גנים סמוכים. בתנאי חסרון אבץ, H3K14ac נשלף מהרבה חיזוקים, וככל שהאובדן גדול יותר כך השינוי בפעילות הגנים הסמוכים חזק יותר. גן בולט היה ZIP10, המקודד לחלבון על פני שטח התא שמייבא אבץ. כאשר H3K14ac ירד בחיזוק של ZIP10, רמות ZIP10 בממברנה עלו, ואפשרו כניסה מוגברת של אבץ לתא. חסימת KAT7 או מניעת אובדן H3K14ac הפריעו לתגובה זו והפחיתו קליטת אבץ, גם לאחר החזרת אבץ חיצוני. זה מראה שהתאים ממירים חוסר אבץ לאות אפיגנטי שמגביר את מכונת הייבוא של אבץ כדי לשחזר את האיזון.
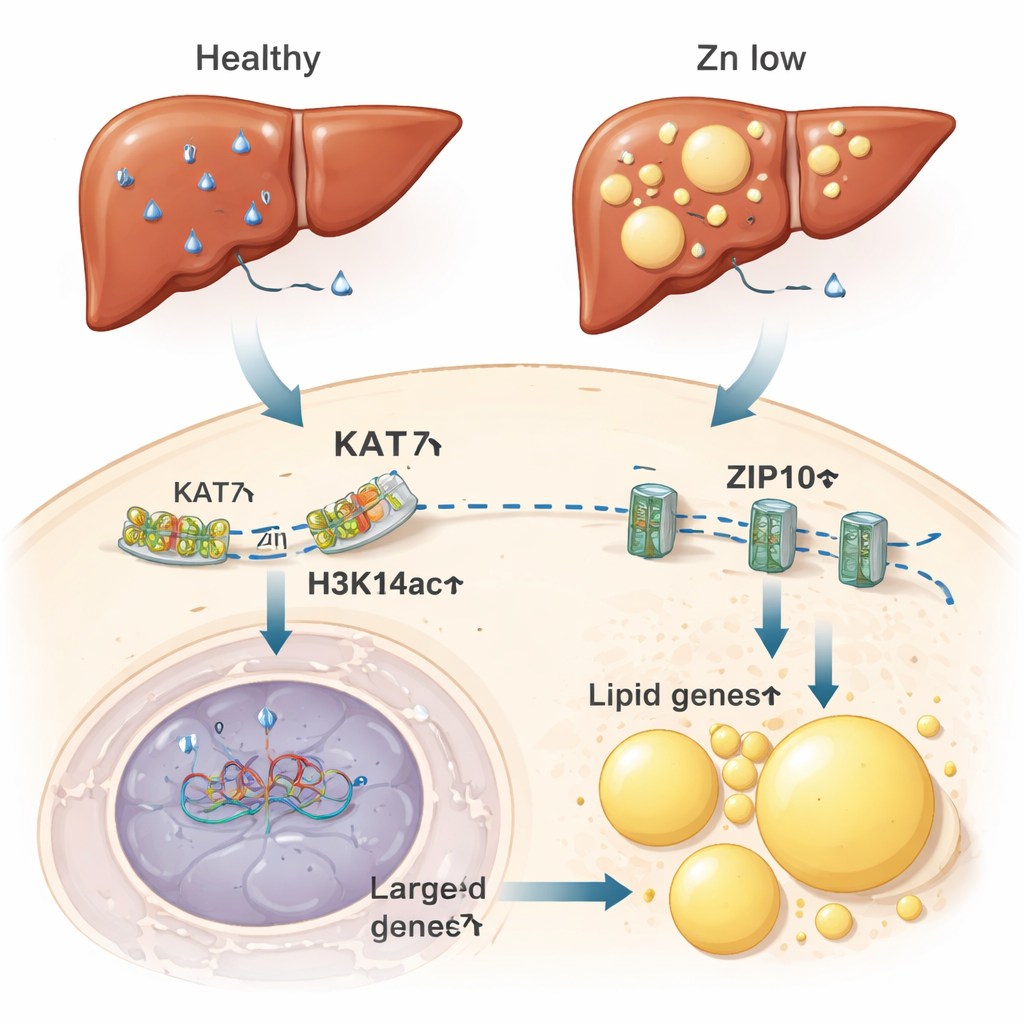
מתאים רעבי אבץ לכבדים שומניים
המחברים אז שאלו האם מפסק הרגיש לאבץ הזה משפיע על יצורים חיים שלמים. בעכברים שקיבלו תזונה דלת אבץ, הכבד — מרכז מטבוליזם חשוב של אבץ ושומן — הראה רמות אבץ נמוכות יותר, H3K14ac מופחת ופעילות KAT7 מוחלשת. שינויים אלה לוּוו בביטוי גבוה יותר של גנים שמקדמים אגירת שומן ויצירת טיפות שומן, אותם שקיות שומניות מיקרוסקופיות בתוך התאים. כבדם של העכברים החסרי אבץ הצטבר בשומן במידה המקבילה לזו של עכברים על תזונה עתירת שומן. באופן מפתיע, הורדה פשוטה של פעילות KAT7 בעזרת תרופה, גם ללא שינוי באבץ התזונתי, הספיקה לקדם הצטברות שומן בתאי כבד. לעומת זאת, אספקת אבץ נוסף הפחיתה את הצטברות השומן שנגרמה על ידי תזונה עתירת שומן.
מה משמעות זה לסיכון למחלות בבני אדם
בהקשר קליני, החוקרים סקרו מחקרים אנושיים שמדדו ריכוזי אבץ ברקמת כבד. בדוחות מרובים, אנשים עם כבד שומני והפרעות קרובות לו נמצאו עם פחות אבץ בכבדם בהשוואה לבריאים. יחד עם ניסויי העכבר, הממצאים הללו מרמזים שחסרון אבץ כרוני עשוי לקדם מחלת כבד שומני על‑ידי השתקת KAT7, מחיקת תג ה‑H3K14ac והגברה מתמשכת של גנים המעודדים אחסון שומן. במילים פשוטות, העבודה חושפת מעגל פנימי של "אבץ‑לאפיגנטיקה": כאשר האבץ יורד, אנזים התלוי באבץ מאבד כוח ומשנה את אריזת ה‑DNA באופן שמתחיל בסיוע למשוך יותר אבץ לתא, אך עם הזמן עלול לדחוף את הכבד להצטברות שומן מזיקה.
ציטוט: Fujisawa, T., Takenaka, S., Maekawa, L. et al. Pathophysiological significance of impaired KAT7-dependent histone H3K14 acetylation during zinc deficiency. Nat Commun 17, 1710 (2026). https://doi.org/10.1038/s41467-026-69476-z
מילות מפתח: חסרון אבץ, אפיגנטיקה, שומן כבד, אצטילציה של היסטונים, משאבות אבץ