Clear Sky Science · he
מפת ייחוס כללית המוגדרת על ידי שיאי קונסנזוס לניתוח נתוני ATAC-seq בתא יחיד
מדוע חשובה מיפוי הדלתות הפתוחות של ה‑DNA שלנו
כל תא בגופך נושא למעשה את אותו ה‑DNA, אך תאי מוח, דם וגידול מתנהגים בצורה שונה מאוד. סיבה מרכזית היא שרק מקטעים מסוימים של ה‑DNA חשופים ו"פתוחים" לשימוש בכל רגע נתון. טכנולוגיות חדשות בתא יחיד מאפשרות למדוד את החשיפה הזו על פני הגנום כולו, אך עד כה חסר להן מפה ייחוס משותפת — מעין אטלס סטנדרטי להשוואת תוצאות בין ניסויים ומעבדות. מחקר זה בונה מפה כזו, הנקראת cPeaks, ומראה כיצד היא מצליחה לחדד את הראייה שלנו לגבי סוגי תאים, התפתחות וסרטן.
להפוך ניסויים רבים למפה משותפת אחת
המחברים התחילו באיסוף 624 ניסויים איכותיים שמדדו כרומטין פתוח — החלקים הנגישים של ה‑DNA — ביותר מ‑40 איברים אנושיים. בכל ניסוי, תוכנות כבר סימנו "שיאים" שבהם ה‑DNA היה חשוף במיוחד. במקום לטפל בכל מערך נתונים בנפרד, הצוות חיפש בזהירות את חפיפת רשימות השיאים האלו לאורך הגנום ומזג אזורים חופפים. לאחר מכן בדקו כמה פעמים כל מיקום קטן בתוך אזורים ממוזגים אלו הוגדר כפתוח בניסויים שונים, והפכו כל אזור לצורת חתימה אופיינית המשקפת עד כמה הוא הופיע בעקביות. כאשר אזור ממוזג הכיל בפועל מספר אתרי פתיחה קרובים זה לזה, פיצלו אותו ליחידות פשוטות רבות יותר. יחידות אלו — כ‑1.4 מיליון בסך הכל — הפכו לשיאי הקונסנזוס הנצפים, או cPeaks, קטלוג מועמד ליוחס כרומטין אנושי.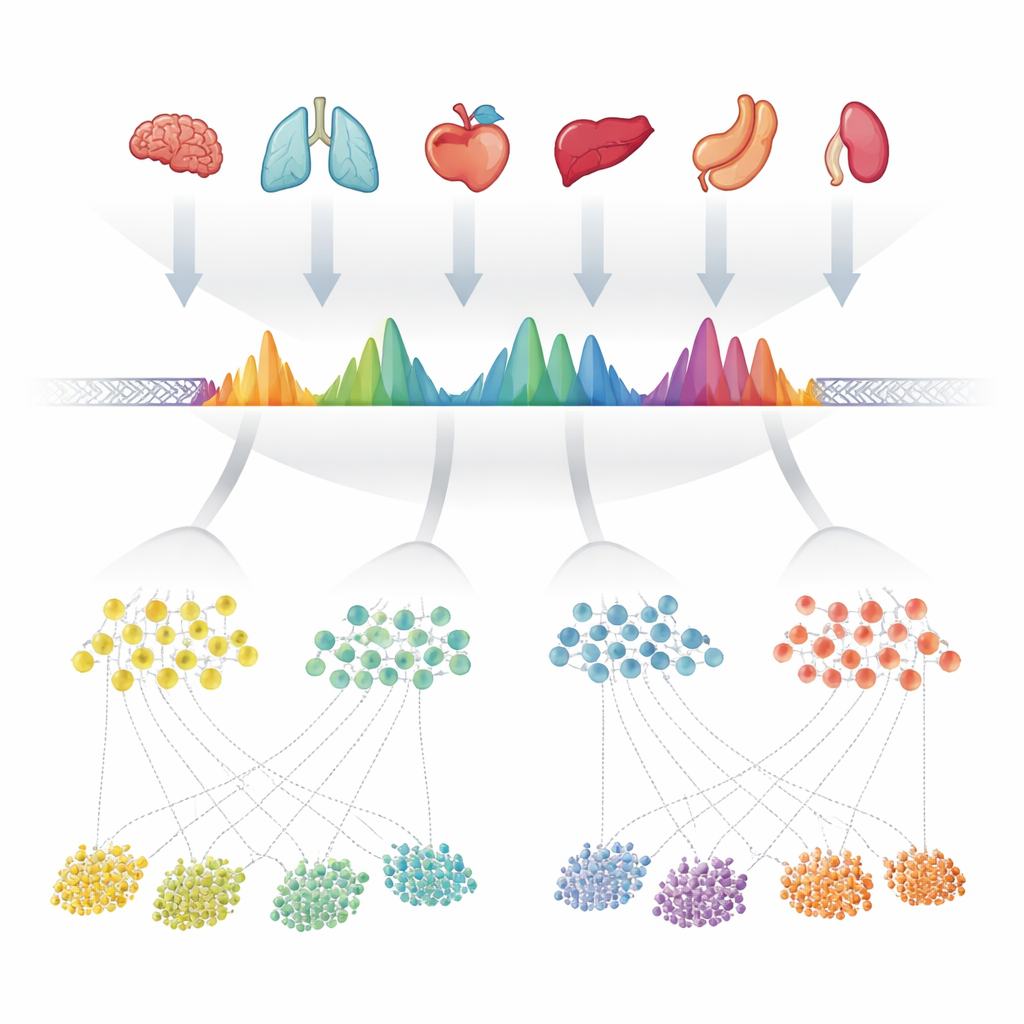
טביעת אצבע יציבה בין רקמות וטכנולוגיות
כדי לשמש ייחוס שימושי, cPeaks חייבים לייצג תכונות אמיתיות וחוזרות של הגנום, ולא מוזרויות של דגימות או תוכנה ספציפית. המחברים בדקו זאת על‑ידי שיחזור האזורים הממוזגים שלהם באמצעות דגימות דם בלבד, רקמות מוצקות בלבד, מאגרים ציבוריים נפרדים ואפילו שיטות מעבדה שונות לחקר DNA פתוח. בכל מקרה, אותם מיקומים גנומיים הצליחו לייצר צורות שיא דומות להפליא, וברוב מערכי התא הבודד שנבדקו חפף יותר מ‑90% מהשיאים המקומיים עם קטלוג ה‑cPeaks. קריאות ממגוון איברים הצטברו במדויק סביב מרכזי ה‑cPeaks, מה שמראה שאזורים אלו תופסים באופן אמין היכן הכרומטין פתוח. בהשוואה לערכות ייחוס קודמות המבוססות על טכנולוגיות קרובות, cPeaks כיסו יותר מה‑DNA הנגיש שנתפס בניסויי ATAC‑seq, ותפסו כמעט אותו כמות אות כמו שיאים שהוגדרו מחדש בכל מערך נתונים — וזאת למרות שהן קבועות ושימושיות חוזרת.
לאמן רשת עצבית למצוא אזורים חסרים
גם מאות דגימות קיימות אינן יכולות לכסות כל סוג תא אפשרי. כדי להרחיב את המפה לאזורים שלא נצפו עדיין, הצוות פנה ללמידה עמוקה. הם אימנו רשת קונבולוציה חד־ממדית על רצפי DNA: דוגמאות שנמצאו בתוך cPeaks משמשות כחיוביות, בעוד שאזורים רקע נבחרים אקראית שימשו כשליליות. המודל למד להבחין בין השניים בדיוק גבוה, מה שמעיד ש‑cPeaks נושאים דפוסי רצף הניתנים לזיהוי. כאשר החוקרים הסתירו במכוון שיאים שמיוחדים לרקמה אחת בכל פעם, הרשת עדיין שחזרה אותם רק מן הרצף, כולל אתרים נדירים ספציפיים לרקמות. לאחר מכן הם החליקו חלון קטן על שאר הגנום, נתנו ניקוד לכל מקטע והוסיפו כ‑280,000 אזורים מצטיינים חדשים לקטלוג כ‑cPeaks חזויים, תוך שיפור כיסוי במיוחד ברקמות שהיו מיוצגות פחות בנתונים המקוריים.
קישור אזורים פתוחים לגנים, סוגי תאים ותאים נדירים
עם ייחוס עשיר יותר ביד, המחברים בדקו מה תפקודם של האזורים הללו. רבים מ‑cPeaks נמצאים ליד אתרי התחלה וסיום של גנים או חופפים אלמנטים ווסתים ידועים כגון פרומוטורים, אננסרים ואתרי קשירה לחלבונים ארכיטקטוניים כמו CTCF. חלק קטן נגיש כמעט בכל מערך נתונים; שיאי "תחזוקה" ארוכים אלה נוטים לשבת באזורים של פרומוטורים מרכזיים של גנים הנחוצים לתחזוקה בסיסית של התא. הצוות גם סיווג את ה‑cPeaks לפי כמה חדים ועקביים הקצוות שלהם בין דגימות, תכונה שמשקפת עד כמה ה‑DNA הסמוך נארז בדיוק לנוקלאוזומים. אזורים עם גבולות מוגדרים בחדות מועשרים למשפחות ספציפיות של גורמי שעתוק הידועים בעיצוב כרומטין ובהנעת ההתפתחות. כשמשתמשים ב‑cPeaks כקבוצת תכונות לניתוח מספר מערכי ATAC‑seq בתא יחיד, הם שיפרו את דיוק תיוג סוגי התאים והיו מועילים במיוחד בזיהוי סוגי תאים נדירים ותת‑סוגים עדינים ששערי שיא קודמים או רשתות גנומיות פשוטות היטשטשו אותן לרוב.
לעקוב אחר התפתחות וסרטן בשפה משותפת
כוחו של ייחוס סטנדרטי מתגלה כשמשווים הקשרים ביולוגיים מאוד שונים. באמצעות cPeaks, המחברים ניתחו מחדש נתוני תא יחיד מהרשת המתפתחת, אטלסים גדולים של רקמות עובריות ובוגרות וכמה סרטן. הם יכלו לשחזר מסלולי התפתחות ולראות ששיעור ה‑cPeaks החדים וה"ממוקמים היטב" נוטה לעלות בשלבים המעבריים, ואז לרדת כאשר תאים מתייצבים לזהות יציבה. דפוס דומה הופיע גם בשלבי הגידול: סרטן במצב ביניים הראה שיעור גבוה יותר של אזורים מסודרים אלו, רמז לעיצוב רגולטורי אינטנסיבי. בגידול שחלה אחד, ה‑cPeaks עזרו לחשוף שני תת‑שבטי תאים סרטניים נפרדים עם שינויים שונים במספר העתקים של ה‑DNA, מה שממחיש כיצד הייחוס יכול לגלות מורכבות נסתרת במחלה.
מה המשמעות למחקר הגנום בעתיד
לא מומחים, ניתן לחשוב על cPeaks כסט קואורדינטות מאוחד המסמן היכן סביר שהגנום פתוח ופועל פיזית בין סוגי תאים אנושיים רבים. על ידי יישור ניסויים חדשים של כרומטין בתא יחיד למפה המשותפת הזו, חוקרים יכולים להשוות תוצאות בין מחקרים, לזהות ביתר קלות מצבי תאים נדירים או מעבריים, ולהתחיל לבנות מודלים בקנה מידה גדול של ויסות גנים — בדומה לאופן שבו קטלוגים גנים סטנדרטיים אפשרו את עליית אטלסי RNA בתא יחיד. קטלוג ה‑cPeaks הנוכחי הוא טיוטה ראשונה שיגדל ככל שיתקבלו נתונים חדשים, אך הוא כבר מספק שפה משותפת לתיאור זמינות כרומטין, ומקרב אותנו לתמונה מאוחדת של האופן שבו אריזת ה‑DNA מנחה התפתחות, בריאות ומחלה. 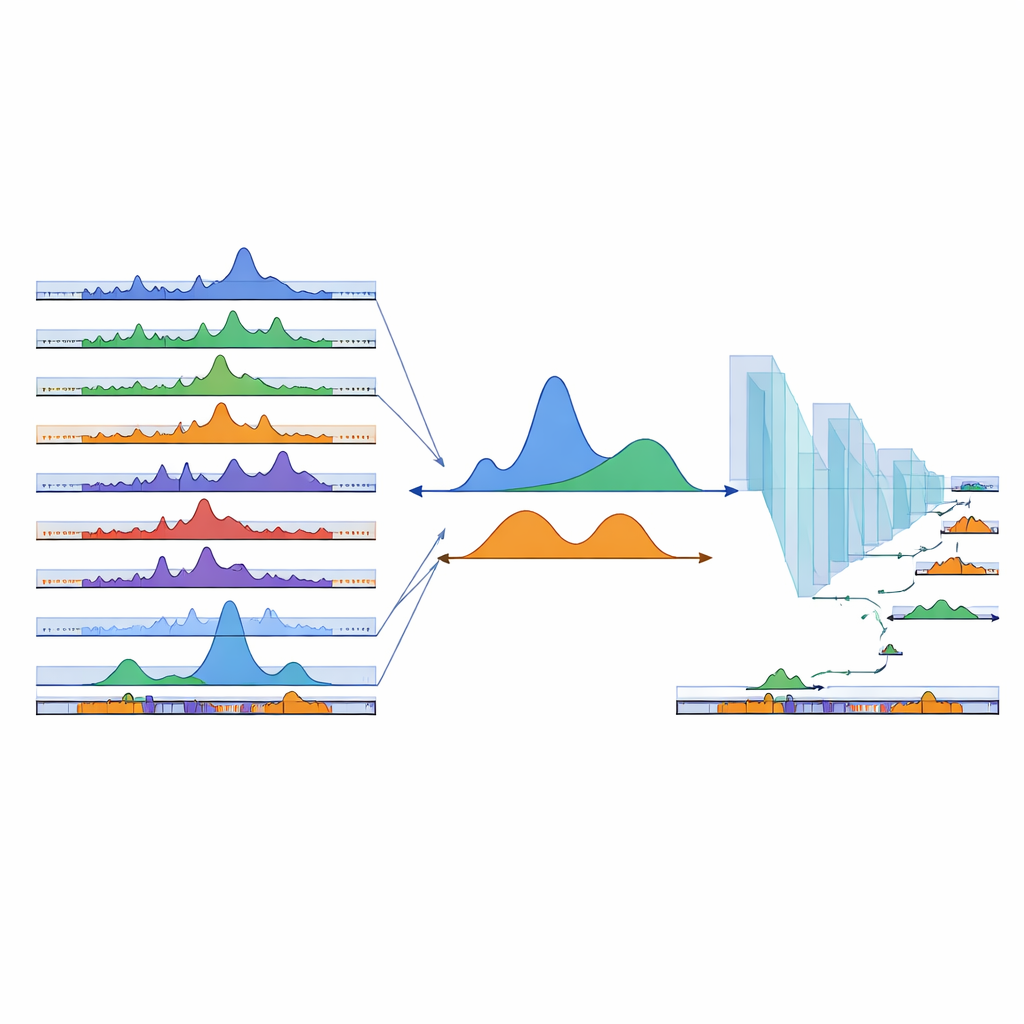
ציטוט: Meng, Q., Wu, X., Chen, W. et al. A generic reference defined by consensus peaks for single-cell ATAC-seq data analysis. Nat Commun 17, 2522 (2026). https://doi.org/10.1038/s41467-026-69461-6
מילות מפתח: זמינות כרומטין, ATAC-seq בתא יחיד, שיאי קונסנזוס, ויסות גנים, למידה עמוקה בגנומיקה