Clear Sky Science · he
מיקוד משולש של STING, TGF-β ו‑PD-L1 מחזק איתות CXCL16–CXCR6 לתגובה אנטי‑גידולית עוצמתית
הפיכת גידולים קרים לחמים
אימונותרפיה נגד סרטן שינתה את הטיפול בחולים מסוימים, אך עדיין ישנם גידולים רבים שמתעלמים מתרופות אלו החזקות. המחקר חוקר מדוע סוגי סרטן מסוימים עמידים לתרופות החסימה המודרניות ומציע גישה חכמה בת שלושה כיוונים שמפעילה את מנגנוני ההגנה של הגוף, מושכת תאי T מתנקשים איכותיים ושומרת על פעילותם בתוך הגידול.
מדוע התרופות החיסוניות הנוכחיות אינן מספיקות
מרבית האימונותרפיות המאושרות מתקינות בלם בודד בתאי החיסון, כגון מסלול PD‑1/PD‑L1. קבוצה חדשה של תרופות מנסה להרחיב את ההשפעה על ידי חסימת TGF‑β, מולקולה שמדכאת בעוצמה את המערכת החיסונית בגידולים מתקדמים. תרופה אחת כזו, YM101, משלבת חסימת TGF‑β ו‑PD‑L1 בנוגדן יחיד והראתה הבטחה בעכברים. עם זאת, גם בבעלי חיים זהים גנטית חלק מהגידולים כמעט שלא הצטמצמו. בהשוואה בין גידולים רגישים לעמידים מצאו החוקרים שטיפול מוצלח התקשר להפעלה חזקה של מערכת החיסון המולדת, ובמיוחד איתות דרך נתיב בשם STING, החושף DNA חריג ומעורר אותות דמויי‑אנטי‑וירוס.
הוספת מנוף שלישי: נתיב STING
בהנחה שהפעלת המערכת המולדת החלשה היא החלק החסר, הצוות שילב את YM101 עם אגוניסט STING בצורת גלולה בשם MSA‑2 במספר דגמי גידול בעכברים, כולל גידולים בדרך כלל «קרים» וקשים לטיפול. הגישה המשולשת — הפעלת STING לצד חסימת TGF‑β ו‑PD‑L1 — הקטינה את הגידולים ביתר יעילות, הרחיבה את ההישרדות ולעתים הגנה על עכברים מפני חזרת הגידול לאחר אתגר מחודש, מה שמעיד על זיכרון חיסוני ארוך טווח. זה עלה על השילוב הרגיל של אגוניסט STING עם חסימת PD‑L1 בלבד, ואף שיפר טיפול באגוניסט STING גם כשחסמו רק את TGF‑β, מה שמראה כי TGF‑β עצמו פועל כבלם מרכזי על החיסון המונע על‑ידי STING. 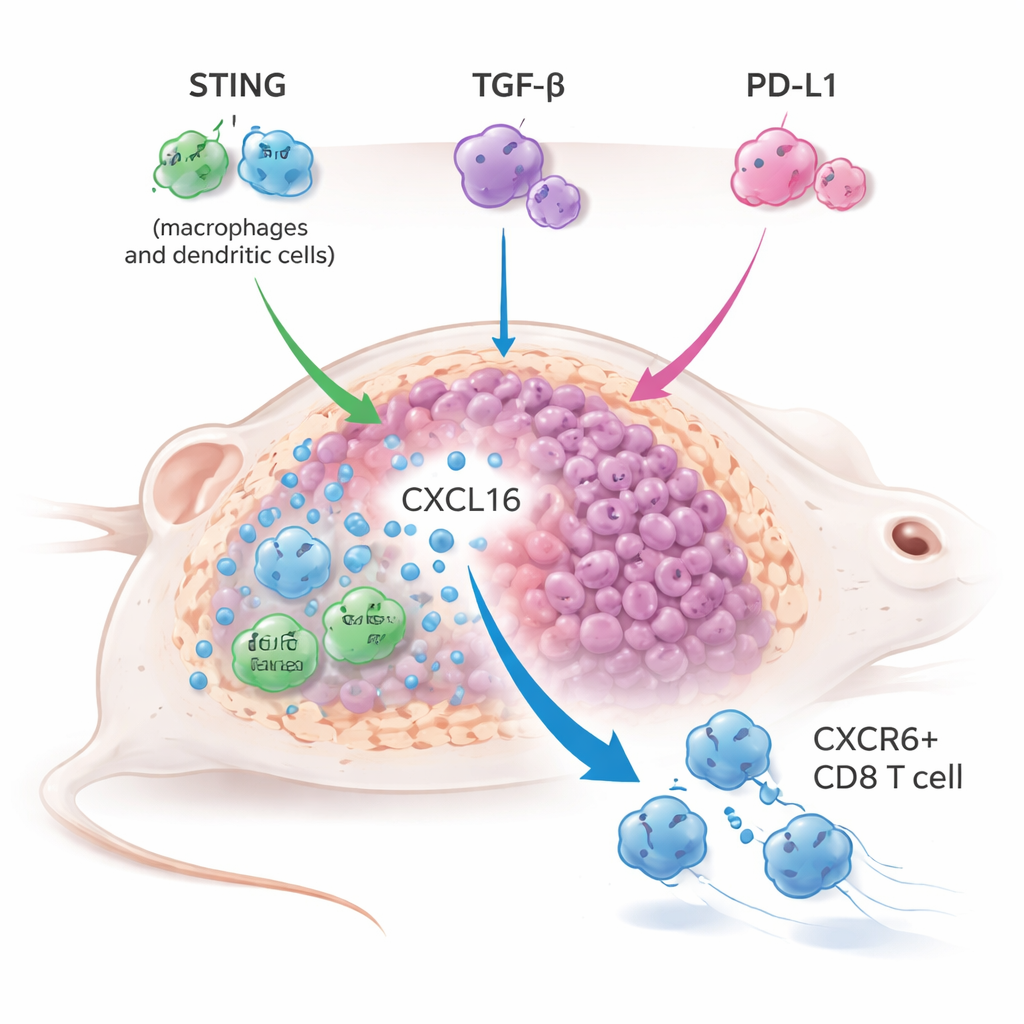
גיוס צוות מתנקשים מתמחה
כדי להבין כיצד האסטרטגיה המשולשת פועלת השתמשו החוקרים בריצוף RNA בתא יחיד ופרופילינג חיסוני מפורט של הגידולים שטופלו. הם גילו הרחבה מרשימה של תת‑קבוצה ספציפית של תאי T קטלניים המסומנת על‑ידי הקולטן CXCR6. תאי CXCR6+ CD8 אלו היו חמושים היטב, הביטאמו רמות גבוהות של גרנזימים, פרפורין ומולקולות דלקתיות, והראו סימנים חזקים של הפעלה והתרבות. במקביל, המאקרופאגים ותאי דנדריט הקשורים לגידול הגבירו את ייצור הכימוקין CXCL16, הקושר את CXCR6 ועוזר לשמר תאים אלה בתוך הגידול. כאשר הקישור CXCL16–CXCR6 נותק — או על‑ידי חסימת CXCL16 או באמצעות השמטה גנטית של CXCR6 בתאי T — הטיפול המשולב איבד ברובו את עוצמתו האנטי‑גידולית, מה שמוכיח שהציר הזה מרכזי להצלחת הטיפול.
כיצד מפעיל שרשרת האיתות
בהעמקה נוסף, הצוות חקר כיצד הפעלת STING וחסימת TGF‑β יחד מגבירות את CXCL16. בתאי חיסון אנושיים ובעכבריים אגוניסטי STING הגבירו בחוזקה את CXCL16 ואת הציטוקין האנטי‑וירלי IFN‑β, בעוד ש‑TGF‑β מוסף הפחית שניהם בחדות. החוקרים הראו ש‑STING מעורר איתות IFN‑I, שמפעיל את גורם השעתוק STAT1; STAT1 נקשר ישירות לאזור הבקרה של גן CXCL16 ומדליק את ביטויו. TGF‑β מפריע לשרשרת זו על‑ידי התערבות בצעד מרכזי באיתות STING, קרוב לוודאי דרך חלבון שנקרא HDAC4 ורדיקלים חופשיים של חמצן, מה שמחליש את הפעלת IRF3 ואת ייצור IFN‑β ו‑CXCL16 במורד. חסימת TGF‑β מסירה את הבלם הזה, ומאפשרת לאגוניסטי STING להצית במלואם את ציר STAT1–CXCL16 בתאי מיואיד ולספק לתאי CXCR6+ את האיתותים הנחוצים להישאר ולהילחם בגידול.
בניית תרופה מדויקת יחידה
כדי להפוך את המשטר המורכב הזה לעממי וממוקד גידול יצרו החוקרים נוגדן‑קוניגט (antibody conjugate) מעורר חיסון יחיד בשם Y101S. המולקולה הזו משלבת את הנוגדן הכפול החוסם TGF‑β/PD‑L1 עם אגוניסט STING קשור בקשר מפרק. Y101S ממוקדת לתאי מיואיד החיוביים ל‑PD‑L1 בגידול, נבלעת לתוך תאים אלה ומשחררת שם את תרופת ה‑STING. בכמה סוגי סרטן בעכברים Y101S השיגה תוצאה שוות ערך או טובה יותר מהיעילות של מתן YM101 יחד עם מנה חופשית גבוהה של אגוניסט STING, אף כי נשאה רק חלק זעיר מאותה מנה של STING. היא הגבירה מאקרופאגים ותאי דנדריט בעלי CXCL16, הרחיבה תאי CXCR6+ CD8, יצרה זיכרון חיסוני עמיד וריכזה אותות דלקתיים בתוך הגידולים תוך שמירה על איברים בריאים, עם פרופיל בטיחות נוח בעכברים. 
מובן הדבר לעתיד טיפול בסרטן
בעבור הקוראים הלא‑מומחים, המסר המרכזי הוא שתקיפה של סרטן בעזרת מתג חיסוני אחד או שניים בלבד עשויה שלא להספיק — במיוחד כאשר הגידולים מכבים באופן אקטיבי מערכות אזעקה מוקדמות. העבודה מראה ששילוב הפעלת STING עם חסימת TGF‑β ו‑PD‑L1 יכול לשכתב את מיקרו‑הסביבה של הגידול, למשוך ולשמר באופן עוצמתי קבוצה מתמחה של תאי T קטלניים, ולהשיג תגובות עמוקות ועמידות יותר במודלים פרה‑קליניים. הנוגדן‑תרופה המשולב Y101S מממש אסטרטגיה זו בתרופה ממוקדת אחת ומציע מפת דרכים לאימונותרפיות מדור הבא שמטרתן גידולים שעומדים כיום בעוצמת תרופות החסימה הסטנדרטיות.
ציטוט: Yi, M., Li, T., Gu, Y. et al. Triple targeting of STING, TGF-β, and PD-L1 boosts CXCL16–CXCR6 signaling for potent antitumor response. Nat Commun 17, 1441 (2026). https://doi.org/10.1038/s41467-026-69456-3
מילות מפתח: אימונותרפיה של סרטן, נתיב STING, חסימת TGF‑בטא, נוגדן כנגד PD‑L1, תאי CXCL16 CXCR6