Clear Sky Science · he
תת‑אוכלוסייה של תאים מזנכימליים המושרית על‑ידי מאקרופאגים ומבטאת Fcer1g תורמת לפיברוזיס הנגרם על‑ידי פציעה
מדוע חלק מהפצעים משאירים צלקות מתמשכות
רובנו נושאים צלקות מחתכים, ניתוחים או תאונות, אך מדוע חלק מהפצעים מרפאים בצורה חלקה בעוד אחרים משאירים סימנים עבים ומרוממים נותר נחבאי. המאמר בוחן שאלה זו על‑ידי התמקדות בתאים המשקמים את העור הפגוע. החוקרים חושפים קבוצה שלא זוהתה קודם של תאים היוצרים צלקת שמופעלת מוקדם אחרי הפציעה, בהשפעת תאי חיסון הקרויים מאקרופאגים. הבנה של השותפות הנסתרת הזו עשויה להצביע על דרכים לטיפולים שיאפשרו לעור להחלים עם פחות צלקות ובאותו זמן לסגור את הפצעים ביעילות.
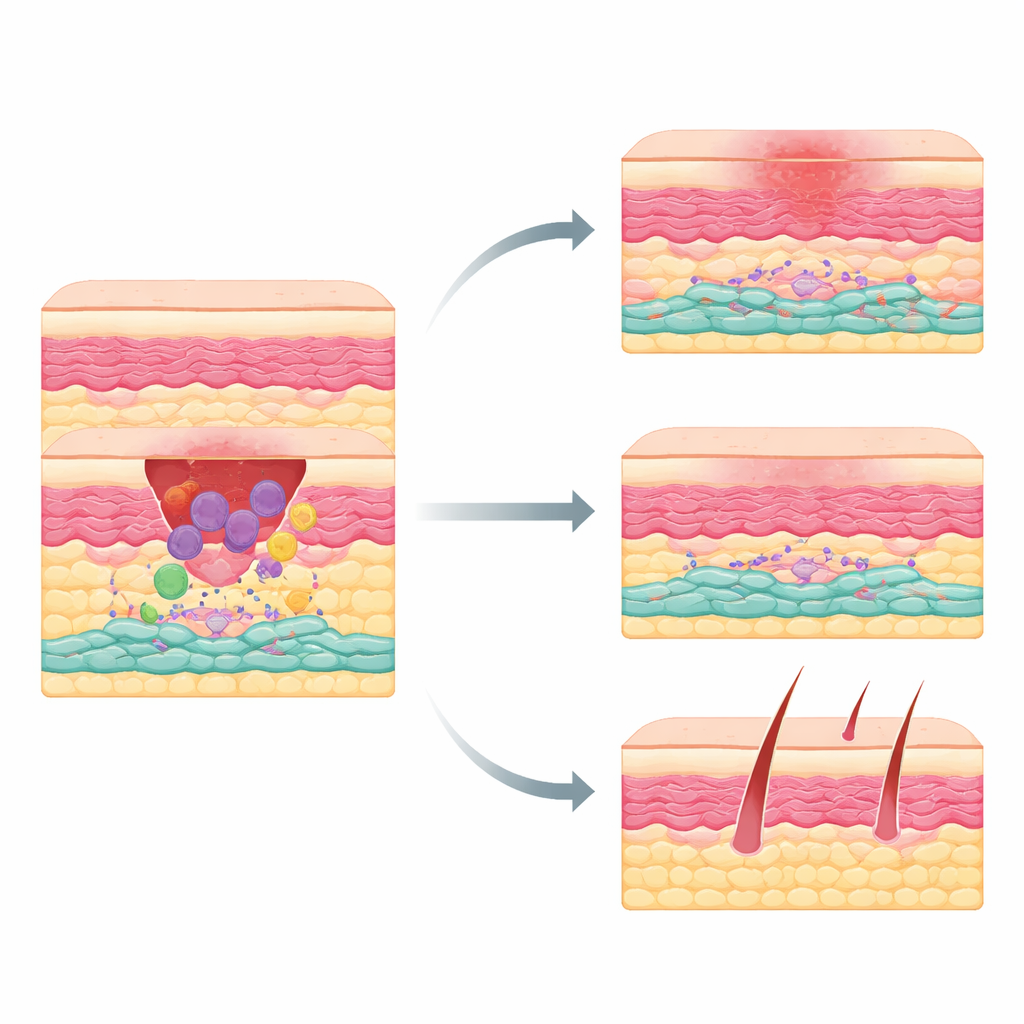
השחקנים הנסתרים בתוך העור המתחשל
כשחוטבים את העור, הגוף עובר רצף מתואם: תחילה דלקת לניקוי הנזק, אז גדילת רקמה, ולבסוף עיצוב מחודש. מאקרופאגים מגיעים מוקדם לנקות שברי רקמה ולשדר אותות כימיים שממונים תאים אחרים. בין המגיבים נמצאים תאים מזנכימליים—בוני סיבים דמויי פיברובלסטים שמניחים קולגן וחומרי תמיכה אחרים. בונים אלה אינם זהים: חלקם תומכים ברגנרציה, בעוד אחרים נוטים לייצר עודף רקמת צלקת. עד כה המדענים לא זיהו בבירור אילו תאים מזנכימליים בעור המבוגר הם האשמים העיקריים בצלקות עבות.
תאי חיסון שמכינים בשקט את הבמה לצלקת
כדי לבדוק כיצד מאקרופאגים משפיעים על היווצרות צלקת, הצוות השתמש בעכברים שבהם ניתן להסיר בררנית מאקרופאגים במהלך הימים הראשונים שלאחר הפציעה. כאשר מאקרופאגים מוקדמים אלה נותרו חסרים, הפצעים עדיין נסגרו אך יצרו צלקות קטנות יותר בהרבה, עם קולגן פחות צפוף. רצף RNA בתא יחיד—שיטה לפרופיל פעילות גנים תא תא—הראה שרוב תת‑הקבוצות המזנכימליות לא השתנו מהיעדרות המאקרופאגים. יוצא מן הכלל הצביע על עצמו: תת‑קבוצה מובחנת של תאים מזנכימליים החיוביים ל‑PDGFRα שהפעילה את הגן הקרוי Fcer1g. תת‑קבוצה זו כמעט ונעלמה כאשר המאקרופאגים הוסרו, מה שמרמז שמאקרופאגים דרושים ליצירה או לשמירה על תאים אלה.
אוכלוסייה מהירה שמניעה צלקת
ניסויים נוספים מיפו היכן ומתי מופיעים תאים מזנכימליים חיוביים ל‑Fcer1g. בעור שאינו פצוע הם היו נדירים, אך לאחר הפציעה הם התרבו במהירות, תחילה סביב קצוות הפצע ואז רוכזו במיטת הפצע, שם הם הרכיבו את רוב התאים החיוביים ל‑PDGFRα עד היום השביעי. תאים אלה התחלקו מהר יותר מאשר תאים מזנכימליים אחרים והציגו נדידה נמוכה, דבר שמצביע על כך שהתרבות מקומית מזינה את עלייתם. כאשר החוקרים השתמשו במערכת גנטית חכמה כדי לחסל באופן בררני תאים שמבטאים גם PDGFRα וגם Fcer1g, סגירת הפצע התנהלה כרגיל—אבל הצלקות הצטמצמו ביותר מ‑20 אחוז, תכולת הקולגן ירדה בכ‑כ‑30 אחוז, ורשת הקולגן בעור המתוקן נראתה יותר כמו עור שלא נפגע. זקיקי שיער היו שכיחים יותר בפצעים שבהם הוקדמו תאים אלה, רמז לריפוי בעל נטייה רגנטיבית יותר.
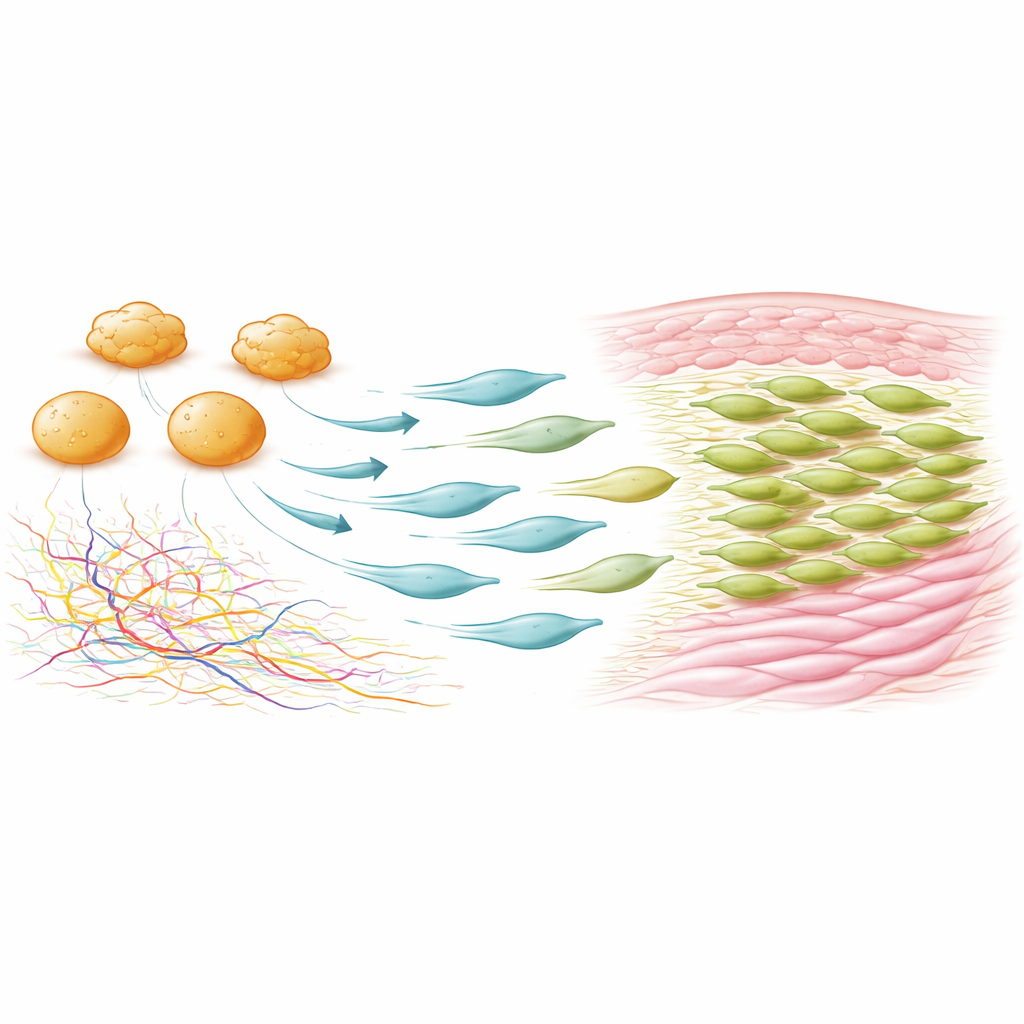
כיצד מאקרופאגים מסמנים לבונים להצטלק יתר על המידה
כדי להבין כיצד מאקרופאגים מדליקים את המצב המייצר צלקת, הצוות ניתח נתיבי תקשורת סבירים בין סוגי התאים. מועמד מרכזי היה פיברונקטין, חלבון דביק החלק מרשת החומר הזמנית בפצעים טריים. מאקרופאגים בפצעים מוקדמים היו מקור עיקרי לפיברונקטין, ורמותיו ירדו בחדות כשהמאקרופאגים הוסרו. בעכברים מהונדסים שחסרו צורה קשורה לפצע של פיברונקטין (צורת EDA), תאים מזנכימליים חיוביים ל‑Fcer1g היו מצומצמים מאוד והצלקות היו מתונות יותר. בתרבית, מגע ישיר עם מאקרופאגים הספיק להמיר פיברובלסטים דרמליים רגילים לתאים חיוביים ל‑Fcer1g ול‑PDGFRα, מה שמדגיש שמאקרופאגים יכולים לגרום ישירות למצב זה.
תוכנית צלקת משותפת בעכברים ובבני אדם
כדי לראות האם סוג תאים זה רלוונטי גם לבני אדם, החוקרים בדקו מחדש מערכי נתונים של פציעות עור אנושיות ברזולוציית תא יחיד וברקמה שלמה. הם מצאו תת‑קבוצה מזנכימלית תואמת בפצעים אנושיים שהביעה FCER1G וחותם גנטי דומה, בשיא בערך שבוע לאחר הפציעה—אותו חלון זמן שנצפה בעכברים. על פני יותר ממאה דגימות אנושיות שכללו עור תקין, פצעים חריפים, פצעים כרוניים וצלקות מורמות, תוכנית הגנים המקושרת ל‑FCER1G הפרידה בבירור רקמה פגועה וצלקתית מעור לא פגוע והייתה החזקה ביותר מוקדם לאחר הפציעה. הדמיון בין המינים מצביע על כך שמצב התא החדש המוגדר הוא מניע משומר אבולוציונית של תיקון פיברוטי.
לקראת ריפוי עדין יותר עם פחות צלקות
לסיכום, הממצאים מתארים שרשרת אירועים שלא הוערכה קודם: מאקרופאגים המגיעים מוקדם מעשירים את הפצע בפיברונקטין, פיברונקטין מסייע להמיר תאים מזנכימליים מקומיים למצב חיובי ל‑FCER1G שמתחלק במהירות, ותת‑קבוצה מיוחדת זו מפרישה עודף קולגן שהופך לרקמת צלקת. מאחר שהסרת תאים אלה בעכברים הקטינה את הצלקות מבלי לאט את סגירת הפצע, הם מהווים מטרה מפתה לטיפולים עתידיים. תרופות או ביולוגים שמפריעים לאותות היוצרים או משמרים את מצב התא הזה—אולי על ידי שינוי התנהגות המאקרופאגים או סביבת הפיברונקטין—יכולים יום אחד לסייע למטופלים להחלים מפגיעות בעור עם צלקות מינימליות ופחות בולטות.
ציטוט: Ma, X., Wang, E., Puviindran, V. et al. A macrophage-induced subpopulation of mesenchymal cells expressing Fcer1g contributes to wound-induced fibrosis. Nat Commun 17, 2686 (2026). https://doi.org/10.1038/s41467-026-69449-2
מילות מפתח: ריפוי פצעים, פיברוזיס בעור, מאקרופאגים, פיברובלסטים, יצירת צלקת