Clear Sky Science · he
קוֹופרָטיביות חיובית בין דומיינים קושרי RAS ודומיינים עשירים בציסטאין בוויסות קינטיקת ההיצמדות של RAF לממברנה דרך קשירה בצד
מדוע הריקוד המולקולרי הקטן הזה חשוב
בתוך התאים שלנו, החלטות של חיים או מוות לגבי גדילה, חלוקה ושימור מתקבלות לעיתים קרובות במשטח ממברנת התא. שחקן מרכזי בהחלטות אלה הוא החלבון RAF, שעוזר להעביר אותות גדילה ולעתים קרובות מוטה בסרטן. המחקר הזה חושף, ברזולוציה קינטית חסרת תקדים, כיצד RAF מתחבר לממברנה התאית, כמה זמן הוא שוהה שם, ולמה טלאים צפופים של חלבון אחר, RAS, יכולים לשמור על RAF פעיל למשך זמן ארוך מהצפוי.
אותות שמפגישים על פני הממברנה
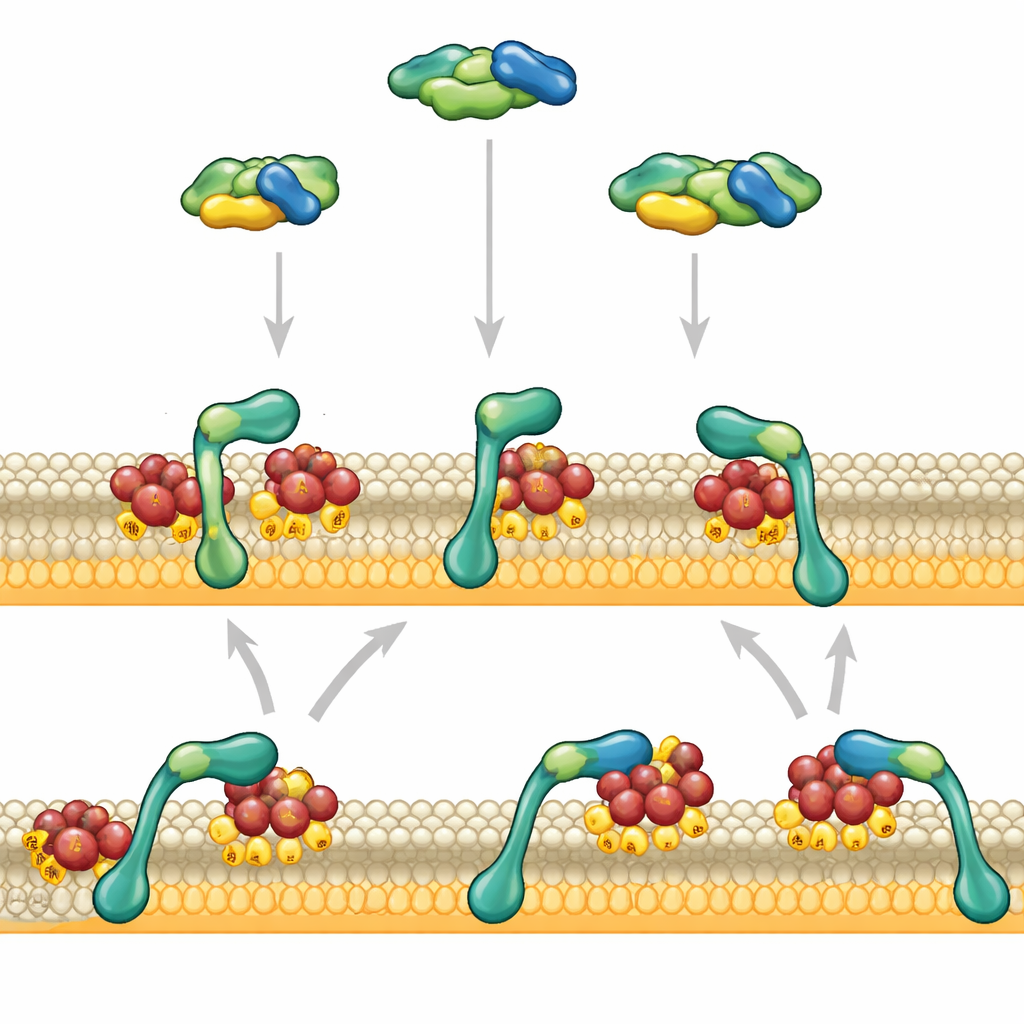
RAF פועל בציר איתות מרכזי הידוע כנתיב MAPK, שמקשר רמזים חיצוניים כמו גורמי גדילה לשינויים בפעילות הגנים. במצב מנוחה, RAF צף בפנים התא בצורתו המקופלת והמעוכבת בעצמה. הוא מופעל רק כאשר הוא פוגש את RAS, מתג מולקולרי קטן המעוגן לפני הפנימי של ממברנת התא. RAS חייב להיות במצב "פועל" ושקוע בסוג הליפידים המתאים כדי ש־RAF יגויס ויופעל. מאחר שמולקולות RAF נדירות יחסית בהשוואה לרכיבי איתות רבים אחרים, האופן המדויק שבו הן נקשרות לממברנה ומונעות שחרור מוקדם משפיע במידה רבה על כך שתא יגיב באופן חלש או חזק לאות גדילה.
שתי ידיים לתפיסת הממברנה
המחברים התרכזו בשני אזורים בקצה הקדמי של RAF: אחד שמתחבר ל‑RAS ואחד שמעדיף ליפידים בעלי מטען שלילי בממברנה. תוך שימוש בממברנות מלאכותיות וחלבונים טהורים הם צפו בחתיכות RAF בודדות שנקשרות לפני שטחים מעוטרים ב‑RAS בעזרת מיקרוסקופיה מתקדמת. כשהאזור הקשור ל‑RAS פעל לבדו, הוא נגע בממברנה לתקופה קצרה ושוחרר בתוך כשנייה. האזור האוהב ליפידים, כשלעצמו, כמעט ולא נדבק. אבל כאשר שני האזורים קושרו זה לזה, הם התנהגו בצורה שונה לחלוטין: RAF התחבר כעת בחוזקה ושהה על הממברנה במשך עשרות שניות, במיוחד כאשר הממברנה נשאה ליפידים שליליים רבים הדומים לאלה שבתאים אמיתיים.
שיתוף פעולה שמאיט את היציאה
השינוי הדרמטי הזה לא נבע מכך ש‑RAF מצא את הממברנה מהר יותר, אלא מכך שהוא עזב לאט יותר. תחילה, קטע קושר־RAS של RAF מזהה RAS מוּפעָל ומעגן את RAF על הממברנה. רק אחרי הלחיצת יד ראשונית זו האזור הקושר ליפידים מתחבר במלואו לליפידים הסובבים, מאט את התנועה הצידית של RAF ומעגן אותו חזק יותר. המגע השני הזה מחזק בתורו את האינטראקציה המקורית בין RAS ל‑RAF, ויוצר לולאת משוב חיובית בין מגעי חלבון‑חלבון ומגעי חלבון‑ליפיד. ניסויים ששינו את הקישור הקצר שמחבר בין שני האזורים הראו שהתיאום המרחבי הצמוד שלהם הוא קריטי: הארכת הקישור או הפיכתו לגמיש יותר החלישה את יכולת RAF להישאר על הממברנה.
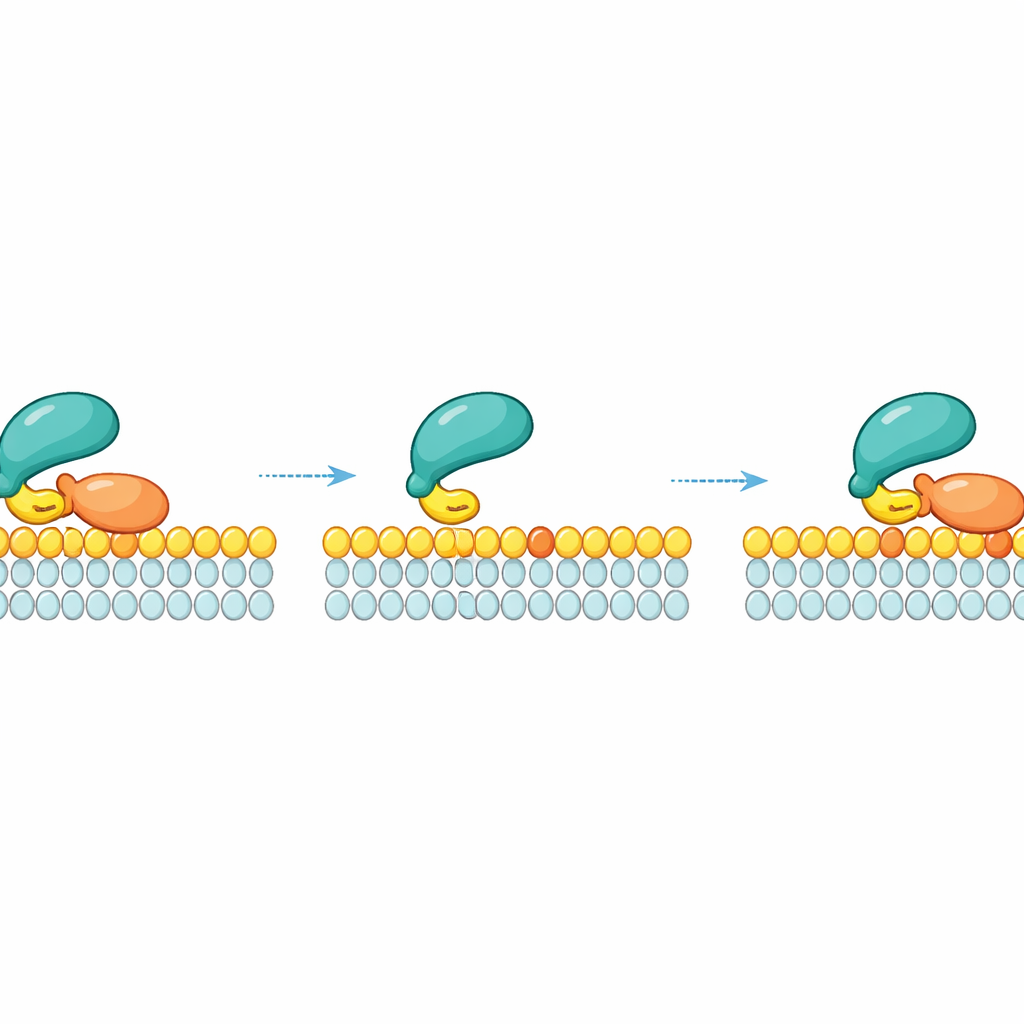
קשירה צידית: גלישה במקום נפילה
תובנה מרכזית בעבודה היא ש‑RAF אינו פשוט מתנתק לנוזל המקיף ברגע שהוא משחרר מולקולת RAS מסוימת. במקום זאת, אחרי ש‑RAS משחרר, RAF יכול להישאר בקשר זמני עם הממברנה דרך מגע הליפידים החלש שלו ולהחליק לצד. בעודו במצב החולף הזה, הוא יכול "לתפוס שוב" מולקולת RAS שכנה על אותו טלא ממברנלי. קשירה צידית זו יוצרת רשת ביטחון קינטית: בצפיפות גבוהה של RAS מקומי — כגון בנאנוקלאסטרים שבהם מולקולות RAS ארוזות בדחיסות — ל‑RAF יש הרבה הזדמנויות להתחבר שוב ל‑RAS לפני שיסחף. מדידות וסימולציות הראו שככל שצפיפות ה‑RAS המופעלת על הממברנה גבוהה יותר, כך RAF נשאר מחובר לממברנה זמן רב יותר בעקבות אותן קשירות מקומיות חוזרות.
מביקורים ממושכים להפעלה מהימנה
הזמן המוארך ש‑RAF מבלה על הממברנה נושא השלכות חשובות. הפעלת RAF אינה אירוע יחיד אלא רצף רב‑שלבי שכולל שינויים במבנה, הסרת תגי עיכוב וזיווג של שתי מולקולות RAF לדימר פעיל. המחקר מציע שרק מולקולות RAF השוהות על הממברנה זמן מספיק יכולות להשלים רצף זה — צורה של "הוכחת קינטיקה" שעוזרת לתאים להימנע מהפעלה מקרית בעקבות אותות חלשים וחולפים. על ידי חשיפת האופן שבו האינטראקציה בין קישור ל‑RAS, מעורבות בליפידים וקשירה צידית מגדירה את שהיית RAF על הממברנה, העבודה מתארת אסטרטגיה כללית שבה תאים עשויים להשתמש בריבוי אינטראקציות קטנות וחלשות על ממברנות כדי לכוונן בדיוק מסלולי איתות רבי‑עוצמה.
ציטוט: Jimenez Salinas, A., Tevdorashvili, K., Grim, J. et al. Positive cooperativity between RAS-binding and cysteine-rich domains regulates RAF membrane binding kinetics via lateral rebinding. Nat Commun 17, 2593 (2026). https://doi.org/10.1038/s41467-026-69437-6
מילות מפתח: RAS, קינאזת RAF, איתות מממברנת התא, קשירה צידית, הוכחת קינטיקה